Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

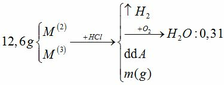
Đồng nhất dữ kiện để thuận lợi cho tính toán, bằng cách nhân đôi khối lượng H2O.
a.
BTNT H: nH2 = nH2O = 0,31 mol
=> nHCl = 0,62mol
BTKL: m kim loại + mHCl = mA + mB => 12,6 + 36,5 . 0,62 = m + 2 . 0,31 => m = 34,61g
b.
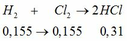
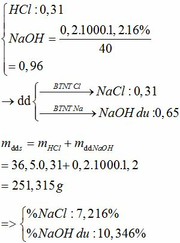

(a)- Khi cho E tác dụng với NaHCO3 sinh ra V lít khí (CO2) và muối natri của X => X là axit
- Ta thấy thể tích khí sinh ra khi cho E tác dụng với Na (khí H2) lớn hơn 0,5 lần thể tích khí khi cho E tác dụng với NaHCO3 (khí CO2) => Y là ancol
Vậy E gồm axit X, ancol Y và este Z (tạo bởi X, Y)
Giả sử V lít tương ứng với 1 (mol) khí
+ nCO2 = n-COOH = 1 (mol)
+ nH2 = 0,5n-COOH + 0,5n-OH => 0,75 = 0,5.1 + 0,5n-OH => n-OH = 0,5 (mol)
+ n hỗn hợp = 2nH2 = 1,5 mol => nX = nY = nZ = 1,5:3 = 0,5 mol
Số chức của axit X là: 1 : 0,5 = 2
Số chức của ancol Y là: 0,5 : 0,5 = 1
=> Este Z có 2 chức
* Đốt cháy muối natri của X:
Muối natri của X có dạng RO4Na2
Gọi số mol muối của X là x (mol)
BTNT Na: nNa2CO3 = n muối = x (mol)
BTNT O: 4n muối + 2nO2 = 2nCO2 + nH2O + 2nNa2CO3
=> 4x + 2nO2 = 0,03.2 + 0,02 + 3x => nO2 = 0,04 – 0,5x (mol)
BTKL: m muối + mO2 = mCO2 + mH2O + mNa2CO3
=> 1,62 + 32(0,04 - 0,5x) = 0,03.44 + 0,02.18 + 106x
=> x = 0,01 mol
=> M muối = 162 => R + 16.4 + 23.2 = 162 => R = 28 => CTPT của X là C4H6O4
* Đun nóng Y với H2SO4 đặc thu được Y1 có tỉ khối so với Y là 34/43 => phản ứng tách nước tạo anken
=> MY1 = MY – 18
=> dY1/Y = (MY-18)/MY = 34/43 => MY = 86 (C5H10O)
Mà khi đun Y1 với KMnO4/H2SO4 thu được Y2 duy nhất, không có khí thoát ra, Y2 có cấu tạo mạch thẳng và là điaxit nên Y1 có cấu tạo mạch vòng, chứa 1 liên kết đôi.
- Cấu tạo Y1:
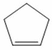
- Cấu tạo Y2: HOOC-(CH2)3-COOH
- Cấu tạo Y: 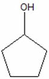
- Cấu tạo X:
HOOC-CH2-CH2-COOH hoặc HOOC-CH(CH3)-COOH
- Cấu tạo Z:
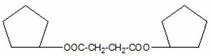
Hoặc
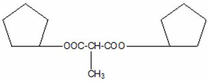
(b)Giả sử số mol mỗi chất trong ½ hỗn hợp G:
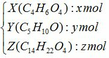
- Khối lượng của ½ hỗn hợp G:
118x + 86y + 254z = 7,8 (1)
- Đốt cháy phần 1 cần nO2 = 9,408 : 22,4 = 0,42 mol:
C4H6O4 + 3,5 O2 → 4CO2 + 3H2O
x 3,5x
C5H10O + 7O2 → 5CO2 + 5H2O
y 7y
C14H22O4 + 17,5O2 → 14CO2 + 11H2O
z 17,5z
Ta có: nO2 = 0,42 => 3,5x + 7y + 17,5z = 0,42 (2)
- Phần 2 tác dụng vừa đủ với nNaOH = 0,04.2 = 0,08 mol:
C2H4(COOH)2 + 2NaOH → C2H4(COONa)2 + 2H2O
x 2x x
C2H4(COOC5H9)2 + 2NaOH → C2H4(COONa)2 + 2C5H9OH
z 2z z 2z
nNaOH = 2nX + 2nZ => 2a + 2c = 0,08 (3)
Từ (1) (2) (3) ta có hệ phương trình:
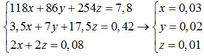
Sau phản ứng thu được:
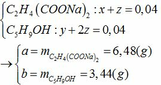

a. Đặt CT muối: \(RCO_3\)
\(RCO_3\rightarrow\left(t^o\right)RO+CO_2\) (1)
\(n_{Ba\left(OH\right)_2}=\dfrac{200.17,1}{171.100}=0,2\left(mol\right)\)
\(n_{BaCO_3}=\dfrac{29,55}{197}=0,15\left(mol\right)\)
`@` TH1: Chỉ tạo ra kết tủa
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\)
0,15 0,15 0,15 ( mol )
Theo ptr (1): \(n_{RCO_3}=n_{RO}=n_{CO_2}=0,15\left(mol\right)\)
\(M_{RCO_3}=\dfrac{21}{0,15}=140\) \((g/mol)\)
\(\Leftrightarrow R=80\) ( loại )
`@` TH2: Ba(OH)2 hết
\(Ba\left(OH\right)_2+CO_2\rightarrow BaCO_3\downarrow+H_2O\)
0,2 ( mol )
0,15 0,15 0,15 ( mol )
\(Ba\left(OH\right)_2+2CO_2\rightarrow Ba\left(HCO_3\right)_2\)
0,05 0,1 ( mol )
Theo ptr (1): \(n_{RCO_3}=n_{RO}=n_{CO_2}=0,15+0,1=0,25\left(mol\right)\)
\(M_{RCO_3}=\dfrac{21}{0,25}=84\) \((g/mol)\)
\(\Leftrightarrow R=24\) `->` R là Mg
\(n_{MgO}=0,25.\left(24+16\right)=10\left(g\right)\)
b.\(n_{MgCO_3}=\dfrac{4,2}{84}=0,05\left(mol\right)\)
\(n_{HCl}=0,05.3=0,15\left(mol\right)\)
\(m_{HCl}=50.1,15=57,5\left(g\right)\)
\(MgCO_3+2HCl\rightarrow MgCl_2+CO_2+H_2O\)
0,05 < 0,15 ( mol )
0,05 0,1 0,05 0,05 ( mol )
\(m_{ddspứ}=4,2+57,5-0,05.44=59,5\left(g\right)\)
\(\left\{{}\begin{matrix}\%m_{MgCl_2}=\dfrac{0,05.95}{59,5}.100=7,98\%\\\%m_{HCl\left(dư\right)}=\dfrac{\left(0,15-0,1\right).36,5}{59,5}.100=3,06\%\end{matrix}\right.\)

a) Nhận xét: 33,84g X > 16g rắn → kim loại còn dư.
Chú ý: sau một thời gian ám chỉ các chất tham gia đều dư.
Giả sử số mol của Mg, Fe lần lượt là x, y
Tăng giảm khối lượng: (64 – 24) . x + (64 – 56) . y = 38,24 – 33,84 (1)
Chất rắn bao gồm MgO: x; Fe2O3: 0,5y; CuO: a – x – y
=> 40x + 160 . 0,5y + 80(a – x – y) = 16 (2)
Từ (1) và (2) => 10a + y = 2,55
amax <=> y = 0 => amax = 0,255
b) giá trị a đạt max thì Fe chưa tham gia pứ.
Giả sử số mol Mg dư là: z (mol) 19,12g Z cho 0,48 mol SO2 → 38,24g Z cho 0,96 mol SO2
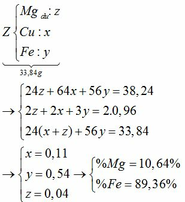

Biết 1 lít hỗn hợp A ở dạng khí nặng gấp hai lần 1 lít khí C 2 H 6 ở cùng điều kiện.
⇒ n A = n C 2 H 6 ⇒ M A = 2 M C 2 H 6
(cùng điều kiện nên tỉ lệ thể tích chính là tỉ lệ số mol)
Ba chất có cùng công thức phân tử ⇒ có cùng khối lượng mol phân tử : M = 2.30 = 60 (gam/mol). Khi đốt cháy hỗn hợp A thu được CO 2 , H 2 O → công thức phân tử của các chất có dạng C x H y O z
Phương trình hoá học
C x H y O z + (x + y/4 - z/2) O 2 → x CO 2 + y/2 H 2 O
CO 2 + Ca OH 2 → Ca CO 3 + H 2 O
Ta có : n CO 2 = n CaCO 3 = 15/100 = 0,15mol
Theo định luật bảo toàn khối lượng, ta có :
m A + m O = m CO 2 + m H 2 O
⇒ 3 + 7,2 = 0,15 x 44 + m H 2 O ⇒ m H 2 O = 3,6g
n A = 3/60 = 0,05mol; n CO 2 = 0,05x = 0,15 ⇒ x = 3
n H 2 O = 0,05y/2 = 3,6/18 ⇒ y = 8
M A = 12x + y + 16z = 60 ⇒ z = 1 ⇒ ông thức phân tử của A là C 3 H 8 O
Công thức cấu tạo của ba chất là : CH 3 CH 2 CH 2 OH
CH 3 CHOH CH 3
CH 3 -O- CH 2 CH 3

a, \(n_{CO_2}=\dfrac{1,7353}{24,79}=0,07\left(mol\right);n_{NaOH}=\dfrac{6,4}{40}=0,16\left(mol\right)\)
PTHH: CO2 + 2NaOH → Na2CO3 + H2O
Mol: 0,07 0,07 0,07
Ta có: \(\dfrac{0,07}{1}< \dfrac{0,16}{2}\) ⇒ CO2 hết, NaOH dư
b, \(m_{Na_2CO_3}=0,07.106=7,42\left(g\right)\)
c, \(m_{NaOHdư}=\left(0,16-0,07\right).40=3,6\left(g\right)\)
\(\Rightarrow m_{muối}=7,42+3,6=11,02\left(g\right)\)


BTKL: mD + mNaHCO3 = mCO2 + mE
mD + 179,88 = 44.0,2 + 492 => mD = 320,92
BTKL: mMg + mddHCl = mH2 + mD
=> 24 . 0,4 + mddHCl = 2 . 0,4 + 320,92 => mddHCl = 312,12
=> C%HCl = 11,69%
Theo giả thiết ta có :
Khối lượng sản phẩm khí = 12,12 - 2,4 = 9,72(g)
Khối lượng dung dịch muối thu được =100 + 9,72 = 109,72 (g)
Gọi công thức muối trong dung dịch là NanX (muối của Na với gốc axit X hoá trị n)
nNaOH = \(\dfrac{100.3,6}{100.40}=0,09\left(mol\right)\)
Số mol NanX = \(\dfrac{0,09}{n}mol\)
Khối lượng NanX = \(\dfrac{\left(23.n+X\right).0,09}{n}\)= \(\dfrac{109,72.6,972}{100}\approx7,65\) ⇒ X = 62n
Biện luận :
Sản phẩm khí có NO2 và O2
\(4NO2+O2+4NaOH->4NaNO3+2H2O\)
0,09mol...0,0225mol...0,09mol....0,09mol
mNO2 + mO2 = 46.0,09+ 32.0,0225 = 4,86 (g) < 9,72 (g)
Như vậy sản phẩm khí phải có thêm H2O :
=>H2O = \(\dfrac{9,72-4,86}{18}=0,27\left(mol\right)\)công thức muối A: M(NO3) m.kH2O
2M(NO3)m.kH2O \(-^{t0}->\) M2Om + 2mNO2 + m/2O2 + 2kH2O
nM2Om = nNO2/2m = 0,09/2m = 0,045/m
mM2Om = \(\dfrac{\left(2M+16\right)0,045}{m}=2,4\) ⇒ M = \(\dfrac{56m}{3}\)
Biện luận :
nFe(NO3)3.kH2O = 0,09/3 = 0,03(mol)
k = 0,27/0,03 = 9 ⇒CTHH của muối là : Fe(NO3)3.9H2O