Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử có 1 mol Zn phản ứng:
A. Zn + Ni(NO3)2 → Zn(NO3)2 + Ni ⇒ mZn(NO3)2 > mNi(NO3)2 ⇒ mdung dịch tăng
B. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag ⇒ mZn(NO3)2 < mAgNO3 ⇒ mdung dịch giảm
C. 3Zn + 2Fe(NO3)3 → 3Zn(NO3)2 + 2Fe ⇒ mZn(NO3)2 > mFe(NO3)3 ⇒ mdung dịch tăng
D. Zn + Cu(NO3)2 → Zn(NO3)2 + Cu ⇒ mZn(NO3)2 > mCu(NO3)2 ⇒ mdung dịch tăng
Chọn đáp án B

Giải thích: Đáp án A
TQ : nZn + 2Xn+ -> nZn2+ + 2X
=>mdd giảm = mthanh KL tăng = 2X – 65n > 0
=> X > 32,5n
Vậy X là Ag thỏa mãn

Đặt nAgNO3 = x mol; nCu(NO3)2 = y mol ⇒ a = 170x + 188y và ∑nNO3– = x + 2y mol.
Cu dư + X → Y
⇒ Y chứa Cu(NO3)2 ⇒ nCu(NO3)2 = 0,5x + y ⇒ b = 94x + 188y.
Fe dư + Y → Z ||⇒ Z chứa Fe(NO3)2 ⇒ nFe(NO3)2 = 0,5x + y ⇒ c = 90x + 180y.
2b = a + c ⇒ 2 × (94x + 188y) = (170x + 188y) + (90x + 180y)
⇒ 72x =Đặt nAgNO3 = x mol; nCu(NO3)2 = y mol ⇒ a = 170x + 188y và ∑nNO3– = x + 2y mol.
Cu dư + X → Y
⇒ Y chứa Cu(NO3)2 ⇒ nCu(NO3)2 = 0,5x + y ⇒ b = 94x + 188y.
Fe dư + Y → Z
⇒ Z chứa Fe(NO3)2 ⇒ nFe(NO3)2 = 0,5x + y ⇒ c = 90x + 180y.
2b = a + c ⇒ 2 × (94x + 188y) = (170x + 188y) + (90x + 180y)
⇒ 72x = 8y ⇒ y = 9x
⇒ %mCu(NO3)2 = 188 × 9x ÷ (170x + 188 × 9x) × 100% = 90,87%. 8y
⇒ y = 9x ⇒ %mCu(NO3)2 = 188 × 9x ÷ (170x + 188 × 9x) × 100% = 90,87%.
Đáp án C

Chọn đáp án D


Dd sau phản ứng thu được 3 muối và không có AgNO3 => tất cả Ag+ chuyển hết thành Ag
BTNT Ag => nAg = nAgNO3 = 0,6 (mol)
Khối lượng giảm = mAg sinh ra – mFe, Cu
=> 50 = 0,6.108 – m
=> m = 14,8 (g)

Đáp án B
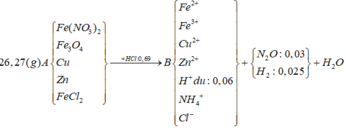
Tính nhanh được nN2O = 0,03 mol và nH2 = 0,025 mol; nFe = 0,09 mol
Do khi cho dung dịch AgNO3 dư vào B thấy có khí NO thoát ra nên B có chứa HCl dư
nHCl dư = nH+ dư = 4nNO = 0,06 mol (do 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O)
=> nHCl pu với A = 0,69 – 0,06 = 0,63 mol
Ta có: A + HCl → muối + khí + H2O
BTKL => mH2O = mA + mHCl pư với A – m muối – m khí = 26,27 + 0,63.36,5 – 0,03.44 – 0,025.2 = 4,5 (g)
=> nH2O = 0,25 mol
BT “H”: nNH4+ = (nHCl – nH+ dư - 2nH2 – 2nH2O):4 = (0,69-0,06-2.0,025-2.0,25):4 = 0,02 mol
BT “N”: nFe(NO3)2 = (2nN2O + nNH4+):2 = (2.0,03 + 0,02):2 = 0,04 mol
BT “O”: 6nFe(NO3)2 + 4nFe3O4 = nN2O + nH2O => 6.0,04+4nFe3O4 = 0,03+0,25 => nFe3O4 = 0,01 mol
BT “Fe”: nFe = nFe(NO3)2 + 3nFe3O4 + nFeCl2 => 0,09 = 0,04 + 3.0,01 + nFeCl2 => nFeCl2 = 0,02 mol
Khi cho B + AgNO3 dư:


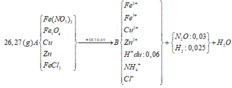
Tính nhanh được nN2O = 0,03 mol và nH2 = 0,025 mol; nFe = 0,09 mol
Do khi cho dung dịch AgNO3 dư vào B thấy có khí NO thoát ra nên B có chứa HCl dư
nHCl dư = nH+ dư = 4nNO = 0,06 mol (do 3Fe2+ + 4H+ + NO3- → 3Fe3+ + NO + 2H2O)
=> nHCl pu với A = 0,69 – 0,06 = 0,63 mol
Ta có: A + HCl → muối + khí + H2O
BTKL => mH2O = mA + mHCl pư với A – m muối – m khí = 26,27 + 0,63.36,5 – 0,03.44 – 0,025.2 = 4,5 (g)
=> nH2O = 0,25 mol
BT “H”: nNH4+ = (nHCl – nH+ dư - 2nH2 – 2nH2O):4 = (0,69-0,06-2.0,025-2.0,25):4 = 0,02 mol
BT “N”: nFe(NO3)2 = (2nN2O + nNH4+):2 = (2.0,03 + 0,02):2 = 0,04 mol
BT “O”: 6nFe(NO3)2 + 4nFe3O4 = nN2O + nH2O => 6.0,04+4nFe3O4 = 0,03+0,25 => nFe3O4 = 0,01 mol
BT “Fe”: nFe = nFe(NO3)2 + 3nFe3O4 + nFeCl2 => 0,09 = 0,04 + 3.0,01 + nFeCl2 => nFeCl2 = 0,02 mol
Khi cho B + AgNO3 dư:
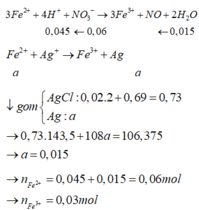

Đáp án B

Giải thích:
Thứ tự xuất hiện trong dãy điện hóa của các cặp oxi hóa khử: Zn2+/Zn; Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+; Ag+/Ag.
Tính oxi hóa: Ag+ > Fe3+ > Cu2+ > Fe2+ > Zn2+. → Dung dịch chứa 2 muối
→ chứa 2 cation kim loại → Zn2+ và Fe2+
Đáp án C

Giải thích:
Thứ tự xuất hiện trong dãy điện hóa của các cặp oxi hóa khử: Zn2+/Zn; Fe2+/Fe; Cu2+/Cu; Fe3+/Fe2+; Ag+/Ag.
Tính oxi hóa: Ag+ > Fe3+ > Cu2+ > Fe2+ > Zn2+. → Dung dịch chứa 2 muối
→ chứa 2 cation kim loại → Zn2+ và Fe2+
Đáp án C

Chọn đáp án B
Giả sử có 1 mol Zn phản ứng:
A. Zn + Ni(NO3)2 → Zn(NO3)2 + Ni ⇒ mZn(NO3)2 > mNi(NO3)2 ⇒ mdung dịch tăng
B. Zn + 2AgNO3 → Zn(NO3)2 + 2Ag ⇒ mZn(NO3)2 < mAgNO3 ⇒ mdung dịch giảm
C. 3Zn + 2Fe(NO3)3 → 3Zn(NO3)2 + 2Fe ⇒ mZn(NO3)2 > mFe(NO3)3 ⇒ mdung dịch tăng
D. Zn + Cu(NO3)2 → Zn(NO3)2 + Cu ⇒ mZn(NO3)2 > mCu(NO3)2 ⇒ mdung dịch tăng