Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

vì nhôm (Al) hóa trị 3 nên hợp chất có dạng :\(Al_aX_3\) gồm 5 nguyên tử \(\Rightarrow a=5-3=2\) \(Al_2X_3\)
\(\Rightarrow\) X có hóa trị 2
\(M=27.2+X.3=150\)
\(\Rightarrow X=32\) => Lưu huỳnh ( S) thõa mãn hóa trị 2.
CTHH của hợp chất \(Al_2S_3\) ( nhóm sulfua ) .
công thức hh dạng: AlaXb mà 1 ptử của nó có 5 ngtử
ta có Al hóa trị 3 nên có tối đa 2 ngtử Al trong AlaXb
theo bài ra ta có: 27.2 + 3.X =150 => X = 32 = S(lưu huỳnh)
cthh là Al2S3

Al luôn hóa trị 3, các NTHH có hóa trị từ 1->7
+ TH1: X(I)=> có 4 nguyên tử (loại)
+TH2:X(II)=> có 5 nguyên tử(chọn)
+TH3:X(III)=>có 2 nguyên tử (loại)
+TH4:X(IV)=>có 7 nguyên tử(loại)
+TH5:X(V)=> có 8 nguyên tử (loại)
+TH6:X(VI)=> có 3 nguyên tử (loại)
+TH7LX(VII)=>có 10 nguyên tử(loại)
=> Al2X3
ta có:
150=2.27+3.X=54+3X
=>X=32=>X là S

CTTQ: XaOb
O có hóa trị II => a = 2
=> b = 7-2=5
=> CTTQ: X2O5
Theo đề bài ta có:
2X16.52X16.5 =11,2911,29
=> X = 31
=> X: P (photpho)
=> CTHH: P2O5
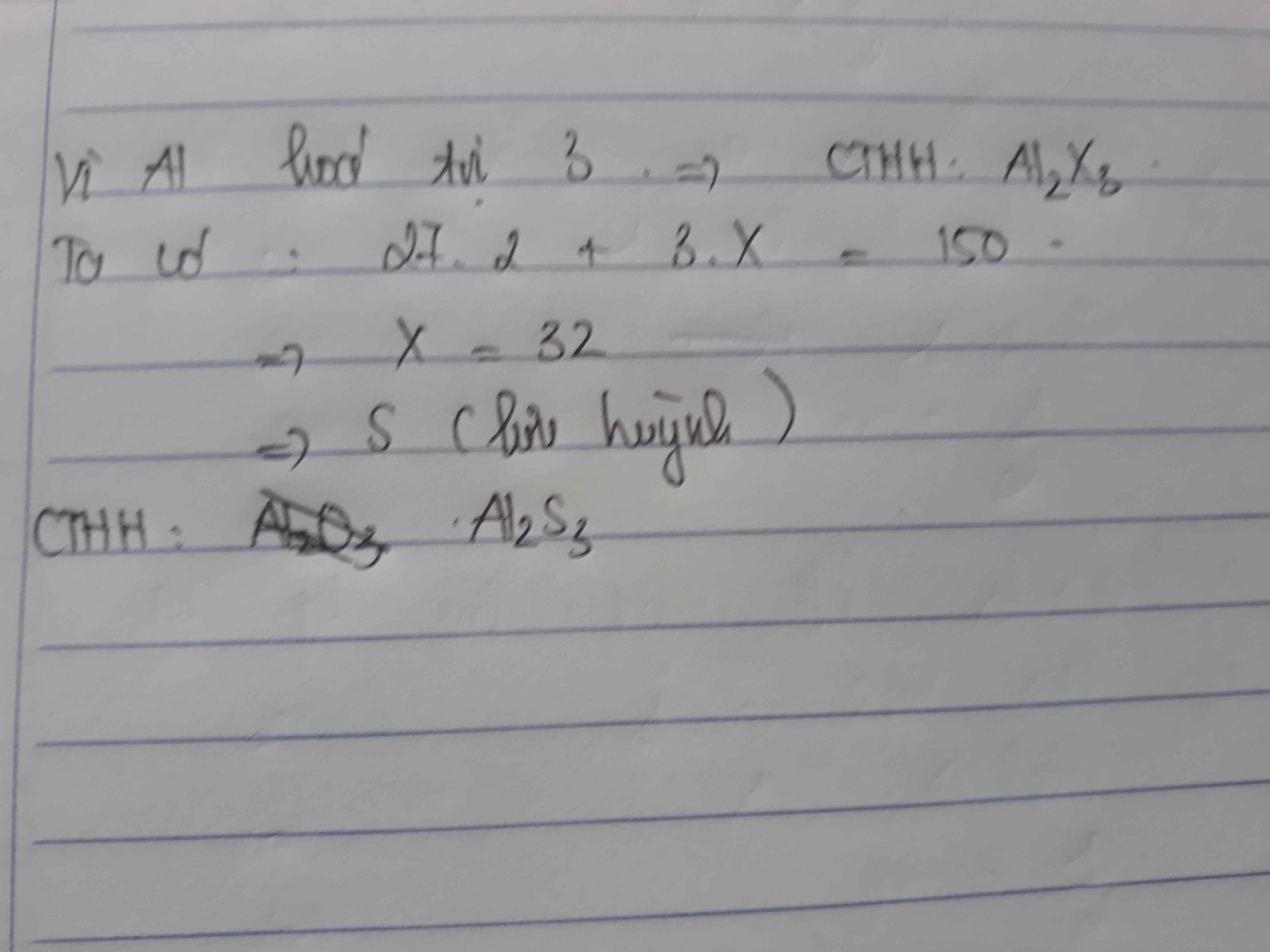
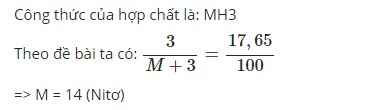
Mik ko hiểu đề lắm
đọc xong đề tự hỏi mình có bị mất gốc hóa ko ._.