Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(2KClO_3\rightarrow\left(t^o,MnO_2\right)2KCl+3O_2\)
0,4 0,6 ( mol )
\(m_{KClO_3}=0,4.122,5=49g\)

\(Coi\ n_{O_2} = 1(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 +O_2\\ n_{KMnO_4} = 2n_{O_2} = 2(mol)\\ m_{KMnO_4} = 2.158 = 316(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{KClO_3} = \dfrac{2}{3}(mol)\\ m_{KClO_3} = \dfrac{2}{3}.122,5= 81,6(gam)\\ m_{KClO_3} < m_{KMnO_4} (81,6 <316)\\ \)

PTHH : \(2KClO_3\rightarrow t^0\rightarrow2KCl+3O_2\uparrow\)
Số mol KClO3 tham gia phản ứng : \(n_{KClO_3}=\frac{m_{KClO_3}}{M_{KClO_3}}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
1. Theo PTHH : Cứ 2 mol KClO3 tham gia phản ứng thì tạo thành 3 mol O2
=> Cứ 0,1 mol KClO3 tham gia phản ứng thì tạo thành 0,15 mol O2
=> Thể tích khí O2 thu được ở đktc là : \(V_{O_2}=n_{O_2}\times22,4=0,15\times22,4=3,36\left(l\right)\)
2. Số mol O2 tạo thành sau phản ứng : \(n_{O_2}=\frac{m_{O_2}}{M_{O_2}}=\frac{48}{32}=1,5\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 1,5 mol O2 tạo thành sau phản ứng thì có 1 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=1\cdot126,9=126,9\left(g\right)\)
3. Số mol O2 thu được sau phản ứng ở đktc : \(n_{O_2}=\frac{V_{O_2}}{22,4}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo PTHH : Cứ 3 mol O2 tạo thành sau phản ứng thì có 2 mol KClO3 tham gia phản ứng
=> Cứ 0.125 mol O2 tạo thành sau phản ứng thì có 1/12 mol KClO3 tham gia phản ứng
=> Khối lượng KClO3 cần nhiệt phân : \(m_{KClO_3}=n_{KClO_3}\times M_{KClO_3}=\frac{1}{12}\cdot126,9=10.575\left(g\right)\)
Quỳnh•Sinestrea⁰⁷ : đừng làm hóa nữa, làm toàn nhầm thôi đấy
1. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
. \(n_{KClO_3}=\frac{12,25}{122,5}=0,1\left(mol\right)\)
Theo pthh : \(n_{O_2}=\frac{3}{2}n_{KClO_3}=0,15\left(mol\right)\)
=> \(V_{O_2}=0,15\cdot22,4=3,36\left(l\right)\)
2. PTHH : \(2KClO_3-t^o->2KCl+3O_2\)
\(n_{O_2}=\frac{48}{32}=1,5\left(mol\right)\)
Theo pthh : \(n_{KClO_3}=\frac{2}{3}n_{O_2}=1\left(mol\right)\)
=> \(m_{KClO_3}=1\cdot122,5=122,5\left(g\right)\)
3. PTHH : \(2KMnO_4-t^o->K_2MnO_4+MnO_2+2O_2\)
\(n_{O_2}=\frac{2,8}{22,4}=0,125\left(mol\right)\)
Theo pthh : \(n_{KMnO_4}=n_{O_2}=0,125\left(mol\right)\)
=> \(m_{KMnO_4}=0,125\cdot158=19,75\left(g\right)\)

\(a)\ n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 0,3.2 = 0,6(mol)\\ \Rightarrow m_{KMnO_4} = 0,6.158 = 94,8(gam)\\ b)\ n_{KClO_3} = \dfrac{24,5}{122,5} = 0,2(mol)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{O_2} = \dfrac{3}{2}n_{KClO_3} = 0,3(mol)\\ \Rightarrow m_{O_2} = 0,3.32 = 9,6(gam)\)
a) nO2 = \(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Pt: \(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
Theo pt: \(n_{KMnO_4}=2nO_2=0,6\left(mol\right)\Rightarrow m_{KMnO_4}=0,6.158=94,8g\)
b) \(n_{KClO_3}=\dfrac{24,5}{122,5}=0,3\left(mol\right)\)
\(Pt:2KClO_3\rightarrow2KCl+3O_2\)
\(nO_2=\dfrac{3}{2}n_{KClO_3}=0,45\left(mol\right)\Rightarrow mO_2=0,45.32=14,4g\)

\(n_{O_2}=\dfrac{3.36}{22.4}=0.15\left(mol\right)\)
\(2KMnO_4\underrightarrow{t^0}K_2MnO_4+MnO_2+O_2\)
\(0.3............................................0.15\)
\(m_{KMnO_4}=0.3\cdot158=47.4\left(g\right)\)

a)6KMnO4--->3K2MnO4 + 3MnO2 + 3O2 (1)
2KClO3---> 2KCl + 3O2 (2)
Dựa vào phương trình trên ---> thu cùng lượng O2, KMnO4 cần nhiều số mol hơn, và khối lượng nhiều hơn.
b)6KClO3-->6KCl + 9O2 (3)
1,3--->Cùng số mol, KClO3 cho nhiều O2 hơn.
c)Giả sử cả 2 chất cùng có khối lượng là 100g
nKMnO4=50/79(mol)
nKClO3=40/49
Thay vào các phương trình phản ứng tính ra mO2
Cụ thể: KMnO4 cho ra 800/79 (g) O2
KClO3 cho ra 1920/49 (g) O2
---> Cùng m thì KClO3 cho nhiều g O2 hơn.
d) Giả sử cần điều chế 32 g O2
--->nO2=1 mol
--->nKMnO4=2 mol--->mKMnO4=316g
và nKClO3=2/3 mol--->nKClO3=245/3g
Ta có:
-1000g KMnO4 <=> 200000đ
316 g=========>63200đ
-1000g KClO3 <=> 300000đ
245/3g========> 24500đ
Vậy để điều chế cùng lượng O2, KClO3 có giá thành rẻ hơn.

\(Coi\ n_{O_2} = 1(mol)\\ 2KMnO_4 \xrightarrow{t^o} K_2MnO_4 + MnO_2 + O_2\\ n_{KMnO_4} = 2n_{O_2} = 2(mol) \\ m_{KMnO_4} = 2.158 =316(gam)\\ 2KClO_3 \xrightarrow{t^o} 2KCl + 3O_2\\ n_{KClO_3} = \dfrac{2}{3}n_{O_2} = \dfrac{2}{3}(mol)\\ m_{KClO_3} = \dfrac{2}{3}.122,5 = 81,6(gam)\\ \Rightarrow m_{KMnO_4} > m_{KClO_3}(316<81,6)\)
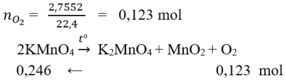

\(n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
2KMnO4 \(\underrightarrow{t^o}\) K2MnO4 + O2 + MnO2
de: 1,2 \(\leftarrow\) 0,6
2KClO3 \(\underrightarrow{t^o}\) 2KCl + 3O2
de: 0,4 \(\leftarrow\) 0,6
\(m_{KMnO_4}=1,2.158=189,6g\)
\(m_{KClO_3}=0,4.122,5=49g\)
=> nhiệt phân KClO3 cần khối lượng ít hơn
Ta có :
nO2 = 13,44 : 22,4 = 0,6 (mol)
PTHH :
2KMnO4(1,2) ----> K2MnO4 + MnO2 + O2(0,6)
=> nKMnO4 = 0,6 . 2 = 1,2 (mol)
=> mKMnO4 (PÚ) = 1,2 . (39 + 55 + 64) = 189,6 (g)
PTHH :
2KClO3(0,4) ----> 2KCl + 3O2(0,6)
=> nKClO3 = 0,6 : 3 . 2 = 0,4 (mol)
=> mKClO3 = 0,4 . (39 + 35,5 + 48) = 49 (g)
Như vậy muốn có 13,44 lít khí O2 (đktc) thì nhiệt phân KClO3 cần khối lượng ít hơn