Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, PTHH: Fe2O3 + 6 HCl => 2FeCl3 + 3H2O.
Ta có: nFe2O3 = 0.1 mol.
Theo tỉ lệ pt ta có: n HCl = 6nFe2O3 = 0.6 mol
=> a= 0.6/ 0.4 = 1.5M
b, dd sau pư là FeCl3: n FeCl3 = 2nFe2O3 = 0.2 mol => CM=0.2/ 0.4 = 0.5 mol.

1. Gọi cthc: Fe2Ox
Pt: \(Fe_2O_x+2xHCl\rightarrow2FeCl_x+xH_2O\)
112 +16x 112 + 71x
14,4 g 25,4g
\(\Rightarrow\dfrac{112+16x}{14,4}=\dfrac{112+71x}{25,4}\)
\(\Rightarrow x=2\)
Vậy cthc: FeO
Đây là 4 bài chứ 3 bài gì
Bài 20:
Đặt CTDC của oxit sắt cần tìm là \(Fe_xO_y\)
Khi Hòa tan 14,4g một oxit sắt trong dung dịch HCl dư thì:
PTHH: \(Fe_xO_y+2yHCl\rightarrow xFeCl_{\dfrac{2y}{x}}+yH_2O\)
\(n_{FeCl_{\dfrac{2y}{x}}}=\dfrac{25,4}{56+35,5.\dfrac{2y}{x}}\left(mol\right)\)
\(n_{Fe_xO_y}=\dfrac{14,2}{56x+16y}\left(mol\right)\)
\(TheoPTHH:n_{Fe_xO_y}.x=n_{FeCl_{\dfrac{2y}{x}}}\)
\(\Leftrightarrow\dfrac{14,4x}{56x+16y}=\dfrac{25,4}{56+\dfrac{71y}{x}}\)
\(\Leftrightarrow616x=616y\)
\(\Rightarrow\dfrac{x}{y}=\dfrac{1}{1}\)
\(\Rightarrow CTHH:FeO\)
Bài 21: Đề sai rồi nhé! Kim loại này không thể có hóa trị III. (Ra Fe đó)
Bài 22: Câu b phải là nồng độ phần trăm thôi,không có nồng độ % klg đâu :>
\(Zn\left(0,2\right)+CuCl_2\rightarrow ZnCl_2+Cu\left(0,2\right)\)
\(n_{Zn}=0,2\left(mol\right)\)
\(m_{CuCl_2}=\dfrac{67,5.60}{100}=40,5\left(g\right)\)\(\Rightarrow n_{CuCl_2}=0,3\left(mol\right)\)
So sánh: \(\dfrac{n_{Zn}}{1}=0,2< \dfrac{n_{CuCl_2}}{1}=0,3\)
=> CuCl2 dư sau phản ứng, chon nZn để tính.
Theo PTHH: \(n_{Cu}=0,2\left(mol\right)\)\(\Rightarrow m_{Cu}=0,2.64=12,8\left(g\right)\)
Dung dịch sau pứ: \(\left\{{}\begin{matrix}ZnCl_2:0,2\left(mol\right)\\CuCl_2\left(dư\right):0,1\left(mol\right)\end{matrix}\right.\)
\(m_{ddsau}=13+67,5-12,8=67,7\left(g\right)\)
\(\Leftrightarrow\left\{{}\begin{matrix}C\%_{ZnCl_2}=\dfrac{0,2.136.100}{67,7}=40,18\%\\C\%_{CuCl_2}\left(dư\right)=\dfrac{0,1.135.100}{67,7}=19,94\%\end{matrix}\right.\)
Bài 23:
Gọi a, b lần lượt là số mol của Mg và Fe có trong hỗn hợp
\(\Rightarrow24a+56b=4\left(I\right)\)
\(Mg\left(a\right)+2HCl\rightarrow MgCl_2+H_2\left(a\right)\)
\(Fe\left(b\right)+2HCl\rightarrow FeCl_2+H_2\left(b\right)\)
\(n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow a+b=0,1\left(II\right)\)
Từ (I) và (II) \(\Rightarrow\left\{{}\begin{matrix}a=0,05\\b=0,05\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Mg}=\dfrac{0,05.24.100}{4}=30\%\\\%m_{Fe}=100\%-30\%=70\%\end{matrix}\right.\)

Ở phần b, nếu trong hỗn hợp đầu thì phải là % khối lượng mỗi oxit chứ nhỉ? Và ở phần c phải là 1,1 g/ml chứ không phải g/mol bạn nhé!


Bạn tham khảo link nhé!
một hỗn hợp gồm Fe2O3 và MgO nặng 16g được hòa tan hết trong udng dịch axit HCL sau đó đem cô cạn dung dịch thu được 35,25g muối khan a) viết các PTHH b) tính thành phần % khối lượng mỗi oxit trong hỗn hợp ban đầu >< giúp với ạ - Hoc24

nZn = 6,5 : 65 = 0,1 (mol)
pthh: Zn+2HCl -> ZnCl2 + H2
0,1 0,1 0,1
=> mHCl = 0,1 . 36,5 = 3,65(g)
pthh : CuO + H2 -to-> Cu + H2O
0,1 0,1
=> mCu = 0,1 . 64 = 6,4 (g)

mk viết nhầm. HSO là H2SO4. BaCl là BaCl2.
NaCO là Na2CO3 . CO là khí CO2

Gọi oxit kim loại cần tìm là \(M_2O_3\).
a) \(M_2O_3+6HCl\rightarrow2MCl_3+3H_2O\left(1\right)\)
b) \(n_{HCl}=C_M\cdot V=1\cdot0,24=0,24\left(mol\right)\)
Theo pthh \(\left(1\right):n_{M_2O_3}=\dfrac{1}{6}n_{HCl}=\dfrac{0,24}{6}=0,04\left(mol\right)\)
\(\Rightarrow M_{M_2O_3}=\dfrac{m}{n}=\dfrac{6,4}{0,04}=160\left(g\right)\\ \Rightarrow2M_M+48=160\\ \Rightarrow2M_M=112\\ \Rightarrow M_M=56\\ \Rightarrow M\text{ }là\text{ }kim\text{ }\text{loại }Fe\left(Sắt\right)\)
\(\Rightarrow M_xO_y=Fe_2O_3\)
c) Gọi CTHH của tinh thể là \(FeCl_3.nH_2O\)
\(pthh:Fe_2O_3+6HCl\rightarrow2FeCl_3+3H_2O\left(2\right)\)
Theo pthh \(\left(2\right):n_{FeCl_3}=\dfrac{1}{3}n_{HCl}=\dfrac{0,24}{3}=0,08\left(mol\right)\)
\(\Rightarrow M_{FeCl_3.nH_2O}=\dfrac{m}{n}=\dfrac{15,88}{0,08}=198,5\left(g\right)\\ \Rightarrow162.5+18n=198,5\\ \Rightarrow18n=36\\ \Rightarrow n=2\)
\(\Rightarrow FeCl_3.nH_2O=FeCl_3.2H_2O\)

- Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Mg}=b\left(mol\right)\end{matrix}\right.\Rightarrow27a+24b=10,2\left(1\right)\)
Khí thu được sau p/ứ là khí H2: \(n_{H_2}=\dfrac{11,2}{22,4}=0,5\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
2 3 (mol)
a 3/2 a (mol)
\(Mg+2HCl\rightarrow MgCl_2+H_2\uparrow\)
1 1 (mol)
b b (mol)
Từ hai PTHH trên ta có: \(\dfrac{3}{2}a+b=0,5\left(2\right)\)
\(\left(1\right),\left(2\right)\) ta có hệ: \(\left\{{}\begin{matrix}27a+24b=10,2\\\dfrac{3}{2}a+b=0,5\end{matrix}\right.\)
Giải ra ta có \(\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,2\left(mol\right)\end{matrix}\right.\)
a) \(\%Al=\dfrac{m_{Al}}{m_{hh}}.100\%=\dfrac{0,2.27}{10,2}.100\%\approx52,94\%\)
\(\%Mg=100\%-\%Al=100\%-52,94=47,06\%\)
b)
\(3H_2+Fe_2O_3\rightarrow^{t^0}2Fe+3H_2O\)
3 1 2 (mol)
0,5 1/6 1/3 (mol)
\(m_{Fe}=\dfrac{1}{3}.56=\dfrac{56}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(pứ\right)}=\dfrac{1}{6}.160=\dfrac{80}{3}\left(g\right)\)
\(m_{Fe_2O_3\left(dư\right)}=60-m_{Fe}=60-\dfrac{56}{3}=\dfrac{124}{3}\left(g\right)\)
\(a=\dfrac{124}{3}+\dfrac{80}{3}=68\left(g\right)\)
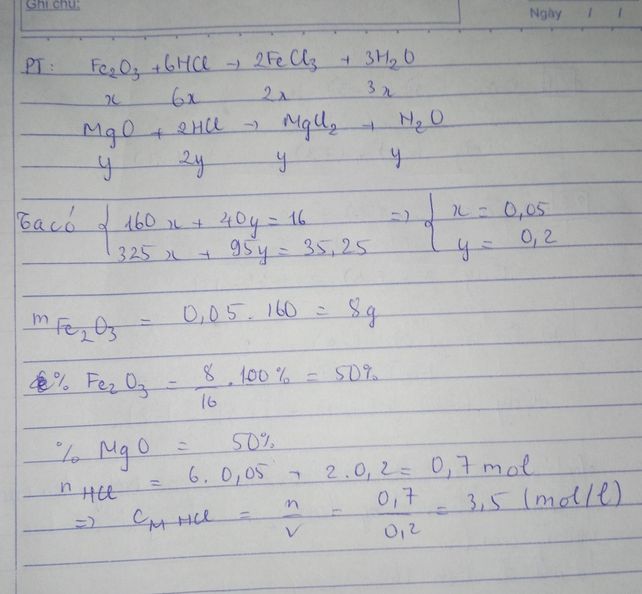
a)
Gọi CTHH của đồng là $Cu_2O_n$
Ta có : $\%O = \dfrac{16n}{64.2 + 16n}.100\% = 20\%$
$\Rightarrow n = 2$
Vậy oxi là $CuO$
$CuO + 2HCl \to CuCl_2 + H_2O$
$n_{CuO} = \dfrac{22}{80} = 0,275(mol)$
$n_{HCl} = 2n_{CuO} = 0,55(mol)$
$a\% = \dfrac{0,55.36,5}{500.11,2}.100\% = 0,35\%$
b)
$C_{M_{CuCl_2}} = \dfrac{0,275}{0,5} = 0,55M$