Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ở điều kiện chuẩn có p0 = 1atm m = V0.
Ở O0C , áp suất 150atm m = V ρ .
Khối lượng không đổi:
V 0 . ρ 0 =V . ρ ⇒ V = ρ 0 . V 0 ρ
Mà V0 ρ o = V ρ
⇒ ρ = p . ρ 0 p 0 = 214 , 5 k g / m 3

Biết ρ 0 = m/ V 0 và ρ = m/V ⇒ ρ 0 V 0 = ρ V
Mặt khác p 0 V 0 = pV
(vì nhiệt độ của khí bằng nhiệt độ ở điều kiện chuẩn).
Từ (1) và (2) suy ra:
ρ = ρ 0 p/ p 0 = 1,43.150/1 = 214,5(kg/ m 3 )
Và m = 214,5. 10 - 2 = 2,145 kg.

V 0 ≈ 1,889 lít. Vì áp suất quá lớn nên khí không thể coi là khí lí tưởng. Do đó kết quả tìm được chỉ là gần đúng.

Đáp án: C
Trạng thái 1: ở điều kiện tiêu chuẩn: p 1 = 1 a t m , t 1 = 0 0 C , ρ = 1,43 k g / m 3
Trạng thái 2: V 2 = 6 l , p 2 = 150 a t m , t 2 = 0 0 C
+ Áp dụng định luật Bôilơ - Mariốt, ta có: p 1 V 1 = p 2 V 2 → V 1 = p 2 V 2 p 1 = 150.6 1 = 900 l = 0,9 m 3
+ Khối lượng của khí là:
m = ρ V = 1,43.0,9 = 1,287 k g

Đáp án: A
+ Ở điều kiện tiêu chuẩn: p 0 = 1 a t m V 0 ρ 0 = 1,43 k g / m 3 t = 0 0 C lại có m = ρ 0 V 0
+ Ở áp suất 150atm: p = 150 a t m V ρ = m V t = 0 0 C
Ta có nhiệt độ của khí không thay đổi, theo định luật Bôi lơ – Ma ri ốt, ta có:
p 0 V 0 = p V ⇔ p 0 m ρ 0 = p m ρ ⇒ ρ = ρ 0 p p 0 = 1,43. 150 1 = 214,5 k g / m 3
Ta có: V = 15 l = 15.10 − 3 m 3
=> Khối lượng m = ρ V = 214,5.15.10 − 3 = 3,22 k g

Do bình không dãn nở vì nhiệt, nên công do khí sinh ra : A' = p ∆ V = 0. Theo nguyên lí I, ta có :
∆ U = Q (1)
Nhiệt lượng do khí nhận được : Q = m c V ( T 2 - T 1 ) (2)
Mặt khác, do quá trình là đẳng tích nên :
![]()
Từ (2) tính được : Q = 15,58. 10 3 J.
Từ (1) suy ra: ∆ U = 15,58. 10 3 J.

Gọi n là số mol khí cacbonic chứa trong bình: n = m/ μ , trong đó M là khối lượng khí cacbonic có trong bình, μ là khối lượng mol của khí cacbonic.
Ta có n = 100 mol
Nếu gọi V 0 là thể tích của lượng khí cacbonic ở điều kiện chuẩn ( p 0 = 1,013. 10 5 Pa; T 0 = 273 K) thì V 0 = n v 0
Áp dụng phương trình trạng thái của khí lí tưởng cho lượng khí cacbonic:
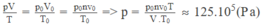

Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn: { V 1 = m p = 3 , 96 1 , 98 m 3 = 2 m 3 p 1 = p 0 = 1 a t T 1 = 0 0 C = 273 K
Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ { V 2 = 0 , 04 m 3 p 2 = 60 a t T 2 = ?
Áp dụng công thức
p 1 V 1 T 1 = p 2 V 2 T 2 ⇒ T 2 = p 2 V 2 T 1 p 1 V 1 = 60.0 , 04.273 1.2 T 2 = 327 , 6 K
Mà T 2 = 273 + t 2 = 327 , 6 K ⇒ t 2 = 54 , 6 0 C

+ Trạng thái 1 là trạng thái khí ở điều kiện tiêu chuẩn:
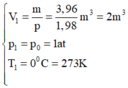
+ Trạng thái 2 là trạng thái khí ở điều kiện có thể nổ:
