Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) Các phương trình phản ứng
2KNO3 2KNO2 + O2↑ (1)
2KClO3 2KCl + 3O2↑ (2)
b) Theo (1) và (2), thấy số mol hai muối tham gia phản ứng như nhau nhưng số mol oxi tạo thành khác nhau và do đó thể tích khí oxi thu được là khác nhau.
Theo (1): nO2 = nKNO3 =
= 0,05 mol; VO2 = 0,05x22,4 = 1,12 lít
Theo (2): nO2 = nKClO3 =
= 0,15 mol; VO2 = 0,15x22,4 = 3,36 lít
c) Để thu được 1,12 lít khí (0,05 mol) O2, thì:
Theo (1): nKNO3 = 2nO2 = = 0,1 mol; mKNO3 = 0,1x101 = 10,1 g
Theo (2): nKClO3 = nO2 =
x0,05 mol; VKClO3 =
x0,05x122,5 = 4,086 g.

\(a/n_{Fe}=\dfrac{2,52}{56}=0,045mol\\ 3Fe+2O_2\xrightarrow[]{t^0}Fe_3O_4\\ n_{O_2}=\dfrac{0,045.2}{3}=0,03mol\\ V_{O_2}=0,03.22,4=0,672l\\ b/2KClO_3\xrightarrow[]{t^0}2KCl+3O_2\\ n_{KClO_3}=\dfrac{0,03.2}{3}=0,02mol\\ m_{KClO_3}=0,02.122,5=2,45g\)

Ở cùng điều kiện nhiệt độ và áp suất, tỉ lệ số mol cũng là tỉ lệ thể tích.
BTNT O, có: \(V_{O\left(trongA\right)}+2V_{O_2}=2V_{CO_2}+V_{H_2O}\Rightarrow V_{O\left(trongA\right)}=0\)
Vậy: A chỉ gồm C và H.
Gọi CTPT của A là CxHy.
\(\Rightarrow\left\{{}\begin{matrix}x=\dfrac{n_{CO_2}}{n_A}=3\\y=\dfrac{2n_{H_2O}}{n_A}=8\end{matrix}\right.\)
Vậy: CTPT cần tìm là C3H8

Gọi nKNO3 = a (mol); nKClO3 = b (mol)
\(\rightarrow\) 101a + 122,5b = 37,35 (1)
2KNO3 --- to --> 2KNO2 + O2
2KClO3 ---to --> 2KCl + 3O2
\(\rightarrow\) 85a + 74,5 b = 27,43 (2)
Giải hệ (1)(2) \(\Rightarrow\)a = 0,2 ; b = 0,14
%nKNO3 = 0,2 / (0,2 + 1,4) = 58,82%
%nKClO3 = 100% - 58,82% = 41,18%
Tương tự tính %m
Bảo toàn khối lượng:
mA = mB + mO2
\(\Leftrightarrow\)37,35 = 27,43 + mO2
\(\Leftrightarrow\) mO2 = 9,92 (g)
\(\Rightarrow\) nO2 = 9,92 / 32 = 0,31 (mol)
VO2 (đktc) = 0,31 . 22,4 = 6,944 (l)
VO2 (thường) = 0,31 . 24 = 7,44 (l)
AgNO3 + KCl -> AgCl + KNO3
0,14 ______ 0,14 ___ 0,14 _0,14 (mol)
Hiện tượng: Xuất hiện kết tủa trắng
mdd AgNO3 = (0,14 . 170)/17% = 140 (g)
\(\rightarrow\) mdd AgNO3 ban đầu = 140 + 10%.140 = 154 (g)
Bảo toàn khối lượng :
m dd sau pứ = mdd AgNO3 + mB - mAgCl
= 154 + 27,43 - 0,14.143,5
= 161,34 (g)
Dd sau pứ gồm: 0,14 mol KNO3, 14(g) AgNO3
C% KNO3 = (0,14 . 101)/161,34 .100%= 8,76%
C% AgNO3 = 14/161,34 . 100% = 8,68%
Mình không gõ được phân số, gõ mà nó không lên. Chả hiểu sao
Bạn thông cảm nha ^^

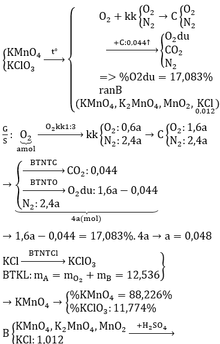
a, Hỗn hợp A gồm CO và CO2.
Gọi: \(\left\{{}\begin{matrix}n_{CO}=x\left(mol\right)\\n_{CO_2}=y\left(mol\right)\end{matrix}\right.\)
Có: dA/O2 = 1,25 ⇒ MA = 1,25.32 = 40 (g/mol)
\(\Rightarrow\dfrac{28x+44y}{x+y}=40\Rightarrow y=3x\) (1)
Ở cùng điền kiện nhiệt độ và áp suất, % số mol cũng là %V.
\(\Rightarrow\left\{{}\begin{matrix}\%V_{CO}=\dfrac{x}{x+y}.100\%=\dfrac{x}{x+3x}.100\%=25\%\\\%V_{CO_2}=75\end{matrix}\right.\)
b, Ta có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
BTNT C, có: nC = nCO + nCO2 = nCaCO3 ⇒ x + y = 0,06 (2)
⇒ m = 0,06.12 = 0,72 (g)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,015\left(mol\right)\\y=0,045\left(mol\right)\end{matrix}\right.\)
BTNT O, có: 2nO2 = nCO + 2nCO2 ⇒ nO2 = 0,0525 (mol)
\(\Rightarrow V_{O_2}=0,0525.22,4=1,176\left(l\right)\)

\(C_2H_4+3O_2\underrightarrow{t^o}2CO_2+2H_2O\)
\(\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(nO_2=3.0,25=0,75\left(mol\right)\)
\(VO_2=0,75.22,4=16,8\left(l\right)\)
\(nCO_2=2.0,25=0,5\left(mol\right)\)
\(VCO_2=0,5.224=11,2\left(l\right)\)

\(n_{CO_2}=\dfrac{3.52}{44}=0.08\left(mol\right)\)
\(n_{H_2O}=\dfrac{1.8}{18}=0.1\left(mol\right)\)
\(m_N=1.72-0.08\cdot12-0.1\cdot2=0.56\left(g\right)\)
\(n_N=\dfrac{0.56}{14}=0.04\left(mol\right)\)
\(M_E=\dfrac{1.29}{\dfrac{0.96}{32}}=43\left(đvc\right)\)
\(n_E=\dfrac{1.72}{43}=0.04\left(mol\right)\)
Số nguyên tử C : \(\dfrac{0.08}{0.04}=2\)
Số nguyên tử H : \(\dfrac{0.2}{0.04}=5\)
Số nguyên tử N : \(\dfrac{0.04}{0.04}=1\)
\(CT:C_2H_5N\)
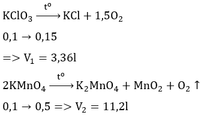
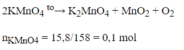
- H2O2
\(n_{H_2O_2}=\dfrac{10}{34}=\dfrac{5}{17}\left(mol\right)\)
PTHH: \(2H_2O_2\underrightarrow{MnO_2}2H_2O+O_2\)
\(\dfrac{5}{17}\)--------------->\(\dfrac{5}{34}\)
=> \(V_{O_2}=\dfrac{5}{34}.22,4=\dfrac{56}{17}\left(l\right)\)
- KMnO4
\(n_{KMnO_4}=\dfrac{10}{158}=\dfrac{5}{79}\left(mol\right)\)
PTHH: \(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
\(\dfrac{5}{79}\)------------------------>\(\dfrac{5}{158}\)
=> \(V_{O_2}=\dfrac{5}{158}.22,4=\dfrac{56}{79}\left(l\right)\)
- KClO3:
\(n_{KClO_3}=\dfrac{10}{122,5}=\dfrac{4}{49}\left(mol\right)\)
PTHH: \(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{4}{49}\)------------->\(\dfrac{6}{49}\)
=> \(V_{O_2}=\dfrac{6}{49}.22,4=\dfrac{96}{35}\left(l\right)\)
- KNO3:
\(n_{KNO_3}=\dfrac{10}{101}\left(mol\right)\)
PTHH: \(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\)
\(\dfrac{10}{101}\)----------->\(\dfrac{5}{101}\)
=> \(V_{O_2}=\dfrac{5}{101}.22,4=\dfrac{112}{101}\left(l\right)\)
Vậy nhiệt phân H2O2 thu được thể tích khí O2 lớn nhất = \(\dfrac{56}{17}\left(l\right)\)
Các PTHH xảy ra:
\(2H_2O_2\underrightarrow{t^o}2H_2O+O_2\) (1)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\) (2)
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\) (3)
\(2KNO_3\underrightarrow{t^o}2KNO_2+O_2\) (4)
Khối lượng mol của \(H_2O_2\) tham gia pứ (1) là: \(M_{H_2O_2}=2M_H+2M_O=2.1+2.16=34\left(g/mol\right)\)
Số mol \(H_2O_2\) tham gia pứ là \(n=\dfrac{m}{M}=\dfrac{10}{34}=\dfrac{5}{17}\left(mol\right)\)
Từ PTHH thứ nhất, ta dễ dàng suy ra được \(n_{O_2}=\dfrac{5}{34}\left(mol\right)\)
Thể tích khí oxi sinh ra trong PTHH (1) ở đktc là \(V_{O_2}=n_{O_2}.22,4=\dfrac{5}{34}.22,4=\dfrac{56}{17}\left(l\right)\)
Khối lượng mol của \(KMnO_4\) tham gia pứ (2) là \(M_{KMnO_4}=M_K+M_{Mn}+4M_O\) \(=39+55+4.16=158\left(g/mol\right)\)
Số mol \(KMnO_4\) tham gia pứ là \(n=\dfrac{m}{M}=\dfrac{10}{158}=\dfrac{5}{79}\left(mol\right)\)
Từ PTHH (2) ta dễ thấy rằng \(n_{O_2}=\dfrac{5}{158}\left(mol\right)\)
Thể tích khí oxi sinh ra trong pứ (2) ở đktc là \(V_{O_2}=n_{O_2}.22,4=\dfrac{56}{79}\left(l\right)\)
Tương tự như trên, bạn sẽ tìm ra được thể tích khí oxi sinh ra trong các pứ (3) và (4). Sau đó cộng tất cả các thể tích khí oxi sinh ra trong cả 4 pứ là có kết quả.