Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

A loại vì NaOH phản ứng với CO 2 và HCl
B loại vì Na 2 CO 3 phản ứng với CO 2 và HCl
C loại vì H 2 SO 4 đặc chỉ tách được nước, không tách được CO 2 và HCl.
D đúng vì NaHCO 3 chỉ phản ứng với HCl sinh ra khí CO 2 và dung dịch H 2 SO 4 để hút nước.
![]()
Đáp án: D

200ml = 0,2l
\(n_{HCl}=2.0,2=0,4\left(mol\right)\)
Pt : \(MnO_2+4HCl_{đặc}\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O|\)
1 4 1 1 2
0,1 0,4
\(n_{MnO2}=\dfrac{0,4.1}{4}=0,1\left(mol\right)\)
⇒ \(m_{MnO2}=0,1.87=8.7\left(g\right)\)
Chúc bạn học tốt

Bình 1 đựng dung dịch NaCl bão hòa để hấp thụ sản phẩm phụ tạo ra sau khi cho MnO2 tác dụng với HCl. Còn lại khí Clo lẫn hơi nước không bị hấp thu, tiếp tục dẫn qua bình 2 chứa H2SO4 đặc nóng, nước bị hấp thụ. Thu lấy khí thoát ra ta thu được khí Clo tinh khiết.
PTHH: \(MnO_2+4HCl_{\left(đăc\right)}-t^o->MnCl_2+Cl_2+2H_2O\)

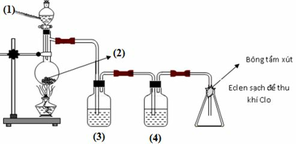
Để tránh Cl2 thoát ra ngoài không khí, người ta tẩm NaOH vào (6). Vì Cl2 có phản ứng với NaOH do đó bị giữ lại
PTPƯ
![]()
Đáp án: B


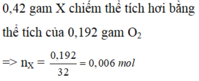
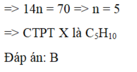
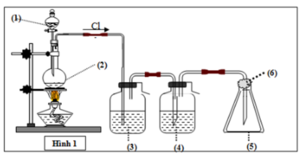
H2SO4 đặc