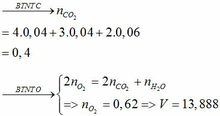Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

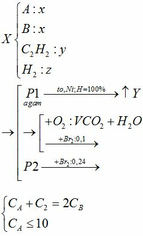
a, \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
\(C_2H_2+2Br_2\rightarrow C_2H_2Br_4\)
Ta có: \(n_{C_2H_4}+n_{C_2H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\left(1\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}+2n_{C_2H_2}=\dfrac{48}{160}=0,3\left(mol\right)\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=0,2\left(mol\right)\\y=0,05\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%V_{C_2H_4}=\dfrac{0,2.22,4}{5,6}.100\%=80\%\\\%V_{C_2H_2}=20\%\end{matrix}\right.\)
b, \(V_{ddBr_2}=\dfrac{0,3}{0,25}=1,2\left(M\right)\)



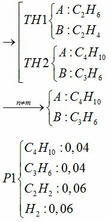
a) Gọi số mol của FeCO3: x (mol) ;
số mol của FeS2: y (mol)
4FeCO3 + O2 → Fe2O3 + 4CO2↑
x → 0,25x → x (mol)
4FeS2 +11O2 → 2Fe2O3 + 8SO2↑
y → 2,75y → 2y (mol)
∑ nO2 = 0,25x + 2,75y (mol)
Cùng điều kiện về nhiệt độ và áp suất nên tỉ lệ về thể tích = tỉ lệ về số mol
=> nN2 = 4nO2 = 4(0,25x + 2,75y)
=> nN2 = x + 11y (mol)
Vậy hỗn hợp Y gồm:

Khối lượng Fe có trong Z là:

Vì H = 80% => nFe2O3 (trong X) = 0,12. 100% : 80% = 0,15 (mol)
nFe2O3 dư (trong Z) = 0,15 – 0,12 = 0,03 (mol)
Khối lượng tạp chất trong Z = 27,96 – mFe – mFe2O3 dư = 27,96 – 0,24.56 – 0,03.160 = 9,72 (g)
Bảo toàn nguyên tố Fe => nFeCO3 + nFeS2 = 2nFe2O3(trong X)
=> x + y = 0,3 (2)
Từ (1) và (2) => x = 0,18 và y = 0,12 (mol)
Áp dụng công thức PV = nRT ( với n = nCO2 + nSO2 + nN2 = 0,18 + 2. 0,12 + 0,18 +11.0,12 = 1,92)
=> P.10 = 1,92.0,082. (136,5 +273)
=> P = 6,447 ( atm) ≈ 6,5 (atm)
Ta có: mA = mFeCO3 + mFeS2 + mtạp chất = 0,18.116 + 0,12.120 + 9,72 = 45 (g)
![]()
b) hỗn hợp Y gồm:

Cho hỗn hợp Y qua O2 ( xúc tác V2O5 ) có phản ứng sau:

Khối lượng dd sau: mdd sau = mSO3 + mH2O = 0,24. 80 + 592,8 = 612 (g)


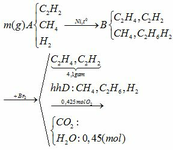
C2H2 + H2 C2H4
C2H2 + H2 C2H6
Khi cho hỗn hợp B qua dd nước Br2 chỉ có C2H4 và C2H2 phản ứng C2H2 +2Br2 → C2H2Br4
C2H4 + Br2 → C2H4Br2
=> khối lượng bình Br2 tăng chính bằng khối lượng của C2H2 và C2H4
mC2H2 + mC2H4 = 4,1 (g)
Hỗn hợp khí D đi ra là CH4, C2H6 và H2
CH4 + 2O2 → t ∘ CO2 + 2H2O
C2H6 + O2 → t ∘ 2CO2 + 3H2O
2H2 + O2 → t ∘ 2H2O
Bảo toàn nguyên tố O cho quá trình đốt cháy hh D ta có:
2nCO2 = 2nO2 – nH2O => nCO2 = ( 0,425. 2– 0,45)/2 = 0,2 (mol)
Bảo toàn khối lượng : mhh D = mCO2 + mH2O – mO2 = 0,2.44 + 0,45.18 – 0,425.32 = 3,3 (g)
Bảo toàn khối lương: mA = (mC2H2 + mC2H4) + mhh D = 4,1 + 3,3 = 7,4 (g)

a. Phương trình phản ứng giữa axetilen và dung dịch Br2:
C2H2 + Br2 → C2H2Br2
b. Theo định luật Avogadro, số mol khí thể tích bằng nhau ở cùng điều kiện nhiệt độ và áp suất. Vì vậy, số mol của hỗn hợp Y bằng số mol của khí thoát ra sau phản ứng.
Theo đó, ta có thể tính số mol mỗi khí trong hỗn hợp:
Số mol khí thoát ra: n = V/ Vm = 2,24/ 22,4 = 0,1 molSố mol axetilen ban đầu: n(C2H2) = n = 0,1 molSố mol metan ban đầu: n(CH4) = (V(Y) - V(C2H2)) / Vm = (3,36 - 2,24) / 22,4 = 0,05 molc. Để tính % về khối lượng từng khí trong hỗn hợp, ta cần biết khối lượng riêng của từng khí. Ở đktc, khối lượng riêng của axetilen là 1,096 g/L và khối lượng riêng của metan là 0,717 g/L.
Khối lượng axetilen trong hỗn hợp: m(C2H2) = n(C2H2) x M(C2H2) = 0,1 x 26 = 2,6 gKhối lượng metan trong hỗn hợp: m(CH4) = n(CH4) x M(CH4) = 0,05 x 16 = 0,8 gTổng khối lượng của hỗn hợp Y: m(Y) = V(Y) x ρ(Y) = 3,36 x 1,25 = 4,2 gVậy, % về khối lượng của axetilen trong hỗn hợp là:
% m(C2H2) = (m(C2H2) / m(Y)) x 100% = (2,6 / 4,2) x 100% = 61,9%
% về khối lượng của metan trong hỗn hợp là:
% m(CH4) = (m(CH4) / m(Y)) x 100% = (0,8 / 4,2) x 100% = 19,0%