Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C

- Giả sử Mg, Fe đều phản ứng hết với muối kim loại => Z chứa toàn bộ số mol Mg2+ ; Fex+
=> T chứa Mg(OH)2 và Fe(OH)x => Chất rắn cuối cùng là MgO và Fe2O3 chắc chắn phải có khối lượng lớn hơn lượng kim loại ban đầu trong X => Không thỏa mãn đề bài (7,2 < 7,36)
=> Các muối nitrat phản ứng hết, kim loại dư và đó là Fe (vì Mg phản ứng trước)
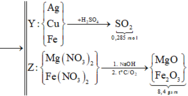
=> kết tủa Y gồm Cu, Ag, Fe.
- Gọi nMg = a ; nFe(pứ) = b ; nFe dư = c => mX = 24a + 56b + 56c = 7,36 (1)
- Bảo toàn e cho phản ứng trao đổi muối: 2nMg + 2nFe pứ = nAg + 2nCu = 2a + 2b
- Khi Y + H2SO4 đặc nóng (Fe → Fe3+)
Bảo toàn electron: 2nCu + nAg + 3nFe dư = 2nSO2 = 2.5,04/22,4 = 0,45 mol
=> 2a + 2b + 3c = 0,45 (2)
- Như đã phân tích ở trên. chất rắn cuối cùng gồm MgO và Fe2O3.
Bảo toàn nguyên tố: nMg = nMgO = a ; nFe2O3 = ½ nFe pứ = 0,5b
=> mrắn = mMgO + mFe2O3 = 40a + 160.0,5b = 40a + 80b = 7,2 (3)
Từ (1,2,3) => a = 0,12 ; b = 0,03 ; c = 0,05 mol
=> mFe(X) = 56.(0,03 + 0,05) = 4,48g
=> %mFe(X) = 4,48: 7,36 = 60,87%

Đáp án : A
Ta thấy mX > mRắn (gồm oxit) => Y gồm cả Fe , Cu , Ag
Gọi số mol Mg là x ; số mol Fe phản ứng đầu là y và dư sau đó là z mol
=> mX = 24x + 56y + 56z = 7,36g (1)
Bảo toàn e : 2nMg + 2nFe pứ + 3nFe dư = nAg + 2nCu + 3nFe dư = 2nSO2
=> 2x + 2y + 3z = 0,45 mol
,mrắn = mMgO + mFe2O3 = 40x + 80y = 7,2g
=> x = 0,12 mol ; y = 0,03 mol ; z = 0,05 mol
=> %mFe(X) = 60,87%

Đáp án : C
nSO2 = 0,225 mol
Chất rắn sau khi nung chỉ nặng 7,2 gam nên toàn bộ Mg và Fe không thể chuyển hết về oxit được (Lúc đó mrắn > 7,36), tức là trong Y phải có Fe dư —> AgNO3 và Cu(NO3)2 đã hết
Đặt a, b, c là số mol Mg, Fe phản ứng và Fe dư —> 24a + 56(b + c) = 7,36
Chất rắn Y gồm Ag, Cu và Fe dư, phần Ag, Cu do Mg (a) và Fe (b) đẩy ra nên 2a + 2b = nAg + 2nCu
Trong khi đó: nAg + 2nCu + 3nFe dư = 2nSO2 —> 2a + 2b + 3c = 0,225.2
Chất rắn cuối bài gồm MgO (a) và Fe2O3 (b/2) —> 40a + 160b/2 = 7,2
Giải hệ: a = 0,12 mol b = 0,03 mol c = 0,05 mol —> nFe = 0,08 mol —> %mFe = 60,87%

Định hướng tư duy giải
→ n NH 4 + = 0 , 235 . 2 - 0 , 14 . 3 8 = 0 , 00625
=> 110,23 = 0,73943m + 96.(0,235+0,26057m/16) => m = 38,07
=> mY = 28,15 + 62.(0,00625.8 + 0,14.3 + 0,62.2) + 80.0,00625 = 134,67

Chọn A.
→ B T : e c h o 1 v à 2 n N H 4 N O 3 = 2 n S O 2 - 3 n N O - 8 n N 2 O 8 = 0 , 0375 m o l
Gọi T là hỗn hợp muối chứa Fe(NO3)2 và Mg(NO3)2 suy ra: m T = m Y - m N H 4 N O 3 = 126 , 4 g a m
Áp dụng phương pháp tăng giảm khối lượng + bảo toàn điện tích cho hỗn hợp T và Z ta có:

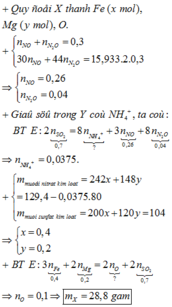



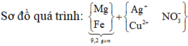

Chọn B
nH trong X = nOH ⟹ nOH = mH = 0,01847m