Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

- Khí thoát ra gồm CO và CO2.
Gọi: \(\left\{{}\begin{matrix}n_{CO}=a\left(mol\right)\\n_{CO_2}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow a+b=\dfrac{2,0608}{22,4}=0,092\left(mol\right)\left(1\right)\)
TỈ khối của C so với O2 là 1,125.
\(\Rightarrow\dfrac{28a+44b}{a+b}=1,125.32\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,046\left(mol\right)\\b=0,046\left(mol\right)\end{matrix}\right.\)
BTNT C, có: nCO (pư) = nCO2 = 0,046 (mol)
Gọi: \(\left\{{}\begin{matrix}n_{FeO}=x\left(mol\right)\\n_{Fe_2O_3}=y\left(mol\right)\end{matrix}\right.\) ⇒ x + y = 0,04 (3)
Theo ĐLBT KL, có: mA + mCO = mB + mCO2
⇒ mA = 4,784 + 0,046.44 - 0,046.28 = 5,52 (g)
⇒ 72x + 160y = 5,52 (4)
Từ (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}x=0,01\left(mol\right)\\y=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{FeO}=\dfrac{0,01.72}{5,52}.100\%\approx13,04\%\\\%m_{Fe_2O_3}\approx86,96\%\end{matrix}\right.\)

A, Gọi X,y lần lượt là số mol của Mg và Al
Pthh:
Mg + H2SO4---> MgSO4 + H2
X. X. X. X
2Al + 3H2SO4---> Al2(SO4)3+3H2
Y. 1.5y. Y. 1.5y
Ta có pt:
24x + 27y= 1.95
X+1.5y=2.24/22.4=0.1
=> X=0.025, Y=0.05
%Mg= 0.025×24×100)/1.95=30.8%
%Al= 100%-30.8%=69.2%
mH2SO4= 0.025+1.5×0.05=0.1g
mH2= (0.025+0.05)×2=0.15g
C, Mdd H2SO4 = 0.1/6.5×100=1.54g
MddY= 1.54+1.95-0.15=3.34g
%MgSO4 vs %Al2(SO4)3 b tự tính nha

P1: Gọi số mol CO, H2 trong phần 1 là a, b mol
PTHH: CuO + CO --to--> Cu + CO2
CuO + H2 --to--> Cu + H2O
\(n_{Cu}=\dfrac{4,48}{64}=0,07\left(mol\right)\)
=> a + b = 0,07 (1)
P2: Gọi số mol CO, H2 trong phần 2 là ak, bk mol
=> 28ak + 2bk - 28a - 2b = 1,32 (2)
\(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
PTHH: CO + O2 --to--> CO2
CO2 + Ca(OH)2 --> CaCO3 + H2O
=> ak = 0,06 (mol) (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}a=0,02\\b=0,05\\k=3\end{matrix}\right.\)
=> m = (0,02.28 + 0,05.2) + (0,06.28+0,15.2) = 2,64(g)
\(\left\{{}\begin{matrix}\%CO=\dfrac{0,02}{0,07}.100\%=28,57\%\\\%H_2=\dfrac{0,05}{0,07}.100\%=71,43\%\end{matrix}\right.\)

n NO = 2,24/22,4 = 0,1 mol
Gọi chất rắn sau khi nung trong ống sứ với CO là hỗn hợp B nặng 19,2 gam.
Vì khi B phản ứng với HNO3 sinh ra 0,1 mol NO và muối Fe(+3) nên B đã nhường cho HNO3 0,1 x 3 = 0,3 mol e.
Nếu B nhường 0,3 mol e này cho oxi nguyên tử thì toàn bộ nguyên tố Fe trong B sẽ trở thành Fe(+3) trong oxit Fe2O3.
Để nhận 0,3 mol e này, cần 0,15 mol oxi nguyên tử phản ứng với B nặng 0,15 x 16 = 2,4 gam. Vì thế, sau khi phản ứng của B với oxi nguyên tử, ta thu được Fe2O3 với khối lượng là:
19,2 + 2,4 = 21,6 gam.
--> n Fe2O3 = 21,6/160 = 0,135 mol --> n Fe = 0,135 x 2 = 0,27 mol
Gọi số mol mỗi oxit trong A là a mol.
Từ n Fe = 0,27 mol, ta có:
2a + 3a + a = 0,27
--> a = 0,045 mol
--> m1 = 0,045 x 160 + 0,045 x 232 + 0,045 x 72 = 20,88 gam.
Từ n Fe = 0,27 mol, ta có:
--> khối lượng nguyên tố Fe trong B = 0,27 x 56 = 15,12 gam
--> m O trong B = 19,2 - 15,12 = 4,08 gam
--> n O trong B = 4,08/16 = 0,255 mol = n CO2 thu được khi dùng CO khử A ban đầu = n BaCO3 kết tủa
--> m2 = m BaCO3 = 0,255 x 197 = 50,235 gam.
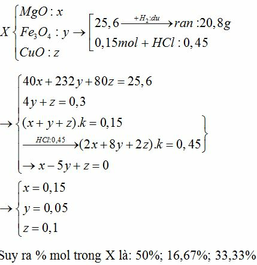
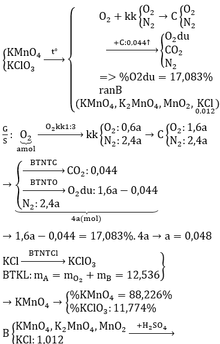
Ta có: $n_{H_2}=0,05(mol);n_{CO}=0,1(mol);n_{CO_2}=0,15(mol)$
Bảo toàn nguyên tố H ta có: \(n_{H_2}=n_{H_2O}=0,02\left(mol\right)\)
Ta có: \(n_O=n_{CuO\text{/}tpgu}=\frac{8-6,88}{16}=0,07\left(mol\right)\)
$CuO+H_2\rightarrow Cu+H_2O$
$CuO+CO\rightarrow Cu+CO_2$
Suy ra $n_{CO}=0,05(mol)$
Do đó trong C còn 0,03 mol $H_2$; 0,05 mol $CO$ và 0,2 mol $CO_2$
Còn trong D có 0,07 mol Cu; 0,03 mol CuO
Từ đó tính được yêu cầu đề