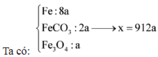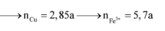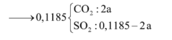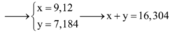Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Điện phân trong 3378 giây tương đương với số e trao đổi là 0,07 mol
Do trao đổi 0,07 mol e chỉ thu được thêm 0,025 mol Cu, chứng tỏ Cu hết
Lúc này ở catot thu thêm 0,025 mol Cu và 0,01 mol H2
Vậy lúc này ở anot thu được thêm 0,025 mol khí
Do số mol khí trao đổi 0,07 nên chứng tỏ đã có tạo ra O2.
Vậy ở anot thu được Cl2 và O2 với số mol lần lượt là 0,015 và 0,01 mol.
Mặt khác do lúc t giây chỉ thu được Cu ở catot và Cl2 ở anot nên a=b.
Vậy t giây thì n e = 2 a nên 2t giây thì n e = 4 a
Lúc 2t giây ở anot thu được a+0,025 mol Cu và a-0,025 mol H2.
Ở catot thu được a+0,015 mol Cl2 và O2 0,5a-0,0075 mol
Tổng số mol khí thu được là:
a - 0,025 +a + 0,015 + 0,5a - 0,0075 = 2,0625a
Giải được a= 0,04
Vậy số mol CuSO4 là 0,065 mol và KCl là 0,11 mol
=> m = 18,595 gam

Đáp án A
Tại catot có thể lần lượt xảy ra các quá trình:
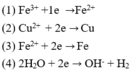
Tại anot có thể lần lượt xảy ra các quá trình:
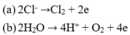
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi thu được hỗn hợp 2 oxit. Trong A có 2 loại ion kim loại
Mặt khác, khi điện phân dung dịch A cho đến khi hết ion Cl - thì catot tăng 6,4 gam
⇒ Quá trình (2) đã xảy ra một phần, Cu 2 + vẫn còn trong dung dịch sau điện phân.
Gọi số mol Fe 3 + , Cu 2 + , Cl - , SO 4 2 - trong 100ml dung dịch A lần lượt là a,b,c,d.
Khi điện phân hết 
Theo bảo toàn e: số e do Fe3+ và Cu2+ nhận bằng số mol Cl- nhường. a + 0,1.2 = c (1)
Khối lượng dung dịch giảm gồm Cu2+ và Cl- đã phản ứng và bị tách ra khỏi dung dịch
6,4 + 35,5c = 17,05 (2)
Sau khi điện phân A, cho dung dịch này phản ứng với NaOH thu được kết tủa B, nung B đến khối lượng không đổi được 16 gam 2 oxit
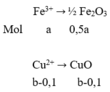
Suy ra: 160,0,5a + 80(b – 0,1) = 16 (3)
Theo định luật bảo toàn điện tích, đối với dung dịch A ta có:
3a + 2b = c + 2d (4)
Giải hệ phương trình ta được:
a = 0,1; b = 0,2; c= 0,3; d = 0,2
Khối lượng muối trong 100ml dung dịch A là 48,25 gam

Chia, tách nhỏ từng bài tập, quá trình ra để giải:
chỉ có Al + NaOH → NaAlO2 + 3/2H2
nNaOH = nH2 = 0,12 mol
⇒ chứng tử sau phản ứng NaOH còn dư 0,04 mol và ∑nAl trong A = 0,08 mol.
Khí B như ta biết gồm CO2 (sinh ra do FeCO3) và H2 (do Fe)
10 gam kết tủa là 0,1 mol CaCO3
⇒ có 0,1 mol CO2 ⇒ nFeCO3 = 0,1 mol.
Rắn R ra chắc chắn có Cu và có thể là còn dư kim loại Fe. Vậy phần trong dung dịch?
À, gồm: 0,08 mol AlCl3; 0,12 mol NaCl + ??? mol FeCl2. Mà ∑nHCl = nHCl = 0,74 mol
⇒ bảo toàn Cl có ngay nFeCl2 = 0,19 mol; sinh ra do 0,1 mol FeCO3 ⇒ còn 0,09 nữa do Fe.
Vậy mR = mCu, Fe lọc ra = 20 – mAl – mFeCO3 – mFe phản ứng = 1,2 gam.
R gồm Cu, Fe là các kim loại hoạt động TB yếu nên + HNO3 sinh NO hoặc NO2.
ở đây dùng HNO3 đặc nên khí duy nhất sinh ra là NO2 |
nNO2 = 0,05 mol
⇒ bảo toàn electron có 3nFe + 2nCu = nNO2 = 0,05 mol mà mFe + Cu = 1,2 gam
⇒ giải ra nFe = nCu = 0,01 mol. Đọc tiếp quá trình cuối
⇒ m gam sản phẩm gồm 0,01 mol CuO và 0,05 mol Fe2O3 ⇒ m = 1,6 gam
Đáp án B

Đáp án A
nFe = 2. 58/400 = 0,29 mol
nFeSO4 = x , nFe2(SO4)3 = y
⇒mdd = 152 x + 400y = 51,76
nFe = nFeSO4 +2.nFe2(SO4)3 = x+ 2y = 0,29
⇒x= 0,13 mol , y= 0,08 mol
BT S: nH2SO4 = nFeSO4 + 3Fe2(SO4)3 = 0,13 + 3.0,08 = 0,37
⇒b = 0,37.98/9,8% = 370g

Đáp án A
nFe2(SO4)3 = 58/400 = 0,145 mol
nFeSO4 = a ; nFe2(SO4)3 =b
⇒152a + 400b = 51,76
BT Fe: a + 2b = 0,145 . 2 = 0,29 ⇒ a= 0,13 mol; b= 0,08 mol
BT S: nH2SO4 = n FeSO4 + 3nFe2( SO4)3 = 0,13 + 3. 0,08 = 0,37
⇒b= 0,37 .98 /0,098 =370g