Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(m_X=56x+64y+108x=29.2\left(g\right)\)
\(\Rightarrow164x+64y=29.2\left(1\right)\)
\(n_{H_2SO_4}=\dfrac{80\cdot98\%}{98}=0.8\left(mol\right)\)
Bảo toàn e :
\(3n_{Fe}+2n_{Cu}+n_{Ag}=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=2x+y\left(mol\right)\)
Bảo toàn S :
\(n_{H_2SO_4}=3n_{Fe_2\left(SO_4\right)_3}+n_{CuSO_4}+n_{Ag_2SO_4}+n_{SO_2}\)
\(\Rightarrow x+y+x+2x+y=0.8\)
\(\Rightarrow4x+2y=0.8\left(2\right)\)
\(\left(1\right),\left(2\right):x=0.1,y=0.2\)

X + O2 → Y
Bảo toàn khối lượng có mO2 = 0,48 g → nO2 = 0,015 mol
Quy đổi Y thành kim loại và oxi
Ta có 4H+ + 4e + NO3- → 2H2O + NO
2H+ + O2- → H2O
→ nH+ = 4nNO + 2nO =4.0,03 + 2.0,03= 0,18 mol
Bảo toàn nguyên tố H thì nHNO3 = 0,18 mol
bài2
Ta có: nCO= 0,8 mol; nSO2= 0,9 mol
MxOy + yCO → xM + yCO2 (1)
Ta thấy đáp án M là Fe hoặc Cr nên M có số oxi hóa cao nhất là +3
2M + 6H2SO4 → M2(SO4)3+ 3SO2+ 6H2O (2)
Theo PT (2): nM= 2/3.nSO2= 0,6 mol
Theo PT (1):
x/y=nM/nCO=0,6/0,8=3/4 => Oxit là Fe3O4

a. Gọi \(a,b\) lần lượt là số mol của \(Mg,Fe\) có trong hỗn hợp ban đầu.
\(\Rightarrow m_{hh}=24a+56b=22,8\left(g\right)\left(1\right)\)
\(n_{SO_2}=\frac{15,68}{22,4}=0,7\left(mol\right)\)
Các quá trình oxi hóa và khử:
\(Mg\rightarrow Mg^{2+}+2e\)
\(a----->2a\)
\(Fe\rightarrow Fe^{3+}+3e\)
\(b----->3b\)
\(S^{+6}+2e\rightarrow S^{+4}\)
\(0,7-1,4-0,7\)
Áp dung định luật bào toàn electron, ta có: \(2a+3b=1,4\left(mol\right)\left(2\right)\)
Từ \(\left(1\right),\left(2\right)\) ta được hệ: \(\left\{{}\begin{matrix}24a+56b=22,8\\2a+3b=1,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,25\left(mol\right)\\b=0,3\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,25.24=6\left(g\right)\Rightarrow\%m_{Mg}=\frac{6}{22,8}=.100\%=26,32\%\)
\(\Rightarrow\%m_{Fe}=100\%-26,32\%=73,68\%\)
b. Từ câu a, ta được: \(n_{H_2SO_4\left(p.ư\right)}=n_{S^{+6}}=0,7\left(mol\right)\)
\(n_{NaOH}=0,4.3=1,2\left(mol\right)\)
PTHH: \(H_2SO_4+2NaOH\rightarrow Na_2SO_4+2H_2O\)
\(\Rightarrow n_{H_2SO_4\left(dư\right)}=\frac{1,2}{2}=0,6\left(mol\right)\)
\(\Rightarrow n_{H_2SO_4\left(bđ\right)}=0,7+0,6=1,3\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4\left(bđ\right)}=1,3.98=127,4\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4\left(bđ\right)}=\frac{127,4.100}{98}=130\left(g\right)\)
c. Gọi \(x\) là số mol của \(Cu_2S\) \(\rightarrow n_{FeS_2}=2x\left(mol\right)\)
PTHH:
\(2FeS_2+14H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+14H_2O+15SO_2\)
\(2x---->14x-->x\)
\(Cu_2S+6H_2SO_4\rightarrow2CuSO_4+5SO_2+6H_2O\)
\(x---->6x-->2x\)
\(\Rightarrow14x+6x=1,3\left(mol\right)\Leftrightarrow x=0,065\left(mol\right)\)
\(\Rightarrow n_{Fe_2\left(SO_4\right)_3}=x=0,065\left(mol\right);n_{CuSO_4}=2x=0,13\left(mol\right)\)
\(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,065.400=26\left(g\right);m_{CuSO_4}=0,13.160=20,8\left(g\right)\)
\(\Rightarrow m\)muối\(=26+20,8=46,8\left(g\right)\)

Coi \(n_{Cu} = n_{FeO} = 1(mol)\\ n_{Fe} = x(mol)\)
Bảo toàn electron cho quá trình 1:
\(2n_{Fe} + 2n_{Cu} = 3n_{NO}\)
⇒ 2x + 2 = 3a(1)
Y gồm \(Cu(NO_3)_2,Fe(NO_3)_2\)
Bảo toàn electron cho quá trình 2 :
\(n_{Fe(NO_3)_2} = x + 1 = 3n_{NO}\)
⇒ x + 1 = 3b(2)
Lấy (1) : (2), ta có \(\dfrac{2x + 2}{x + 1} =\dfrac{3a}{3b} \Rightarrow \dfrac{a}{b} = 2\)
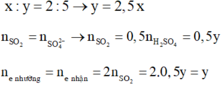

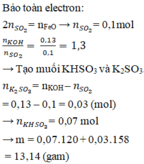

Chọn A
C u F e S 2 ⏞ 0 → C u + 2 + F e + 3 + 2 S + 6 + 17 e
x → 17x (mol)
N + 5 + 1e → N + 4
y ← y (mol)
Bảo toàn e → 17x = y