Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Giả sử: \(\left\{{}\begin{matrix}n_{SO_2}=a\left(mol\right)\\n_{H_2S}=b\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow a+b=\dfrac{2,24}{22,4}=0,1\left(1\right)\)
Vì: dX/H2 = 24,5 \(\Rightarrow64a+34b=4,9\left(2\right)\)
Từ (1) và (2) ⇒ a = b = 0,05 (mol)
Giả sử: \(\left\{{}\begin{matrix}n_{Zn}=x\left(mol\right)\\n_{Cu}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow65x+64y=12,9\left(3\right)\)
Các quá trình:
\(Zn^0\rightarrow Zn^{+2}+2e\)
x____________ 2x (mol)
\(Cu^0\rightarrow Cu^{+2}+2e\)
y____________ 2y (mol)
\(S^{+6}+2e\rightarrow S^{+4}\)
_____0,1__0,05 (mol)
\(S^{+6}+8e\rightarrow S^{-2}\)
_____0,4__0,05 (mol)
Theo ĐLBT mol e, có: 2x + 2y = 0,1 + 0,4 ⇒ x + y = 0,25 (4)
Từ (3) và (4) \(\Rightarrow\left\{{}\begin{matrix}x=\\y=\end{matrix}\right.\)
Tới đây ra số âm, bạn xem lại đề nhé!

a)
$Cu + 2H_2SO_4 \to CuSO_4 + SO_2 + H_2O$
$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O$
b) n Cu =a (mol) ; n Fe = b(mol)
=> 64a + 56b = 12(1)
n SO2 = a + 1,5b = 5,6/22,4 = 0,25(2)
(1)(2) suy ra a = b = 0,1
%m Cu = 0,1.64/12 .100% = 53,33%
%m Fe = 100% -53,33% = 46,67%
c)
n CuSO4 = a = 0,1(mol)
n Fe2(SO4)3 = 0,5a = 0,05(mol)
m muối = 0,1.160 + 0,05.400 = 36(gam)
d) n H2SO4 = 2n SO2 = 0,5(mol)
V H2SO4 = 0,5/2 = 0,25(lít)

nSO2 = \(\dfrac{2,8}{22,4}\)=0,125 mol
S+6 + 2e → S+4
0,25<-----0,125
=> Số mol e do 3,35 gam hỗn hợp kim loại nhường là 0,25 mol.
Xét phản ứng với Clo
Kim loại + Cl2 → Muối clorua
Có 3,35 gam kim loại phản ứng nên số mol e kim loại nhường cũng là 0,25 mol
Cl20 + 2e → 2Cl-1
0,25 --> 0,25
=> nCl-1 trong muối clorua = 0,25 mol
<=> mCl-1 = 0,25.35,5 = 8,875 gam.
mMuối = mKim loại + mCl-1 = 3,35 + 8,875 = 12,225 gam.

\(n_{SO_2}=\dfrac{V_{SO_2}}{22,4}=\dfrac{2,24}{22,4}=0,1mol\)
Gọi \(\left\{{}\begin{matrix}n_{Mg}=x\\n_{Cu}=y\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}m_{Mg}=24x\\m_{Cu}=64y\end{matrix}\right.\)
\(Mg+2H_2SO_4\rightarrow MgSO_4+SO_2+2H_2O\)
x 2x x ( mol )
\(Cu+2H_2SO_4\rightarrow CuSO_4+SO_2+2H_2O\)
y 2x y ( mol )
Ta có:
\(\left\{{}\begin{matrix}24x+64y=4,4\\x+y=0,1\end{matrix}\right.\) \(\Leftrightarrow\left\{{}\begin{matrix}x=0,05\\y=0,05\end{matrix}\right.\)
\(\Rightarrow m_{Mg}=0,05.24=1,2g\)
\(\Rightarrow m_{Cu}=0,05.64=3,2\)
\(m_{H_2SO_4}=n_{H_2SO_4}.M_{H_2SO_4}=\left(2.0,05+2.0,05\right).98=0,2.98=19,6g\)
À thêm đk H2SO4 đặc nóng nhá chứ H2SO4 loãng thì PTHH là:
Mg + H2SO4 -> MgSO4 + H2
Cu không tác dụng với H2SO4 loãng



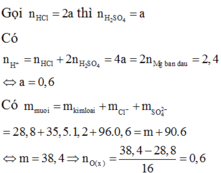
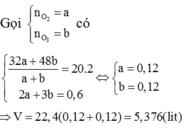
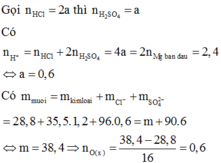
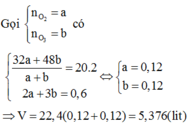
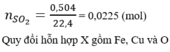
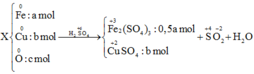
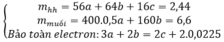
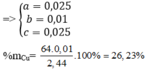
Đặt số mol của SO2 và H2S lần lượt là a,b
Ta có Tỉ khối hơi so với H2 là 27
--> \(\dfrac{\overline{M_{hh}}}{M_{H_2}}=27->\overline{M}=54\)
Có \(\dfrac{m_{hh}}{n_{hh}}=\overline{M_{hh}}\)
--> \(\dfrac{64a+34b}{a+b}=54->10a-20b=0\left(1\right)\)
Lại có \(a+b=0,15\left(2\right)\)
Giải \(\left(1\right),\left(2\right)\) ta có \(\left\{{}\begin{matrix}a=0,1\\b=0,05\end{matrix}\right.\)
Gọi số mol của Cu,Mg lần lượt là x,y (mol)
Ta có \(\dfrac{n_{Cu}}{n_{Mg}}=\dfrac{1}{2}\)--> \(\dfrac{x}{y}=\dfrac{1}{2}->2x=y\left(3\right)\)
Áp dụng phương pháp bảo toàn e
Ta có
\(\overset{0}{Cu}\)->\(\overset{+2}{Cu}\)+2e
x --> x 2x (mol)
\(\overset{0}{Mg}\)->\(\overset{+2}{Mg}\)+2e
y --> y 2y (mol)
\(\overset{+6}{S}\)+2e->\(\overset{+4}{S}\)(SO2)
0,2 <-0,1 (mol)
\(\overset{+6}{S}\)+8e->\(\overset{-2}{S}\)(H2S)
0,4 <-0,05 (mol)
--> ta có phương trình \(2x+2y=0,2+0,4\left(4\right)\)
Giải \(\left(3\right),\left(4\right)->\left\{{}\begin{matrix}x=0,1\\y=0,2\end{matrix}\right.\)
\(m_{Cu}=0,1\cdot64=6,4\left(g\right)\)
\(m_{Mg}=0,2\cdot24=4,8\left(g\right)\)
--> \(m_{kl}=6,4+4,8=11,2\left(g\right)\)
\(m_{CuSO_4}=0,1\cdot160=16\left(g\right)\)
\(m_{MgSO_4}=0,2\cdot120=24\left(g\right)\)
\(m_{muối}=16+24=40\left(g\right)\)