K
Khách
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.
Các câu hỏi dưới đây có thể giống với câu hỏi trên

27 tháng 12 2019
Chọn C.
Giả sử số mol KCl trong X là 1 mol, khi đó quá trình điện phân xảy ra như sau:Theo đề bài ta có:
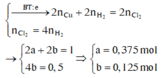
Vậy hỗn hợp X gồm CuSO4 (0,375 mol) và KCl (1 mol)
![]()
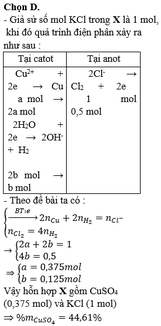




Chọn B
Cu2+:x
Cl-: y
Ở catot thoát ra khí => H2O bị đp
Catot:
Cu2+ +2e → Cu
x 2x
H2O +1e → 0,5H2 + OH-
y-2x 0,5y-x
Anot:
Cl- - 1e → 0,5Cl2
y y 0,5y
=> 0,5y = 4(y-2x) => x/y=3/8
=>%mCuSO4 = 160.3/(160.3+74,5.8) = 44,61%