Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Định hướng tư duy giải
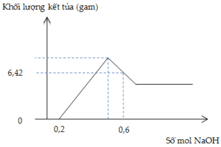
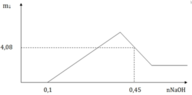
Từ đồ thị ta thấy số mol HNO3 dư là 0,2 → H + n N O = 0 , 12 → n e = 0 , 36
Tại vị trí 0,6 mol, điền số
→ N a + : 0 , 6 N O 3 - : 0 , 56 → A l O 2 - : 0 , 04 → 6 , 42 M g ( O H ) 2 : a A l ( O H ) 3 : b - 0 , 04 → a = 0 , 03 b = 0 , 1 → % A l = 78 , 95 %

Mg + HCl - MgCl2 + H2
Al + HCl - AlCl3 + H2
còn Cu đứng sau H nên không phản ứng với HCl.
nCuO = \(\dfrac{16}{80}=0,2\) mol
Pt: 2Cu + O2 --to--> 2CuO
0,2 mol<--------------0,2 mol
.....Mg + 2HCl --> MgCl2 + H2
0,2 mol<-----------0,2 mol
.....2Al + 6HCl --> 2AlCl3 + 3H2
....MgCl2 + 2NaOH --> Mg(OH)2 + 2NaCl
...0,2 mol<---------------0,2 mol
....AlCl3 + 3NaOH --> Al(OH)3 + 3NaCl
....Al(OH)3 + NaOH --> NaAlO2 + 2H2O
..........................................(tan)
...Mg(OH)2 --to--> MgO + H2O
0,2 mol<------------ 0,2 mol
nMgO = \(\dfrac{8}{40}=0,2\) mol
mCu = 0,2 . 64 = 12,8 (g)
mMg = 0,2 . 24 = 4,8 (g)
mAl = mhh - mCu - mMg = 20 - 12,8 - 4,8 = 2,4 (g)
% mCu = \(\dfrac{12,8}{20}.100\%=64\%\)
% mMg = \(\dfrac{4,8}{20}.100\%=24\%\)
% mAl = \(\dfrac{2,4}{20}.100\%=12\%\)

Chọn đáp án C
Định hướng tư duy giải
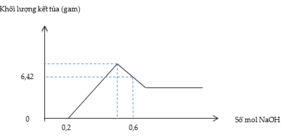
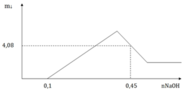
Từ đồ thị ta thấy số mol HNO3 dư là 0,1 → H + n N O = 0 , 1 → n e = 0 , 3
Tại vị trí 0,45 mol
→ D S N a + : 0 , 45 N O 3 - : 0 , 4 → A l O 2 - : 0 , 05 → m A l + M g + 0 , 3 . 17 - 0 , 05 . 78 = 4 , 08 → m A l + M g = 2 , 88 → m m u ố i = 2 , 88 + 0 , 3 . 62 = 21 , 48

Gọi số mol K và Al trong hỗn hợp x, y
2K + 2H2O → KOH + H2 (1)
x x (mol)
2Al + 2KOH + 2H2O → 2KAlO2 + 3H2↑ (2)
y y (mol)
Do x tan hết nên Al hết, KOH dư sau (2). Khi thêm HCl, ban đầu chưa có kết tủa vì:
HCl + KOH → KCl + H2O (3)
X – y x – y (mol)
Khi HCl trung hòa hết KOH dư thì bắt đầu có kết tủa:
KAlO2 + HCl + H2O → Al(OH)3 ↓ + KCl (4)
Vậy để trung hòa KOH dư cần 100 ml dung dịch HCl 1M.
Ta có: nHCl = nKOH dư sau phản ứng (2) = x – y = 0,1.1 = 0,1 (mol) (I)
Mặt khác: 39x + 27 y = 10,5 (II)
Từ (1) và (II) => x = 0,2; y = 0,1.
% nK = 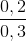 .100% = 66,67%;
.100% = 66,67%;
%nAl = 100% - 66,67% = 33,33%.
K + HOH --> KOH +1/2H2
Al + KOH + HOH --> KAlO2 +3/2H2
-Cho HCl vào bd kg có ket tua => KOH du
HCl + KOH --> KCl + HOH
-Sau đó có ket tua => KOH het => KAlO2 phan ung
KAlO2 + HCl + HOH --> Al(OH)3 + KCl
vì den 100ml dd HCl 1M co xuat hien ket tua nen => n(KAlO2) =n(HCl) = 0,1
=> n(Al) = 0,1
=> %Al = 25,71%
=> %K =74,29%
Luu y: hoi hóa xem bai giai co dung hay co van de nao kg gop ý dum nha thanks

C2H2 + 2AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
CH3CHO + 2AgNO3 + 3NH3 + H2O → CH3COONH4 + 2Ag ↓ + 2NH4NO3
C2Ag2 + 2HCl → 2AgCl ↓ + C2H2 ↑
Y(AgCl, Ag) + HNO3 --> ...
Ag + 2HNO3 → AgNO3 + NO2 ↑ + H2O

Coi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>ACoi hh gồm FeO và Fe2O3
nFeO=x,nFe2O3=y
72x + 160y = 5.36
x=0.01*3 ( bt e)
=> y=0.02
3Fe2+ + 4H+ + NO3- = 3Fe3+ + NO + 2H2O
0.02-----0.08-----0.01
=> nO2-=0.09=> nH+ pứ=0.09*2+0.01*4=0.22 => nH+ dư=0.17
=> nFe3+ = 0.03+0.02*2=0.07
3Cu + 8H+ + 2NO3- = 3Cu2+ + 2NO + 4H2O
0.03----0.08----0.02------0.03
Cu + 2Fe3+ =2Fe2+ + Cu2+
0.01--0.02------0.02
Áp dụng đl bt đt
=> nSO42- = (0.04*2 + 0.02*2 + 0.05*3)/2=0.135
=> mM' = 0.04*65 + 0.07*56 + 0.135*96 = 19.44g
=>C

MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

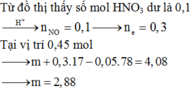
Chọn đáp án C.