Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
n H 2 = 0 , 2 ( m o l )
=> mhh= mFe + mAl
Bảo toàn electron:
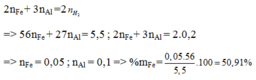

a) Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\) \(\Rightarrow27a+56b=11\) (1)
Ta có: \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Bảo toàn electron: \(3a+2b=0,4\cdot2=0,8\) (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,2\cdot27}{11}\cdot100\%\approx49,09\%\\\%m_{Fe}=50,91\%\end{matrix}\right.\)
b) Bảo toàn nguyên tố: \(\left\{{}\begin{matrix}n_{AlCl_3}=n_{Al}=0,2\left(mol\right)\\n_{FeCl_2}=n_{Fe}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{muối}=m_{AlCl_3}+m_{FeCl_2}=0,2\cdot133,5+0,1\cdot127=39,4\left(g\right)\)
c) Bảo toàn electron: \(3\cdot0,2+3\cdot0,1=2n_{SO_2}\)
\(\Rightarrow n_{SO_2}=0,45\left(mol\right)\) \(\Rightarrow V_{SO_2}=0,45\cdot22,4=10,08\left(l\right)\)
a) Gọi nAl = x, nFe = y
Có 27x + 56y = 11 (1)
Bảo toàn e
3x + 2y = 2.0,4 (2)
Từ 1 và 2 => x = 0,2, y = 0,1
\(\%mAl=\dfrac{0,2.27}{11}.100\%=49,09\%\)
\(\%mFe=100-49,09=50,91\%\)
b) BTKL:
m muối = mkim loại + mHCl - mH2
= 11 + 0,4.2.36,5 - 0,4.2 = 39,4g
c)
Bảo toàn e
Al => Al+3 + 3e S+6 + 2e => S+4
0,2 0,6 2x x
Fe => Fe+3 + 3e
0,1 0,3
=> 2x = 0,6 + 0,3 => x = 0,45 mol
=> VSO2 = 0,45.22,4 = 10,08 lít

\(n_{H_2}=\dfrac{0,784}{22,4}=0,035\left(mol\right)\\ Đặt:n_{Al}=a\left(mol\right);n_{Fe}=b\left(mol\right)\left(a,b>0\right)\\ PTHH:2Al+6HCl\rightarrow2AlCl_3+3H_2\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ \Rightarrow\left\{{}\begin{matrix}27a+56b=1,39\\1,5a+b=0,035\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,01\\b=0,02\end{matrix}\right.\\ \Rightarrow\%m_{Al}=\dfrac{0,01.27}{1,39}.100=37,53\%\\ \Rightarrow\%m_{Fe}=100\%-37,53\%=62,47\%\)

Gọi a,b lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu
=> 27a+56b=8,3 (1)
\(n_{H_2}=\dfrac{5,6}{22,4}=0,25mol\)
Ta có quá trình trao đổi elcetron
\(Al^0\rightarrow Al^{+3}+3e\)
a----------------3a--(mol)
\(Fe^0\rightarrow Fe^{+2}+2e\)
b----------------2b--(mol)
\(2H^{-1}+2e\rightarrow H_2^0\)
----------0,5------0,25-(mol)
Áp dụng định luật bảo toàn e ta có: 3a+2b=0,5 (2)
Giải hệ phương trình gồm (1) và (2) ta được: \(\left\{{}\begin{matrix}a=0,1\\b=0,1\end{matrix}\right.\)
\(\left[{}\begin{matrix}m_{Al}=0,1\cdot27=2,7g\\m_{Fe}=0,1\cdot56=5,6g\end{matrix}\right.\)

Ta có: \(n_{H_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
BTNT, có: \(n_{SO_4}=n_{H_2SO_4}=n_{H_2}=0,6\left(mol\right)\)
Mà: m muối = mKL + mSO4
⇒ m = mKL = 93,6 - 0,6.96 = 36 (g)
Bạn tham khảo nhé!

a) Gọi số mol của Al và Fe trong 13,8 gam hỗn hợp lần lượt là x và y
nH2 = 10,08:22.4= 0,45 mol
2Al + 3H2SO4 → Al2(SO4)3 + 3H2
x ------------------------------------------>3/2x
Fe + H2SO4 → FeSO4 + H2
y ------------------------------------> y
Ta có hệ pt\(\left\{{}\begin{matrix}27x+56y=13,8\\\dfrac{3}{2}x+y=0,45\end{matrix}\right.\) => x = 0,2 và y = 0,15
=> mFe = 0,15.56 = 8,4 gam <=> %mFe = \(\dfrac{8,4}{13,8}\).100% = 60,87%
b)
X + O2 → Y
Bảo toàn khối lượng => mO2 = mY - mX = 5,76 gam <=> nO2 = 0,18 mol
Ta có sơ đồ: \(\left\{{}\begin{matrix}Fe\\Al\end{matrix}\right.\) + O2 → Y \(\underrightarrow{H_2SO_4đ,n}\) → Fe2(SO4)3 + Al2(SO4)3 + SO2 + H2O
Các quá trình oxi hóa - khử:
Fe0 → Fe+3 + 3e O20 + 4e → 2O-2
0,15 -> 0,45 0,18 --> 0,72
Al0 → Al+3 + 3e S+6 + 2e → S+4
0,2 -> 0,6 2x <- x
Áp dụng ĐLBT electron => 2x + 0,72 = 0,45 + 0,6
<=> x = 0,165
=>V SO2 đktc = 0,165.22,4 = 3,696 lít
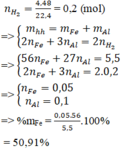
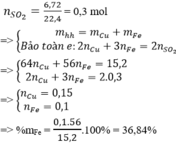

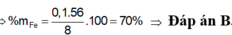
Gọi $n_{Al} = a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 5,5(1)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
Theo PTHH : $n_{H_2} = 1,5a + b = \dfrac{4,48}{22,4} = 0,2(2)$
Từ (1)(2) suy ra : a = 0,1 ; b = 0,05
$\%m_{Al} = \dfrac{0,1.27}{5,5}.100\% = 49,1\%$
$\%m_{Fe} = 100\% - 49,1\% = 50,9\%$