Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

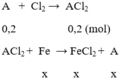
số mol FeCl2 là n = 0,25 . 0,4 = 0,1 (mol)
gọi x là số mol Fe phản ứng
khối lượng kim loại tăng là Δm = mA - mFe = Ax – 56x = 0,8
x = 0,1 → A.0,1 – 56.0,1 = 0,8 → A = 64. A là Cu
số mol Cu là nCu = 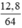 = 0,2 (mol)
= 0,2 (mol)
số mol CuCl2 → n(CuCl2) = nCu = 0,2 (mol)
nồng độ mol/l CuCl2 là C(M(CuCl2)) = 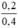 = 0,5M
= 0,5M

Đáp án C
nAl = 0,06 (mol) ; nHNO3 = 0,28 (mol)
BT e: ne (Al nhường) = 0,06. 3 = 0,18 < n e (N+5 nhận ) = (0,28: 4). 3 = 0,21
=> nHNO3 dư = 0,28 – 4nNO = 0,28 – 4. 0,06 = 0,04 (mol)
Vậy dd X thu được gồm: Al3+ : 0,06 mol ; H+ : 0,04 mol; NO3- : 0,22 mol
nH2 = 0,125 (mol) => n e (KL kiềm nhận) = 2nH2 = 0,25 (mol)
Khi cho KL kiềm + axit thiếu thì khi phản ứng hết với axit KL sẽ tiếp tục phản ứng với H2O để tạo thành dd bazơ
=> dd Y thu được phải chứa OH- : y (mol); ( y < 0,25 mol)
Trộn X + Y → nAl(OH)3 ↓ = 0,02 (mol) xảy ra các PTHH sau:
H+ + OH - → H2O
0,04→ 0,04
Al3+ + 3OH- → Al(OH)3
0,06 ← 0,02
=> ∑ nOH- = 0,04 + 0,06 = 0,1 (mol) = y
=> nHCl = 0,25 – 0,1 = 0,15 (mol) => CM = 0,15 : 0,5 = 0,3 (M)

nFe = 0,15 mol ; nCu = 0,1 ; nAg+ = 0,7 mol
Fe + 2Ag+ → Fe2+ + 2Ag (1)
0,15→ 0,3 0,15 0,3
Cu + 2Ag+ → Cu2+ + 2Ag
0,1 → 0,2 0,2
Fe2+ + Ag+ → Fe3+ + Ag (3)
0,15 → 0,15 0,15
Từ (1) ; (2) → m = (0,3 + 0,2 + 0,15).108 = 70,2 gam → Đáp án A

Giải thích:
nHCl = (25. 3,65%)/( 100%. 36,5) = 0,025 (mol) => ne = 0,025.2 = 0,05 (mol)
MX = 0,575 : 0,05 = 23 => Na
Đáp án A

Giải thích:
nOH- = nH+ = nHCl = ( 50.3,65%):(100%. 36,5) = 0,05 (mol)
X + nH2O → X(OH)n + nH2↑
=> MX = 1,15 : 0,05n = 23n
Vậy n = 1 => MX = 23 => Na
Đáp án A
Đáp án B
nKOH = nK = 1,95/39 = 0,05 (mol)
=> [KOH] = n :V = 0,05 : 0,5 = 0,1 (M)
=> pH = 14 + lg[OH-] = 14 -1 = 13