Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án C
Đặt n N 2 = x ; n N H 4 + = y ⇒ n H N O 3 p u = 12 x + 10 y = 2 m o l
Bảo toàn electron:
10x+8y=3x.0,54
![]()

Chọn đáp án C
+ Đặt nNH4NO3 = a || nN2 = b
⇒ 10nNH4NO3 + 8nN2 = 3nAl = 1,62 (1)
⇒ 12nNH4NO3 + 10nN2 = nHNO3 = 2 (2)
+ Giải hệ (1) và (2) ⇒ b = nN2 = 0,05 mol
⇒ VN2 = 1,12 lít ⇒ Chọn C

Đáp án C
+ Đặt nNH4NO3 = a , nN2 = b
⇒ 10nNH4NO3 + 8nN2 = 3nAl = 1,62 (1)
⇒ 12nNH4NO3 + 10nN2 = nHNO3 = 2 (2)
+ Giải hệ (1) và (2) ⇒ b = nN2 = 0,05 mol
⇒ VN2 = 1,12 lít

Đáp án B
+ Đặt nNH4NO3 = a || nN2 = b
⇒ 10nNH4NO3 + 8nN2 = 3nAl = 1,62 (1)
⇒ 12nNH4NO3 + 10nN2 = nHNO3 = 2 (2)
+ Giải hệ (1) và (2) ⇒ b = nN2 = 0,05 mol
⇒ VN2 = 1,12 lít

Chọn đáp án B
nAl = 0,02 mol; nZn = 0,05 mol; nNaOH = 0,485 mol.
NaOH + Y → dung dịch trong suốt {NaAlO2, Na2ZnO2, NaNO3}
Bảo toàn nguyên tố Natri: nNO3–/Y = nNaNO3 = 0,365 mol.
► Hòa tan "hoàn toàn" ⇒ HNO3 dư hoặc đủ, kim loại hết.
Đặt nNH4+ = x; nN2 = y. Bảo toàn electron:
8x + 10y = 0,02 × 3 + 0,05 × 2. Bảo toàn nguyên tố Nitơ:
∑nN/spk = 0,394 - 0,365 = x + 2y || Giải hệ có:
⇒ x = 0,005 mol; y = 0,012 mol ⇒ V = 268,8 ml ⇒ chọn B.

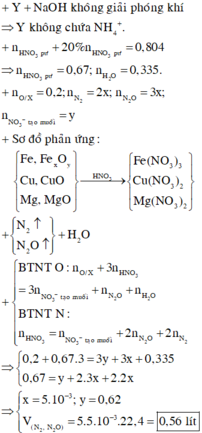
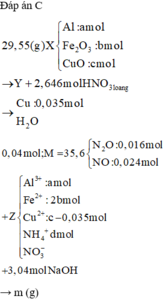


Đáp án A
nAl = 0,54
Gọi