Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
____0,05<------------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6 - 2,8 = 3,2 (g)
=> D

a, gọi a= nFe
b= nFeO
=> 56a + 72b= 12,8 (1)
Fe +H2SO4 -> FeSO4 +H2
a b b a
FeO +H2SO4 -> FeSO4 +H2O
b b b
a=nH2 = 2,24/22,4= 0,1 mol
từ (1) => b= 0,1
mFe= 56.0,1=5,6(g)
m FeO = 72.0,1= 7,2(g)
b, nH2SO4 (bđ) = 0,25 mol
nH2SO4 pứ = a+b =0,2 mol
=> nH2SO4 dư = 0,25-0,2=0,05 mol
2NaOH +H2SO4 -> Na2SO4 +2H2O
0,1 0,05
V(NaOH)= 0,1/ 1= 0,1 lit =100ml

Chọn C
Gọi số mol của Fe và Al lần lượt là x và y mol

Muối trong dung dịch A gồm x mol F e S O 4 và 0,5y mol A l 2 ( S O 4 ) 3


\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
Gọi x, y lần lượt là số mol Al, Fe
Theo đề bài ta có hệ pt
\(\left\{{}\begin{matrix}27x+56y=8,3\\\dfrac{3}{2}x+y=\dfrac{5,6}{22,4}=0,25\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}x=0,1\\y=0,1\end{matrix}\right.\)
a)\(x=\dfrac{\dfrac{0,1.3}{2}+0,1}{0,2}=0,25M\)
b)\(\%m_{Al_2(SO_4)_3}=\dfrac{\dfrac{0,1}{2}.342}{\dfrac{0,1}{2}.342+0,1.152}.100=52,94\%\)
=> %mFeSO4=100-52,94=47,06%
c)\(CM_{Al_2(SO_4)_3}=\dfrac{0,05}{0,2}=0,25M\)
\(CM_{FeSO_4}=\dfrac{0,1}{0,2}=0,5M\)
d) 1> Thu được kết tủa bé nhất
-TH1 : Lượng KOH chỉ phản ứng với FeSO4 tạo kết tủa, không đủ để tạo kết tủa với Al2(SO4)3
\(2KOH+FeSO_4\rightarrow Fe\left(OH\right)_2+K_2SO_4\)
=> \(m_{ddKOH}=\dfrac{0,1.2.56}{15\%}=74,67\left(g\right)\)
TH2: Lượng KOH phản ứng với FeSO4 tạo kết tủa và tạo kết tủa với Al2(SO4)3 sau đó tan kết tủa của Al2(SO4)3
\(2KOH+FeSO_4\rightarrow K_2SO_4+Fe\left(OH\right)_2\)
\(6KOH+Al_2(SO_4)_3\rightarrow2Al\left(OH\right)_3+3K_2SO_4\)
\(Al\left(OH\right)_3+KOH\rightarrow KAlO_2+2H_2O\)
=>\(m_{ddKOH}=\dfrac{\left(0.1.2+0,05.6+0,1\right).56}{15\%}=224\left(g\right)\)
2> Thu được kết tủa lớn nhất :
Lượng KOH phản ứng với FeSO4 tạo kết tủa và tạo kết tủa với Al2(SO4)3 và không tan kết tủa của Al2(SO4)3
\(2KOH+FeSO_4\rightarrow K_2SO_4+Fe\left(OH\right)_2\)
\(6KOH+Al_2(SO_4)_3\rightarrow2Al\left(OH\right)_3+3K_2SO_4\)
=>\(m_{ddKOH}=\dfrac{\left(0.1.2+0,05.6\right).56}{15\%}=186,67\left(g\right)\)
Đặt \(\left\{{}\begin{matrix}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{matrix}\right.\)
\(PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
\(\left(mol\right)\) \(a\) \(1,5a\) \(0,5a\) \(1,5a\)
\(PTHH:Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(\left(mol\right)\) \(b\) \(b\) \(b\) \(b\)
Ta có hpt: \(\left\{{}\begin{matrix}27a+56b=8,3\\1,5a+b=\dfrac{5,6}{22,4}\end{matrix}\right.\Leftrightarrow a=b=0,1\left(mol\right)\)
\(a.x=\dfrac{1,5a+b}{0,2}=\dfrac{0,15+0,1}{0,2}=1,25\left(M\right)\\ b.\%m_{Al}=\dfrac{27.0,1}{8,3}.100=32,53\left(\%\right)\\ \%m_{Fe}=100-32,53=67,47\left(\%\right)\\ c.C_{M_{Al_2\left(SO_4\right)_3}}=\dfrac{0,5a}{0,2}=0,25\left(M\right)\\ C_{M_{FeSO_4}}=\dfrac{b}{0,2}=0,5\left(M\right)\\ d.\)
\(PTHH:Al_2\left(SO_4\right)_3+6KOH\rightarrow3K_2SO_4+2Al\left(OH\right)_3\)
\(\left(mol\right)\) \(0,05\) \(0,3\) \(0,1\)
\(PTHH:FeSO_4+2KOH\rightarrow Fe\left(OH\right)_2+K_2SO_4\)
\(\left(mol\right)\) \(0,1\) \(0,2\)
\(PTHH:Al\left(OH\right)_3+KOH\rightarrow KAlO_2+2H_2O\)
\(\left(mol\right)\) \(0,1\) \(0,1\)
\(d.1.\) Lượng kết tủa bé nhất khi kết tủa \(Al\left(OH\right)_3\) sinh ra tan hết trong dd KOH
Khi đó: \(n_{KOH}=0,6\left(mol\right)\rightarrow m_{ddKOH}=\dfrac{0,6.100.56}{15}=224\left(g\right)\)
\(d.2.\) Lượng kết tủa lớn nhất khi KOH tác dụng vừa đủ với dd A
Khi đó: \(n_{KOH}=0,5\left(mol\right)\rightarrow m_{ddKOH}=\dfrac{0,5.56.100}{15}=186,67\left(g\right)\)

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
_____0,05<--------------------0,05
=> mFe = 0,05.56 = 2,8 (g)
=> mCu = 6-2,8 = 3,2 (g)
=> A

Bài 1 :
Số mol của nhôm
nAl = \(\dfrac{m_{Al}}{M_{Al}}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
Pt : 2Al + 3H2SO4 → Al2(SO4)3 + 3H2\(|\)
2 3 1 3
0,2 0,3 0,3
a) Số mol của dung dịch axit sunfuric
nH2SO4 = \(\dfrac{0,2.3}{2}=0,3\left(mol\right)\)
Thể tích của dung dịch axit sunfuric
CMH2SO4 = \(\dfrac{n}{V}\Rightarrow V=\dfrac{n}{C_M}=\dfrac{0,3}{0,2}=1,5\left(l\right)\)
b) Số mol của khí hidro
nH2 = \(\dfrac{0,3.3}{3}=0,3\left(mol\right)\)
Thể tích của khí hidro ở dktc
VH2 = nH2 . 22,4
= 0,3. 22,4
= 6,72 (l)
Chúc bạn học tốt
2. Để hòa tan hoàn toàn m(g) kẽm cần vừa đủ 100(g) dung dịch H2SO4 4,9% .
a) Tìm m?
b) Tìm V lít khí thoát ra ở đktc?
c) Tính C% của muối thu được sau sau phản ứng?
---
a) mH2SO4=4,9%.100=4,9(g) -> nH2SO4=4,9/98=0,05(mol)
PTHH: Zn + H2SO4 -> ZnSO4 + H2
Ta có: nZn=nZnSO4=nH2=nH2SO4=0,05(mol)
m=mZn=0,05.65=3,25(g)
b) V(H2,đktc)=0,05.22,4=1,12(l)
c) mZnSO4=0,05. 161=8,05(g)
mddZnSO4=mZn + mddH2SO4 - mH2= 3,25+100 - 0,05.2=103,15(g)
=> C%ddZnSO4= (8,05/103,15).100=7,804%

2Al + 3H2SO4 → Al2(SO4)3 + 3H2
2 3 1 3
0,2 0,3
nAl=\(\dfrac{5,4}{27}\)=0,2(mol)
Ta có: nH2 = \(\dfrac{0,2.3}{2}\)= 0,3(mol)
⇒ VH2 = n . 22,4 = 0,3 . 22,4= 6,72l
Ủa??? kì z??![]()


Vậy n = 3, R = 56 thỏa mãn, oxit là F e 2 O 3
n F e 2 O 3 = 20 160 = 0,125 m o l
m m u o i = m F e S O 4 + m F e 2 ( S O 4 ) 3
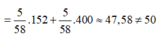
![]()
Đáp án: D


\(n_{Al}=\dfrac{0,27}{27}=0,01\left(mol\right)\)
PTHH: 2Al + 3H2SO4 --> Al2(SO4)3 + 3H2
____0,01------------------------------->0,015
=> VH2 = 0,015.22,4 = 0,336 (l) = 336ml
=> D