Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

nSO2= 0,4(mol)
Đặt: nAl=a(mol); nMg=b(mol) (a,b>0)
PTHH: 2 Al + 6 H2SO4(đ) -to-> Al2(SO4)3 + 3 SO2 + 6 H2O
a____________3a______0,5a___________1,5a(mol)
Mg + 2 H2SO4(đ) -to-> MgSO4 + SO2 + 2 H2O
b_____2b________b________b(mol)
Ta có hpt:
\(\left\{{}\begin{matrix}27a+24b=7,8\\1,5a+b=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\)
=> mMg=0,1.24=2,4(g)
=>%mMg=(2,4/7,8).100=30,769%
=> %mAl= 69,231%

\(n_{Mg}=a\left(mol\right),n_{Al}=b\left(mol\right)\)
\(24a+27b=15\left(1\right)\)
Bảo toàn e :
\(2a+3b=0.1\cdot\left(2+3+1+8\right)\left(2\right)\)
\(\left(1\right),\left(2\right):\)
\(a=0.4,b=0.2\)
\(\%Mg=64\%,\%Al=36\%\)

Gọi số mol Al và Fe lần lượt là a;b
$\Rightarrow 27a+56b=8,3$
Bảo toàn e ta có: $3a+3b=0,6$
Giải hệ ta được $a=b=0,1$
$\Rightarrow m_{Al}=2,7(g);m_{Fe}=5,6(g)$
\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=8.3\left(g\right)\left(1\right)\)
\(n_{SO_2}=\dfrac{6.72}{22.4}=0.3\left(mol\right)\)
\(BTe:\)
\(3a+3b=0.3\cdot2=0.6\left(2\right)\)
\(\left(1\right),\left(2\right):a=b=0.1\)
\(m_{Al}=0.1\cdot27=2.7\left(g\right)\)
\(m_{Fe}=5.6\left(g\right)\)

\(n_{Al}=a\left(mol\right),n_{Fe}=b\left(mol\right)\)
\(m=27a+56b=6.95\left(g\right)\left(1\right)\)
\(n_{NO_2}=\dfrac{10.08}{22.4}=0.45\left(mol\right)\)
Bảo toàn e :
\(3a+3b=0.45\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.05,b=0.1\)
\(m_{Al}=0.05\cdot27=1.35\left(g\right)\)
\(m_{Fe}=0.1\cdot56=5.6\left(g\right)\)

Giả sử số mol của Mg, Al trong Y lần lượt là a, b (mol)
=> 24a + 27b = 5,1
PTHH: Mg + 2HCl --> MgCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
=> a + 1,5b = 0,25
=> a = 0,1 ; b = 0,1
Gọi số mol Na là k (mol)
\(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
PTHH: 2Na + 2H2O --> 2NaOH + H2
k-------------------->k---->0,5k
2Al + 2NaOH + 2H2O --> 2NaAlO2 + 3H2
k<-----k------------------------------>1,5k
=> 0,5k + 1,5k = 0,4
=> k = 0,2 (mol)
=> nAl(X) = 0,2 + 0,1 = 0,3 (mol)
=> mAl(X) = 0,3.27 = 8,1 (g)

Coi X gồm Fe và O.
Ta có: 56nFe + 16nO = 49,6 (1)
\(n_{SO_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
BT e, có: 3nFe - 2nO = 2nSO2 = 0,8 (2)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{Fe}=0,7\left(mol\right)\\n_O=0,65\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\%m_O=\dfrac{0,65.16}{49,6}.100\%\approx20,97\%\)
Muối thu được là Fe2(SO4)3
BTNT Fe, có: \(n_{Fe_2\left(SO_4\right)_3}=\dfrac{1}{2}n_{Fe}=0,35\left(mol\right)\)
\(\Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,35.400=140\left(g\right)\)

a) nMg:a(mol) ,nAl:b(mol)
nNO=2,464/22,4=0,11(mol)
hpt: mX=24a+27b=3,42
nNO=23a+b=0,11
→a=0,075(mol),b=0,06(mol)
%mMg=(0,075.24/3,42).100%=52,63%
%mAl=100%−52,63%=47,37%
b)
nHNO3=4nNO=0,44(mol)
mdd HNO3=(0,44.63)/10%=277,2(g)

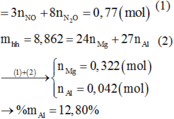
Gọi $n_{Al} =a (mol) ; n_{Mg} = b(mol) \Rightarrow 27a + 24b = 7,8(1)$
Bảo toàn electron : $3n_{Al} + 2n_{Mg} = 2n_{SO_2}$
$\Rightarrow 3a + 2b = 0,4.2(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,1
$\%m_{Al} = \dfrac{0,2.27}{7,8}.100\% = 69,23\%$
$\%m_{Mg} = 100\% - 69,23\% = 30,77\%$
b) $n_{Al_2(SO_4)_3} = \dfrac{1}{2}n_{Al} = 0,1(mol)$
$n_{MgSO_4} = n_{Mg} = 0,1(mol)$
$\Rightarrow m_{muối} = 0,1.342 + 0,1.120 = 46,2(gam)$