Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(nSO_2=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(nKOH=\dfrac{0,4}{2}=0,2\left(mol\right)\)
\(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
=> dd X có những chất tan gồm K2SO3 và KOH.
\(n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{KOH}=0,4.2=0,8\left(mol\right)\)
Xét \(T=\dfrac{0,8}{0,3}=\dfrac{8}{3}>2\) => phản ứng tạo muối trung hoà và có dư KOH
=> dd sau phản ứng gồm K2SO3 và KOH

Đáp án B
![]()
Các phương trình phản ứng xảy ra:
SO2 + KOH → KHSO3
0,1 0,1 0,1 mol
SO2 + 2KOH → K2SO3 + H2O
0,05 0,1 mol
Tổng số mol SO2 = 0,15 mol
→ V = 3,36 lit

1) Ptpư:
2Al + 6HCl \(\rightarrow\) 2AlCl3 + 3H2
Fe + 2HCl \(\rightarrow\) FeCl2 + H2
Cu + HCl \(\rightarrow\) không phản ứng
=> 0,6 gam chất rắn còn lại chính là Cu:
Gọi x, y lần lượt là số mol Al, Fe
Ta có:
3x + 2y = 2.0,06 = 0,12
27x + 56 y = 2,25 – 0,6 = 1,65
=> x = 0,03 (mol) ; y = 0,015 (mol)
=> \(\%Cu=\frac{0,6}{2,25}.100\%=26,67\%\); \(\%Fe=\frac{56.0,015}{2,25}.100\%=37,33\%\); %Al = 36%
2) \(n_{SO_2}=\frac{1,344}{22,4}=0,06mol\); m (dd KOH) = 13,95.1,147 = 16 (gam)
=> mKOH = 0,28.16 = 4,48 (gam)=> nKOH = 0,08 (mol)=> \(1<\)\(\frac{n_{KOH}}{n_{SO_2}}<2\)
=> tạo ra hỗn hợp 2 muối: KHSO3: 0,04 (mol) và K2SO3: 0,02 (mol)
Khối lượng dung dịch sau pu = 16 + 0,06.64 = 19,84 gam
=> \(C\%\left(KHSO_3\right)=\frac{0,04.120}{19,84}.100\%\)\(=24,19\%\)
\(C\%\left(K_2SO_3\right)=\frac{0,02.158}{19,84}.100\%\)\(=15,93\%\)

Kí hiệu CO 2 và SO 2 là YO 2 => Σn YO 2 cần dùng = 0,25 mol
Chất tan sinh ra khi dung dịch NaOH hấp thụ tối đa YO 2 sẽ là NaHYO 3
YO 2 + NaOH → NaHYO 3
a = 0,25/0,5 = 0,5 (mol/l)

\(SO_2+2KOH\rightarrow K_2SO_3+H_2O\)
\(n_{KOH}=2.0,2=0,4\left(mol\right)\)
\(\Rightarrow n_{K_2SO_3}=\frac{0,4.1}{2}=0,2\left(mol\right)\)
\(\Rightarrow m_{K_2SO_3}=0,2.158=31,6\left(g\right)\)
#trannguyenbaoquyen

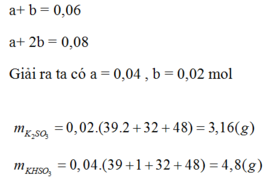


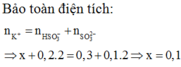

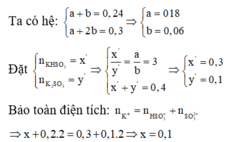
Đáp án C.