
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


5.
\(n_{Na}=a\left(mol\right)\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)
\(a...............a.....0.5a\)
\(m_{\text{dung dịch sau phản ứng}}=23a+500-0.5a\cdot2=22a+500\left(g\right)\)
\(m_{NaOH}=40a\left(g\right)\)
\(C\%_{NaOH}=\dfrac{40a}{22a+500}\cdot100\%=20\%\)
\(\Rightarrow a=2.8\)
\(b.\)
\(n_{H^+}=10^{-3}\cdot V\cdot\left(1+0.5\cdot2\right)=2\cdot10^{-3}V\left(mol\right)\)
\(\Rightarrow n_{NaOH}=2\cdot10^{-3}V=2.8\left(mol\right)\)
\(\Rightarrow V=1400\)

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
\(2C_2H_5OH+2Na\rightarrow2C_2H_5ONa+H_2\)
0,1 0,05 ( mol )
\(m_{C_2H_5OH}=0,1.46=4,6g\)


a) HCl +NaOH-----> NaCl + H2O
b)Ta có
nHCl=0,4.0,5=0,2(mol)
mNaOH=50.40100=20(g)
nNaOH=2040=0,5(mol)
=> NaOH dư
=> dd A gồm NaOH dư và NaCl
Theo pthh
nNaOH=nHCl=0,2(mol)
nNaOHdư=0,5−0,2=0,3(mol)
CM(HCl)=0,30,6=0,5(M)
Theo pthh
nNaCl=nNaOH=0,2(mol)
CM(NaCl)=0,20,6=0,33(M)
Chúc bạn học tốt

\(\%Fe_{FeCl_3}=\dfrac{56}{56+35.5\cdot3}\simeq34,46\%\)
Fe không có trong CuSO4 nha bạn

\(M_{KNO_3}=39+14+16\cdot3=101g/mol\\ M_{H_2SO_4}=1\cdot2+32+16\cdot4=98g/mol\\ M_{CuSO_4}=64+32+16\cdot4=160g/mol\\ M_{Al\left(OH\right)_3}=27+\left(1+17\right)\cdot3=78g/mol\\ M_{NaCl}=23+35,5=58,5g/mol\)

Bài 2:
Gọi x,y lần lượt là KL dung dịch NaOH 10% và KL dd NaOH 20% (x,y>0)
=> (1) : x+y=400
Mặt khác, KL chất tan của NaOH tổng là : 400.16%=64(g)
=> (2) 0,1x+0,2y=64
Từ (1), (2) ta có hpt:
\(\left\{{}\begin{matrix}x+y=400\\0,1x+0,2y=64\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=160\\y=240\end{matrix}\right.\)
=> Cần 160 gam dung dịch NaOH 10% và 240 gam dung dịch NaOH 20% để tạo ra 400 gam dung dịch NaOH 16%.
Chúc em học tốt!
Bài 4:
nH2SO4(2M)= 0,3(mol)
VddH2SO4(5M)= 200/1,29=20000/129(ml)=20/129(l)
=>nH2SO4(5M)= 5. 20/129=100/129(mol)
=> \(CMddH2SO4\left(mới\right)=\dfrac{0,3+\dfrac{100}{129}}{0,15+\dfrac{20}{129}}\approx3,525\left(M\right)\)

Câu 3:
\(a,n_{Fe}=x(mol);n_{Zn}=y(mol)\\ \Rightarrow 56x+65y=18,6(1)\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3(mol)\\ PTHH:Zn+H_2SO_4\to ZnSO_4+H_2\\ Fe+H_2SO_4\to FeSO_4+H_2\\ \Rightarrow x+y=0,3(2)\\ (1)(2)\Rightarrow x=0,1;y=0,2\\ \Rightarrow \%_{Fe}=\dfrac{0,1.56}{18,6}.100\%=30,11\%\\ \Rightarrow \%_{Zn}=100\%-30,11\%=69,89\%\)
\(b,\Sigma n_{H_2SO_4}=x+y=0,3(mol)\\ \Rightarrow C_{M_{H_2SO_4}}=\dfrac{0,3}{0,1}=3M\\ c,n_{ZnSO_4}=0,2(mol);n_{FeSO_4}=0,1(mol)\\ \Rightarrow m_{ZnSO_4}=0,2.161=32,2(g)\\ m_{FeSO_4}=0,1.152=15,2(g)\)
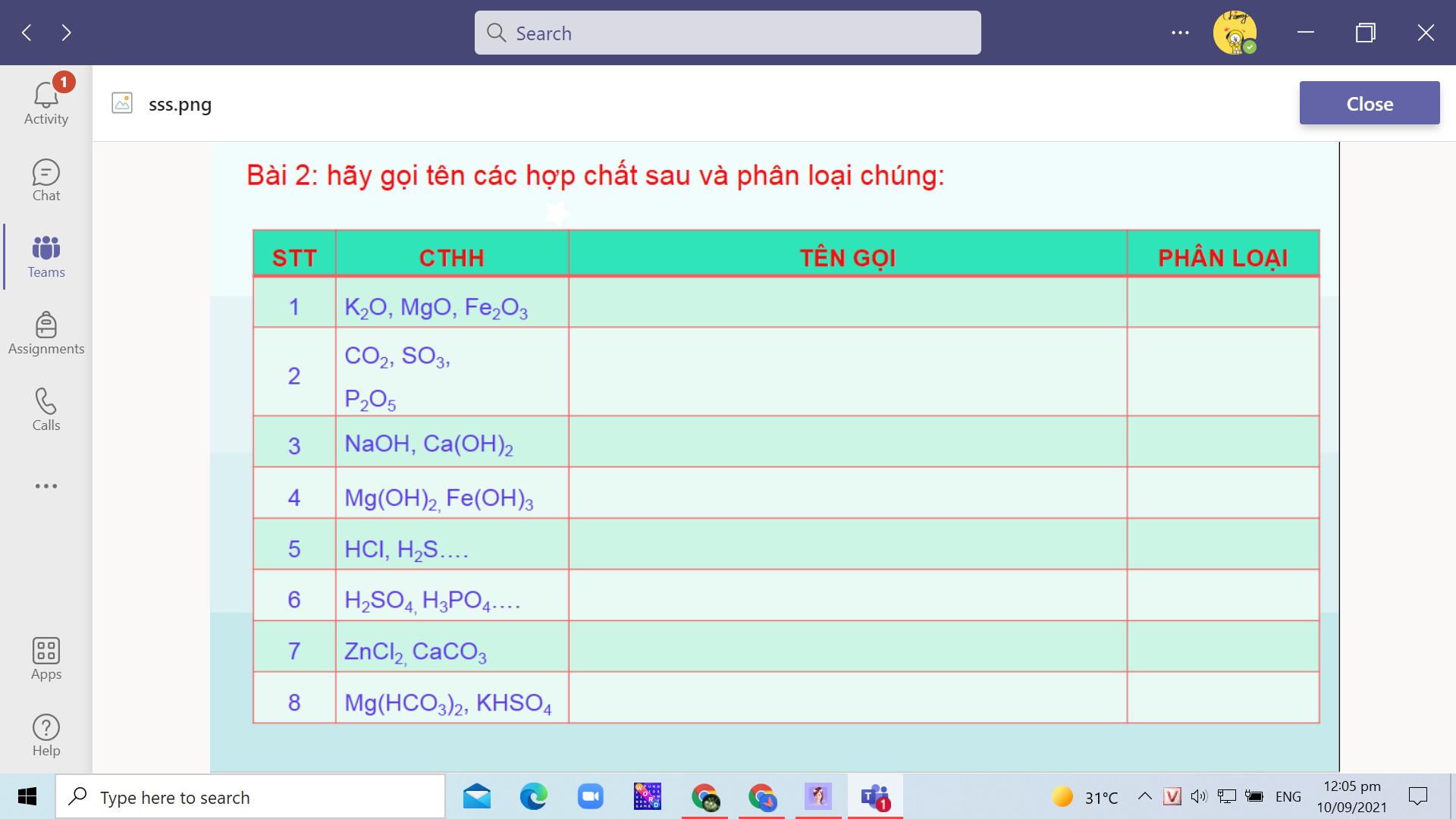




K2O: kali oxit: oxit bazơ
MgO: magie oxit: oxit bazơ
Fe2O3: sắt(lll) oxit: oxit bazơ
CO2: cacbon ddioxxit: oxit axit
SO3: lưu huỳnh trioxit: oxit axit
P2O5: điphotpho pentaoxit
NaOH: natri hidroxit: bazơ kiềm
Ca(OH)2: canxi hidroxit: bazơ không tan
Mg(OH)2: magie hidroxit: bazơ không tan
Fe(OH)3: sắt(llI) hidroxit: bazơ không tan
HCl: axit clohidric: axit không có oxi
H2S: axit sunfit: axit không có oxi
H2SO4: axit sunfuric: axit có oxi
H3PO4: axit photphoric: axit có oxi
ZnCl2: kẽm clorua: muối trung tính
CaCO3: canxi cacbonat: muối trung tính
Mg(HCO3)2: magie hidrocacbonat: muối axit
KHSO4: kali hidrosunfat: muối axit