
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(a.PTHH:\)
\(Mg+2HCl--->MgCl_2+H_2\left(1\right)\)
\(CuO+2HCl--->CuCl_2+H_2O\left(2\right)\)
b. Theo PT(1): \(n_{Mg}=n_{H_2}=0,25\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,25.24=6\left(g\right)\)
\(\Rightarrow m_{CuO}=24,25-6=18,25\left(g\right)\)
c. Ta có: \(n_{CuO}=\dfrac{18,25}{80}=\dfrac{73}{320}\left(mol\right)\)
\(\Rightarrow n_{hh}=\dfrac{73}{320}+0,25=0,478125\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_{hh}=2.0,478125=0,95625\left(mol\right)\)
Đổi 300ml = 0,3 lít
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,95625}{0,3}=3,1875M\)

a) nCuCl2 = 0,15.2 = 0,3 (mol)
PTHH: 2Al + 3CuCl2 --> 2AlCl3 + 3Cu
____0,2<------0,3--------->0,2---->0,3
=> m = 0,3.64 - 0,2.27 = 13,8 (g)
b) \(C_{M\left(AlCl_3\right)}=\dfrac{0,2}{0,15}=1,3333M\)

Ta có: \(p_1V_1=p_2V_2\Leftrightarrow V_2=\dfrac{P_1V_1}{P_2}=\dfrac{22,4.1}{27,3}=\dfrac{32}{39}\left(l\right)\) (1 mol chất khí)
\(\Rightarrow n_{H_2}=\dfrac{6,72}{\dfrac{32}{39}}=8,19\left(mol\right)\)

Các khí tm đề bài là H2,O2,CO2 SO2 do H2SO4đ có khả năng tác dụng với NH3 và CO
H2SO4 +2NH3 =>(NH4)2SO4
HayH2SO4 +CO =>SO2 + CO2 + H2O
* Điều kiện làm khô khí: hóa chất được sử dụng để làm khô khí ko tác dụng với khí được làm khô.
* Sau đây là một số kiến thức về các chất làm khô:
- H2SO4 đặc:
+ Làm khô được: Cl2, NO2, CO2, SO2, O3
+ Không làm khô được: NH3, CO, H2S, NO
- P2O5:
+ Làm khô được: CO2, SO2, H2S, Cl2, NO2, NO, CO, O3
+ Không làm khô được: NH3
- CaO:
+ Làm khô được: NH3, CO, O3, NO
+ Không làm khô được: CO2, SO2, NO2, H2S, Cl2
- NaOH rắn (khan):
+ Làm khô được: NH3, CO, O3, NO
+ Không làm khô được: CO2, SO2, NO2, H2S, Cl2
- CaCl2 khan:
+ Làm khô được: NH3, CO2, SO2, NO2, H2S, Cl2, NO, CO, O3.
* Quay lại bài toán:
Do H2SO4 đặc có tính oxi hóa mạnh nên sẽ tác dụng với những khí có tính khử mạnh NH3 và CO
Vậy những khí được làm khô gồm: H2, CO2, SO2, O2.

b. - Trích mỗi chất một ít làm mẫu thử.
| Na2O | P2O5 | MgO | |
| Qùy tím ẩm | Hóa xanh | Hóa đỏ | Không đổi màu |
PTHH:
\(Na_2O+H_2O\rightarrow2NaOH\\ P_2O_5+3H_2O\rightarrow2H_3PO_4\)
e.Dùng que diêm :
+Nếu cho diêm vào mà không có lửa thì đó là khí CO2
+Cho tàn đóm lửa của que diêm vào bình nếu bùng cháy là có khi Oxi
+Nếu như lửa trong bình khí đó cháy càng ngày càng to và bắt đầu chuyển sang màu xanh nhạt thì đó chính là khí Hidro

Bài 1 :
a) Khí đó là $SO_2$
$Na_2SO_3 + H_2SO_4 \to Na_2SO_4 + SO_2 + H_2O$
b) Dung dịch đó là $CuSO_4$
$CuO + H_2SO_4 \to CuSO_4 + H_2O$
c) Dung dịch đó là $Fe_2(SO_4)_3$
$Fe_2O_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 3H_2O$
$2Fe(OH)_3 + 3H_2SO_4 \to Fe_2(SO_4)_3 + 6H_2O$
d) Dung dịch đó là : $Al_2(SO_4)_3$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
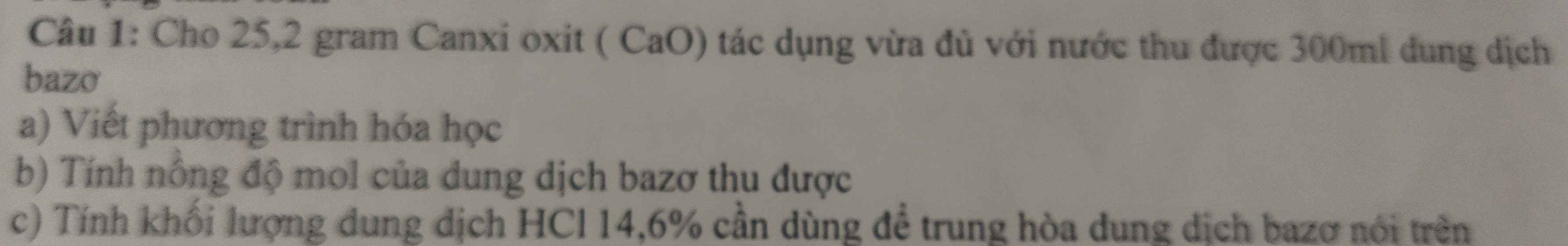



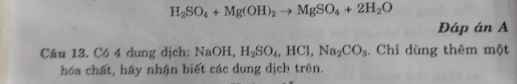
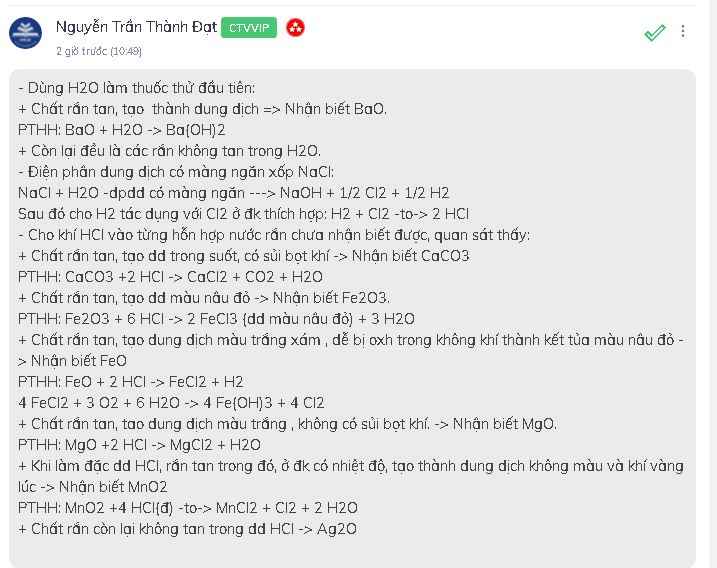



Bài 10) PTHH: CuO + H2SO4 → CuSO4 + H2O
Khối lượng dung dịch H2SO4 là:
( 0,2 . 98 ) : 20% = 98 gam
Khối lượng dung dịch A là: 0,2 . 80 + 98 = 114 gam
Khối lượng CuSO4 là: 0,2 . 160 = 32 gam
Khối lượng nước có trong dung dịch A là:144 - 32 = 82 gam
82 gam nước hoà tan hoàn toàn 32 gam CuSO4 để tạo ra 114 gam dung dịch bão hoà ở nhiệt độ này.
( Gọi Khối lượng CuSO4.5H2O là: m => Khối lượng CuSO4 kết tinh là \( {160m \over250}\) ; Khối lượng nước kết tinh là: \({90m \over 250}\) )
+) 100 gam nước hoà tan hoàn toàn 17,4 gam CuSO4 để tạo 117,4 gam dung dịch CuSO4 bão hoà
+) 82 - \({90m\ \over 250}\) gam nước hoà tan 32 - \( {160m\over 250}\) gam CuSO4 để tạo dung dịch bão hoà ở nhiệt độ này.
Nhân chéo 2 phương trình trên ta được pt sau:
<=> 100 ( 32 - \({160m\ \over 250}\) ) = 17,4 ( 82 - \( {90m \over 250}\) )
<=> 3200 - \( {16000m \ \over 250}\) = 1426,8 - \({1566m \over 250}\)
<=> m = 30,71 gam
Vậy khối lượng CuSO4 tách ra khỏi dung dịch là: 30,71 gam
Bạn tải lại trang là ok đó