
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


$2Fe + 6H_2SO_4 \to Fe_2(SO_4)_3 + 3SO_2 + 6H_2O(1)$
$Fe_2(SO_4)_3 + Fe\ to 3FeSO_4(2)$
Gọi $n_{Fe_2(SO_4)_3} = a(mol) ; n_{FeSO_4} = b(mol)$
Ta có : $400a + 152b = 62,8(1)$
$n_{SO_2} = 0,15(mol)$
$n_{Fe_2(SO_4)_3(1)} = \dfrac{1}{3}n_{SO_2} = 0,05(mol)$
$n_{Fe_2(SO_4)_3(2)} = \dfrac{1}{3}n_{FeSO_4} = \dfrac{b}{3}$
Suy ra:
$0,05 - \dfrac{b}{3} = a(2)$
Từ (1)(2) suy ra $a = \dfrac{45}{112} ; b = -1,055<0$
=> Sai đề

Bài 2) Ở 90 độ C:
- 100 gam nước hoà tan 50 gam KCl để tạo 150 gam dung dịch bão hoà ở nhiệt độ này
a) C% của dung dịch bão hoà tại 90 độ C là:
(Khối lượng chất tan/Khối lượng dung dịch) . 100%
<=> (50:150).100% = 33,33%
b) Ở 0 độ C:
Gọi m là khối lượng chất tan KCl ở 0o C => Khối lượng dung dịch tại nhiệt độ này là: 100+m
Theo đề bài ra ta có: m/100+m = 25,93%
=> m = 35 gam
Vậy ở 0 độ C độ tan của KCl trong nước là 35 gam
c) Ở 90 độ C:
100 gam nước hoà tan 50 gam KCl tạo 150 gam dd
=> 600 gam dung dịch tạo 200 gam KCl và 400 gam nước
- Ở 0 độ C:
100 gam nước hoà tan 35 gam KCl tạo 135 gam dd
=> 400 gam nước hoà tan được 140 gam KCl tạo 400 + 140 = 540 gam dung dịch
Vậy khi làm lạnh 600 gam dung dịch KCl từ 90 độ xuống 0 độ thì khối lượng dung dịch thu được là 540 gam



A là dung dịch H2SO4
B: Na2CO3
C: H2SO4 đặc
D: Xút (NaOH)
Khi cho DD H2SO4 tác dụng với Na2CO3 giải phóng khí SO2 mang theo hơi nước.
Bình C để giữ hơi nước lại trong bình (H2SO4 đặc háu nước) SO2 không tác dụng tiếp tục được dẫn qua bình đựng.
Để tránh SO2 thoát ra bên ngoài gây ô nhiễm môi trường và 1 số bệnh cho con người nên Xút được đặt ở miệng bình để tạo muối.


(1) S + O2 → SO2
(2) SO2 + CaO → CaSO3
(3) SO2 + H2O → H2SO3
(4) H2SO3 + 2NaOH → Na2SO3 + 2H2O
(5) Na2SO3 + H2SO4 → Na2SO4 + SO2↑ + H2O
(6) SO2 + 2NaOH →Na2SO3 + H2O

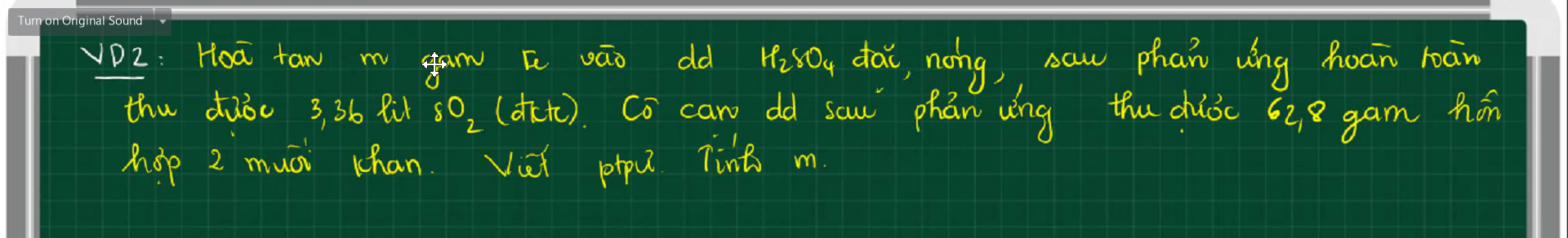









 Giúp mình nha !!!
Giúp mình nha !!!






Ta có: \(n_{H_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
\(a.PTHH:\)
\(Mg+2HCl--->MgCl_2+H_2\left(1\right)\)
\(CuO+2HCl--->CuCl_2+H_2O\left(2\right)\)
b. Theo PT(1): \(n_{Mg}=n_{H_2}=0,25\left(mol\right)\)
\(\Rightarrow m_{Mg}=0,25.24=6\left(g\right)\)
\(\Rightarrow m_{CuO}=24,25-6=18,25\left(g\right)\)
c. Ta có: \(n_{CuO}=\dfrac{18,25}{80}=\dfrac{73}{320}\left(mol\right)\)
\(\Rightarrow n_{hh}=\dfrac{73}{320}+0,25=0,478125\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_{hh}=2.0,478125=0,95625\left(mol\right)\)
Đổi 300ml = 0,3 lít
\(\Rightarrow C_{M_{HCl}}=\dfrac{0,95625}{0,3}=3,1875M\)