
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Câu 1:
\((1)Mg+H_2SO_4\to MgSO_4+H_2\\ (2)MgSO_4+2NaOH\to Mg(OH)_2\downarrow+Na_2SO_4\\ (3)Mg(OH)_2+2HCl\to MgCl_2+2H_2O\\ (4)MgCl_2+2AgNO_3\to Mg(NO_3)_2+2AgCl\downarrow\)
Câu 2:
\(a,Mg,Al,Cu,Ag\\ b,Mg,Al\\ Mg+2HCl\to MgCl_2+H_2\\ 2Al+6HCl\to 2AlCl_3+3H_2\)
\(c,\) Dùng Al vì Al bị thụ động hóa với \(H_2SO_4\) đặc nguội

Gọi CTC là \(C_xH_6\)
\(M_X=21\cdot2=42\)
\(\Rightarrow12x+6=42\Rightarrow x=3\)\(\Rightarrow CTC:C_3H_6\)
\(n_X=\dfrac{2,24}{22,4}=0,1mol\)
\(\Rightarrow m_X=42\cdot0,1=4,2g\)
\(BTC:n_{C\left(X\right)}=3\cdot0,1=0,3mol\)
Do \(KOHdư\Rightarrow n_{K_2CO_3}=n_C=0,3mol\)
\(\Rightarrow m_2=0,3\cdot138=41,4g\)

2. Ta có: \(n_{HCl}=0,4.2=0,8\left(mol\right)\)
PT: \(CaO+2HCl\rightarrow CaCl_2+H_2O\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(MgO+2HCl\rightarrow MgCl_2+H_2O\)
Gọi: \(\left\{{}\begin{matrix}n_{CaO}=x\left(mol\right)\\n_{Fe}=y\left(mol\right)\\n_{MgO}=z\left(mol\right)\end{matrix}\right.\) ⇒ 56x + 56y + 40z = 20,8
⇒ 56.(x + y) + 40z = 20,8 (1)
Theo PT: \(n_{HCl}=2n_{CaO}+2n_{Fe}+2n_{MgO}=2x+2y+2z=0,8\)
⇒ x + y = 0,4 - z (2)
Thay (2) vào (1) được 56.(0,4 - z) + 40z = 20,8
⇒ nMgO = z = 0,1 (mol)
Theo PT: \(n_{MgCl_2}=n_{MgO}=0,1\left(mol\right)\)
\(\Rightarrow m_{MgCl_2}=0,1.95=9,5\left(g\right)\)
Câu 1 bạn xem lời giải ở đây nhé.
https://hoc24.vn/cau-hoi/hoa-tan-hoan-toan-2914g-oxit-kim-loai-hoa-tri-1-vao-100ml-d-hcl-1679-sau-phan-ung-thu-duoc-dd-x-co-can-x-thu-duoc-4611g-chat-ran-tim-a.8554821623147

khi phảng ứng với axit và khi tác dụng với những muối clorua của các kim loại đứng sau sắt

CuO + H2 -> Cu + H2O
0.01 0.01
FexOy + yH2 -> xFe + yH2O
Fe + 2HCl -> FeCl2 + H2
\(\)0.02 0.02 \(\)
Cu + HCl -> (không phản ứng)
nH2 = 0.02mol => mFe = 1.12g
=> mCu = 1.76 - 1.12 = 0.64g => nCu = 0.01mol
=> mCuO = 0.8g => mFexOy = 2.4 - 0.8 = 1.6g
Ta có: 56x + 16y -> 56x
1.6g -> 1.12g
=> \(1.6\times56x=1.12\times\left(56x+16y\right)\)
=> \(26.88x=17.92y\Leftrightarrow\dfrac{x}{y}=\dfrac{2}{3}\)
=> Fe2O3


nSO3=0,75(mol)
mH2SO4(bđ)= 600.15%=90(g) => nH2SO4(bđ)= 90/98=45/49(mol)
PTHH: SO3 + H2O -> H2SO4
0,75______0,75____0,75(mol)
=> mH2SO4(tổng)= 0,75.98+90= 163,5(g)
mddH2SO4= mSO3+mddH2SO4(bđ)= 0,75.80 + 600= 660(g)
=>C%ddH2SO4(sau)= (163,5/660).100=24,773%
VddH2SO4(sau)= 660/1,25= 528(ml)=0,528(l)
nH2SO4(tổng)= 45/49 + 0,75= 327/196(mol)
=> CMddH2SO4(sau)= 327/196 : 0,528=3,16(M)


Câu 1
1)
$(1) 4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$(2) 2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3$
$(3) SO_3 + H_2O \to H_2SO_4$
$(4)6FeSO_4 + 3Cl_2 \to 2Fe_2(SO_4)_3 + 2FeCl_3$
$(5) Fe_2(SO_4)_3 + 3BaCl_2 \to 3BaSO_4 + 2FeCl_3$
$(6) FeCl_3 + 3KOH \to Fe(OH)_3 + 3KCl$
$(7) 2Fe(OH)_3 \xrightarrow{t^o} Fe_2O_3 + 3H_2O$
2)
Trích mẫu thử
Cho dung dịch phenolphtalein vào
- mẫu thử hóa hồng là NaOH
Cho ba mẫu thử còn lai tác dụng lần lượt với nhau
- mẫu thử tạo kết tủa trắng là $H_2SO_4,Ba(NO_3)_2$
$Ba(NO_3)_2 + H_2SO_4 \to BaSO_4 + 2HNO_3$
- mẫu thử không hiện tượng là HCl
Cô cạn hai mẫu thử còn :
- mẫu thử thu được chất rắn khan là $Ba(NO_3)_2$
- mẫu thử không thu được chất rắn là $H_2SO_4$


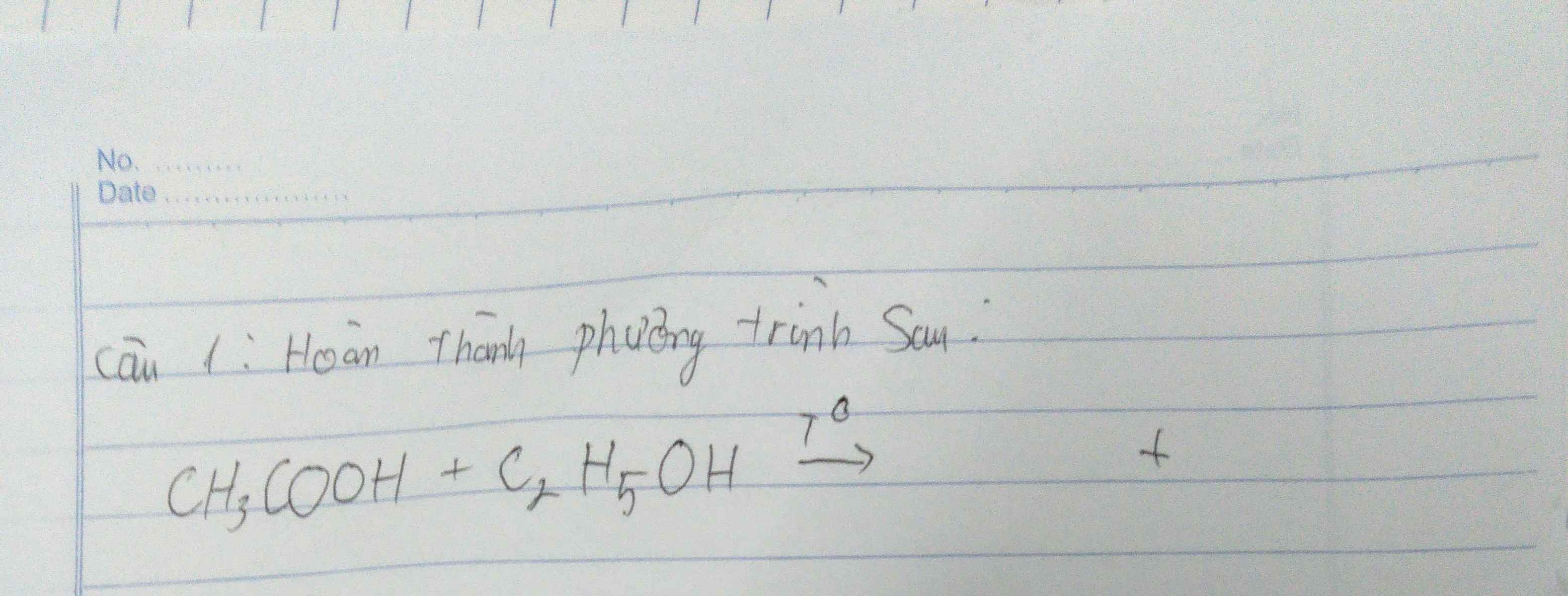




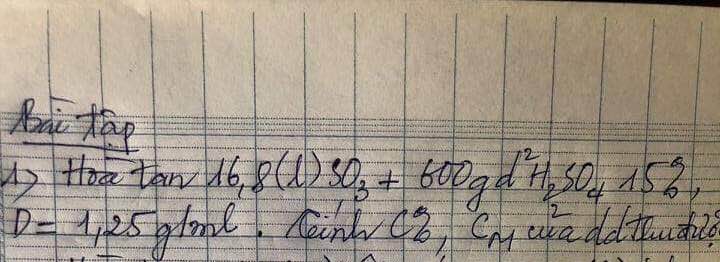
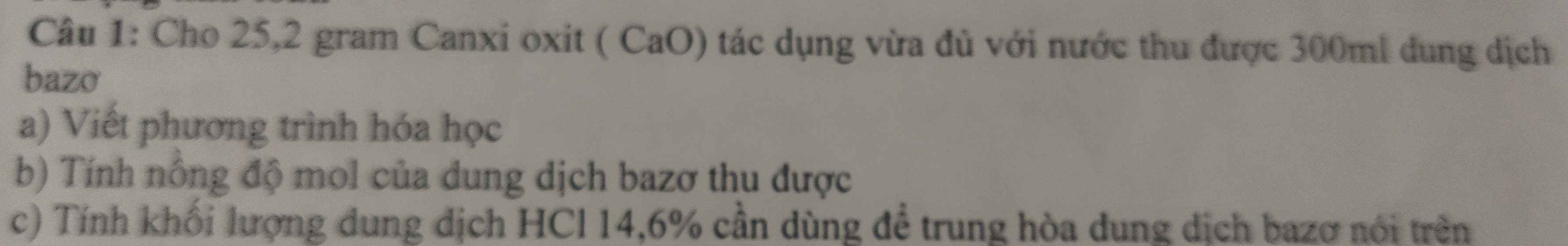

a,
Cho quỳ tím vào các dd:
+ Quỳ tím hóa đỏ: HCl
+ Quỳ tím hóa xanh: NaOH
+ Không hiện tượng: Na2SO4, NaCl (1)
Cho BaCl2 vào (1)
+ Mẫu tạo kết tủa trắng là: Na2SO4
BaCl2 + Na2SO4 \(\rightarrow\) BaSO4 + 2NaCl
+ Không hiện tượng là: NaCl
b, Cho quỳ tím vào các dd:
+ Quỳ tím hóa đỏ: HCl, H2SO4 (1)
+ Không hiện tượng: NaNO3, Na2CO3 (2)
Cho BaCl2 vào (1):
+ Mẫu tạo kết tủa là: H2SO4
BaCl2 + H2SO4 \(\rightarrow\) BaSO4 + 2HCl
+ Không hiện tượng là: HCl
Cho BaCl2 vào (2):
+ Mẫu tạo kết tủa trắng là: Na2CO3
BaCl2 + Na2CO3 \(\rightarrow\) BaCO3 + 2NaCl
+ Không hiện tượng: NaNO3