
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


nNa2SO4= 9,94/142=0,07(mol);
mBa(OH)2= 20,52(g) -> nBa(OH)2=0,12(mol)
PTHH: Na2SO4 + Ba(OH)2 -> BaSO4 + 2 NaOH
Ta cps: 0,07/1 < 0,12/1
=> Ba(OH)2 dư, Na2SO4 hết, tính theo nNa2SO4.
-> nBaSO4=nNa2SO4= 0,07(mol)
=> m(kết tủa)=mBaSO4=0,07.233=16,31(g)
=>m=16,31(g)
b) Dung dịch A thu được bao gồm NaOH và Ba(OH)2 dư.
nNaOH=2.0,07=0,14(mol) => mNaOH= 0,14.40=5,6(g)
nBa(OH)2 (dư)=0,12-0,07=0,05(mol)
=> mBa(OH)2 (dư)= 0,05.171=8,55(g)
=> mddA=Na2SO4 + mddBa(OH)2 - mBaSO4 = 9,94+ 100 - 16,31= 93,63(g)
=> C%ddBa(OH)2 (dư)= (8,55/93,63).100=9,132%
C%ddNaOH= (5,6/93,63).100=5,981%

d) Gọi x,y lần lượt là số mol Al, Fe
\(\left\{{}\begin{matrix}27x+56y=8,3\\1,5x+y=0,25\end{matrix}\right.\)
=> x=0,1 ; y=0,1
Kết tủa : Al(OH)3, Fe(OH)2
Bảo toàn nguyên tố Al: \(n_{Al\left(OH\right)_3}=n_{Al}=0,1\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{Fe\left(OH\right)_2}=n_{Fe}=0,1\left(mol\right)\)
=> \(m=0,1.78+0,1.90=16,8\left(g\right)\)
Nung kết tủa thu được chất rắn : Al2O3 và FeO
Bảo toàn nguyên tố Al: \(n_{Al_2O_3}.2=n_{Al}\Rightarrow n_{Al_2O_3}=0,05\left(mol\right)\)
Bảo toàn nguyên tố Fe: \(n_{FeO}=n_{Fe}=0,1\left(mol\right)\)
=> \(a=0,05.102+0,1.72=12,3\left(g\right)\)

PTHH: Al2O3+6HCl➝2AlCl3+3H2O(1)
a)nAl2O3=\(\dfrac{10,2}{102}\)=0,1(mol)
mHCl=\(\dfrac{5\%.219}{100\%}\)=10,95(g)
⇒nHCl=\(\dfrac{10,95}{36,5}\)=0,3(mol)
Xét tỉ lệ Al2O3:\(\dfrac{0,1}{1}\)=0,1
Xét tỉ lệ HCl:\(\dfrac{0,3}{6}\)=0,05
⇒HCl pứng hết,Al2O3 còn dư
Theo PTHH(1) ta có nAl2O3 pứng=\(\dfrac{nHCl}{6}\)=\(\dfrac{0,3}{6}\)=0,05(mol)
⇒nAl2O3 dư=nAl2O3ban đầu-nAl2O3 pứng=0,1-0,05=0,05(mol)
⇒mAl2O3 dư=0,05.102=5,1(g)
b) C%HCl=\(\dfrac{0,3.36,5}{219+10,2}\).100%=4,8%
nAlCl3=0,1(mol)
⇒C%AlCl3=\(\dfrac{0,1.136,5}{10,2+219}\).100%=6%


1.
\(n_{KNO_3}=0.15\cdot0.1=0.015\left(mol\right)\)
\(m_{KNO_3}=0.015\cdot101=1.515\left(g\right)\)
2.
\(m_{KOH}=200\cdot20\%=40\left(g\right)\)
Sau khi pha :
\(m_{dd_{KOH}}=\dfrac{40}{16\%}=250\left(g\right)\)
\(m_{H_2O\left(tv\right)}=250-200=50\left(g\right)\)
3.
\(n_{NaOH}=2\cdot1=2\left(mol\right)\)
Sau khi pha :
\(V_{dd_{NaOH}}=\dfrac{2}{0.1}=20\left(l\right)\)
\(V_{H_2o\left(tv\right)}=20-2=18\left(l\right)\)
3)
$n_{KNO_3} = 0,15.0,1 = 0,015(mol)$
$m_{KNO_3} = 0,015.101 = 1,515(gam)$
4)
$m_{KOH} = 200.20\% = 40(gam)$
$m_{dd\ KOH\ 16\%} = \dfrac{40}{16\%} = 250(gam)$
$\Rightarrow m_{H_2O} = 250 -200= 50(gam)$
5)
$n_{NaOH} = 2.1 = 2(mol)$
$V_{dd\ NaOH} = \dfrac{2}{0,1} = 20(lít)$
$\Rightarrow V_{H_2O} = 20 - 2 = 18(lít)$
4)






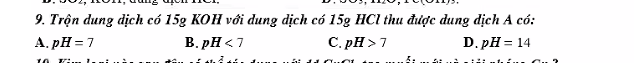

 giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ
giúp mình với ạ , mình đang cần gấp ạ, các bạn làm theo cách kẻ bảng ra giúp mình được không ạ





