Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Mg}=\dfrac{8,4}{24}=0,35\left(mol\right)\)
PTHH:
\(2Mg+O_2\xrightarrow[]{t^o}2MgO\\
MgO+2HCl\rightarrow MgCl_2+H_2O\\
Mg+2HCl\rightarrow MgCl_2+H_2\)
ĐLBTKL: \(m_{O_2}=m_X-m_{Mg}=10-8,4=1,6\left(g\right)\)
\(\Rightarrow n_{O_2}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
Quá trình oxi hóa - khử:
\(\overset{0}{Mg}\rightarrow\overset{+2}{Mg}+2e\)
\(\overset{0}{O_2}+4e\rightarrow2\overset{-2}{O}\)
\(2\overset{+1}{H}+2e\rightarrow H_2\)
\(\xrightarrow[]{BTelectron}2n_{Mg}=4n_{O_2}+2n_{H_2}\)
\(\Rightarrow n_{H_2}=\dfrac{0,35.2-0,05.4}{2}=0,25\left(mol\right)\)
`=> V = 0,25.22,4 = 5,6 (l)`

PTHH: Fe + 2HCl --> FeCl2 + H2
FeS + 2HCl --> FeCl2 + H2S
=> \(n_{Fe}+n_{FeS}=n_{H_2}+n_{H_2S}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
Và 56.nFe + 88.nFeS = 18,8
=> \(\left\{{}\begin{matrix}n_{Fe}=0,1\left(mol\right)\\n_{FeS}=0,15\left(mol\right)\end{matrix}\right.\)
Bảo toàn S: nCaSO3 = 0,15 (mol)
=> m = 0,15.120 = 18 (g)
=> B

Đáp án B
Khí thi được là
![]()
Cu là kim loại đứng sau hiđro trong dãy hoạt động hóa học, do đó Cu không tác dụng với dung dịch H 2 SO 4 loãng => Chất rắn không tan là Cu
Sơ đồ phản ứng:

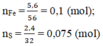
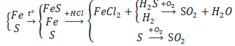

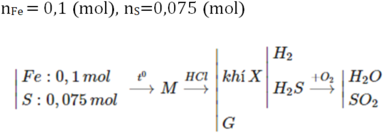




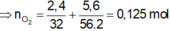
Ta có: \(n_{Al}=\dfrac{3,24}{27}=0,12\left(mol\right)\)
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
Theo ĐLBT e, có: 3nAl = 2nCl2 + 2nH2
⇒ nCl2 = 0,03 (mol)
Ta có: m = mAl + mCl2 = 5,37 (g)