Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
HCl → H++ Cl-
[H+] = a M ; suy pH = -log a = x
![]()
Cứ 100 phân tử CH3COOH thì có 1 phân tử điện li nên [H+] = a/100 M suy ra pH = -log (a/100) = y
Do đó y-x = 2

Dung dịch axit ban đầu có [H+] = 0,1 M
⇒ nH+= 0,1.0,1 = 0,01 mol
Dung dịch sau phản ứng có pH = 12
⇒ dư bazơ và có pOH =14 – 12 = 2
⇒ [OH-] = 0,01M
⇒ nOH− dư = 0,002 mol
Phản ứng trung hòa:
nH+phản ứng = nOH−phản ứng = 0,01 mol
⇒ nNaOH ban đầu = nOH−phản ứng + nOH− dư
= 0,01 + 0,002 = 0,012 mol
⇒ a = 0,12M

Đáp án A
pH = 11 => OH- dư sau phản ứng => pOH =3
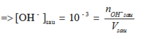
=> nOH- sau = Vsau . [OH-] = 10-3. 0,6= 0,0006 = 6.10-4 (mol)
pH = 2 => [H+]= 10-2 = 0,01M => nH+= 0,3 . 0,01= 0,003
nOH- = 0,3.a
H+ + OH- → H2O
Ban đầu: 0,003 0,3.a
Phản ứng: 0,003 0,003
Sau: 0 0,3.a-0,003
nOH- sau= 6.10-4 = 0,3a -0,003 => a=0,012M

Đáp án D
Dd axit ban đầu có [H+] =0,1 M → nH+=0,1.0,1 =0,01 mol
Dd sau phản ứng có pH = 12 → dư bazo và có pOH =14-12=2 → [OH-] =0,01M→ nOH = 0,002 mol
PTHH: H+ + OH- → H2O
Ta có nNaOH = nH+ + nOH dư = 0,01 + 0,002 = 0,012 mol → a = 0,12M

Không mất tính tổng quát, ta đặt:
![]()
Vì HCl là chất điện li mạnh nên ta có phương trình điện li như sau:
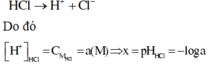
Vì CH3COOH là chất điện li yếu nên ta có phương trình điện li như sau
Xét cân bằng điện li: CH3COOH ⇌ CH3COO- + H+
Nồng độ ban đầu: aM 0
Nồng độ phân li: 0,01a M → 0,01a M
Nồng độ cân bằng: 0,99a M 0,01a M
Ta có
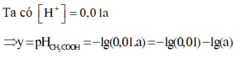
![]()
Đáp án A.

Đáp án B
► Dung dịch thu được không pứ với AgNO₃ ⇒ dung dịch thu được không còn Cl⁻
Ở đây ta cần chú ý, với H⁺ bị điện phân tại catot và anot bị điện phân H₂O
thì: 2H⁺ + 2e → H₂ || 2H₂O → 4H⁺ + O₂ + 4e ⇒ cộng lại cho khử e thì:
2H₂O → 2H₂ + O₂ ⇒ xem như điện phân H₂O ⇒ pH không đổi
Mà ta thấy sau t(s) đầu tới t(s) sau thì pH bị thay đổi
⇒ H₂O và H⁺ không bị điện phân cùng lúc ngay t(s) đầu
► Mặt khác, phần xem như điện phân H₂O không cần quan tâm vì không có gì đặc biệt
⇒ xét phần còn lại, thấy nH⁺ giảm = nH⁺ bị điện phân = 0,1 – 0,01 = 0,09 mol
nH⁺ sau khi điện phân t(s) = 0,1 mol = nHCl ban đầu ⇒ nCl⁻ = 0,1 mol
BTe: nCu = (0,1 – 0,09) = 0,005 mol

ta có : 0,01>4,47.10-7=>[H+]=0,01=> pH = -log(H+)
=> pH = -log(0,01) = 2
:)

Đáp án D
nH+ = 0,1.0,1= 0,01
Trong dụng dịch sau phản ứng có nOH- = 0,01 .0,2=0,002
⇒ nOH- ban đầu = n H+ + n OH-dư = 0,01+0,002=0,012
⇒ a = 0,012 ÷ 0,1 =0,12
Đáp án D.
\(\alpha=\dfrac{C}{C_0}\Rightarrow C=0.002\cdot1.2\%=2.4\cdot10^{-5}\left(M\right)\)
\(CH_3COOH⇌H^++CH_3COO^-\)
\(0.002..................0..................0\left(BĐ\right)\)
\(2.4\cdot10^{-5}.....2.4\cdot10^{-5}...2.4\cdot10^{-5}\left(PL\right)\)
\(1.976\cdot10^{-3}....2.4\cdot10^{-5}...2.4\cdot10^{-5}\left(CB\right)\)
\(pH=-log\left[H^+\right]=-log\left(2.4\cdot10^{-5}\right)=4.6\)
Em xem đáp án thử nha.