Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1) \(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
mA = mKMnO4(bđ) - mO2 = 79 - 0,15.32 = 74,2 (g)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
0,3<-----------0,15<----0,15<---0,15
=> \(H=\dfrac{0,3.158}{79}.100\%=60\%\)
2)
\(\left\{{}\begin{matrix}\%m_{K_2MnO_4}=\dfrac{0,15.197}{74,2}.100\%=39,825\%\\\%m_{MnO_2}=\dfrac{0,15.87}{74,2}.100\%=17,588\%\\\%m_{KMnO_4\left(không.pư\right)}=\dfrac{79-0,3.158}{74,2}.100\%=42,587\%\end{matrix}\right.\)
3) \(n_{KMnO_4\left(không.pư\right)}=\dfrac{79}{158}-0,3=0,2\left(mol\right)\)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,2----------------------------------->0,5
K2MnO4 + 8HCl --> 2KCl + MnCl2 + 2Cl2 + 4H2O
0,15-------------------------------->0,3
MnO2 + 4Hcl --> MnCl2 + Cl2 + 2H2O
0,15------------------->0,15
=> \(V_{Cl_2}=22,4\left(0,5+0,3+0,15\right)=21,28\left(l\right)\)
\(n_{KMnO_4}=\dfrac{79}{158}=0,5mol\)
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15mol\)
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\)
0,5 0,15
a)\(m_{KMnO_4}=0,15\cdot197=29,55g\)
\(m_{MnO_2}=0,15\cdot87=13,05g\)
\(m_{CRắn}=m_{KMnO_4}+m_{MnO_2}=29,55+13,05=42,6g\)
\(n_{KMnO_4pư}=0,15\cdot2=0,3mol\)
\(H=\dfrac{0,3}{0,5}\cdot100\%=60\%\)
b)\(m_{O_2}=0,15\cdot32=4,8g\)
\(\%m_{K_2MnO_4}=\dfrac{29,55}{42,6}\cdot100\%=69,37\%\)
\(\%m_{MnO_2}=100\%-69,37\%=30,63\%\)

Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)

c2
a/ 2KMnO4(x)to→K2MnO4(0,5x)+MnO2(0,5x)+O2(0,5x)
Gọi số mol của KMnO4 tham gia phản ứng là x.
⇒mKMnO4=158x(g)
⇒mK2MnO4=0,5x.197=98,5x(g)
⇒mMnO2=0,5x.87=43,5x(g)
⇒22,12−158x+98,5x+43,5x=21,26
⇔x=0,05375(mol)
⇒VO2=0,05375.0,5.22,4=0,602(l)
b/ mKMnO4(pứ)=0,05375.158=8,4925(g)
⇒%KMnO4=8,4925\22,12.100%=38,39%

a) $n_{O_2} = 0,15(mol)$
\(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
0,3 0,15 0,15 0,15 (mol)
$H = \dfrac{0,15.158}{63,2}.100\% = 37,5\%$
b)
$m_B = 63,2 - 0,15.32 = 58,4(gam)$
$\%m_{K_2MnO_4} = \dfrac{0,15.197}{58,4}.100\% = 50,59\%$
$\%m_{MnO_2} = \dfrac{0,15.87}{58,4}.100\% = 22,35\%$
$\%m_{KMnO_4\ dư} = 100\% -50,59\% -22,35\% = 27,06\%$

a, \(m_A=8+1,02=9,02\)
\(m_{giam}=m_O=9,02-7,74=1,28\left(g\right)\)
\(\rightarrow n_O=n_{H2\left(pu\right)}=0,08\left(mol\right)\)
\(n_{H2}=0,02\left(mol\right)\)
\(\rightarrow H=\frac{0,08.100}{0,2}=40\%\)
b, \(n_{CuO}=0,1\left(mol\right)\)
\(n_{F2eO3}=0,006\left(mol\right)\)
Gọi a là số mol của CuO (pu) , b là số mol Fe2O3 (pu)
\(\rightarrow\frac{a}{b}=\frac{0,1}{0,006}=\frac{50}{3}\Leftrightarrow3a-50b=0\left(1\right)\)
\(n_{H2\left(pu\right)}=n_{O\left(bi.khu\right)}=0,08\left(mol\right)\)
\(\rightarrow a+3b=0,08\)
Từ (1) và (2) \(\rightarrow\left\{{}\begin{matrix}a=0,068\\b=0,004\end{matrix}\right.\)
\(\rightarrow n_{Cu}=0,068,n_{Fe}=0,008\)
\(n_{CuO_{du}}=0,032\left(mol\right)\)
\(n_{Fe2O3_{du}}=0,002\left(mol\right)\)
\(\rightarrow m_{Cu}=4,352\left(g\right),m_{Fe}=0,448\left(g\right)\)
\(m_{Fe2O3_{du}}=0,32\left(g\right),m_{CuO_{du}}=2,56\left(g\right)\)
Mình thấy nó hơi sai sai ấy. Bài này cô mình chữa rồi nên bạn có cần gửi bài cô mình chữa để so sánh ko ạ

2KMnO4-to>K2MnO4+MnO2+O2
0,14-------------0,07------0,07-------0,07 mol
n KMnO4=\(\dfrac{22,12}{158}\)=0,14 mol
=>a=mcr=0,07.197+0,07.87=23,82g
=>VO2=0,07.22,4=1,568l
b)
2Cu+O2-to>2CuO
0,07-----0,14
n Cu=\(\dfrac{10,24}{64}\)=0,16 mol
Cu dư :0,01 mol
m chất rắn =0,01.64+0,14.80=11,84g
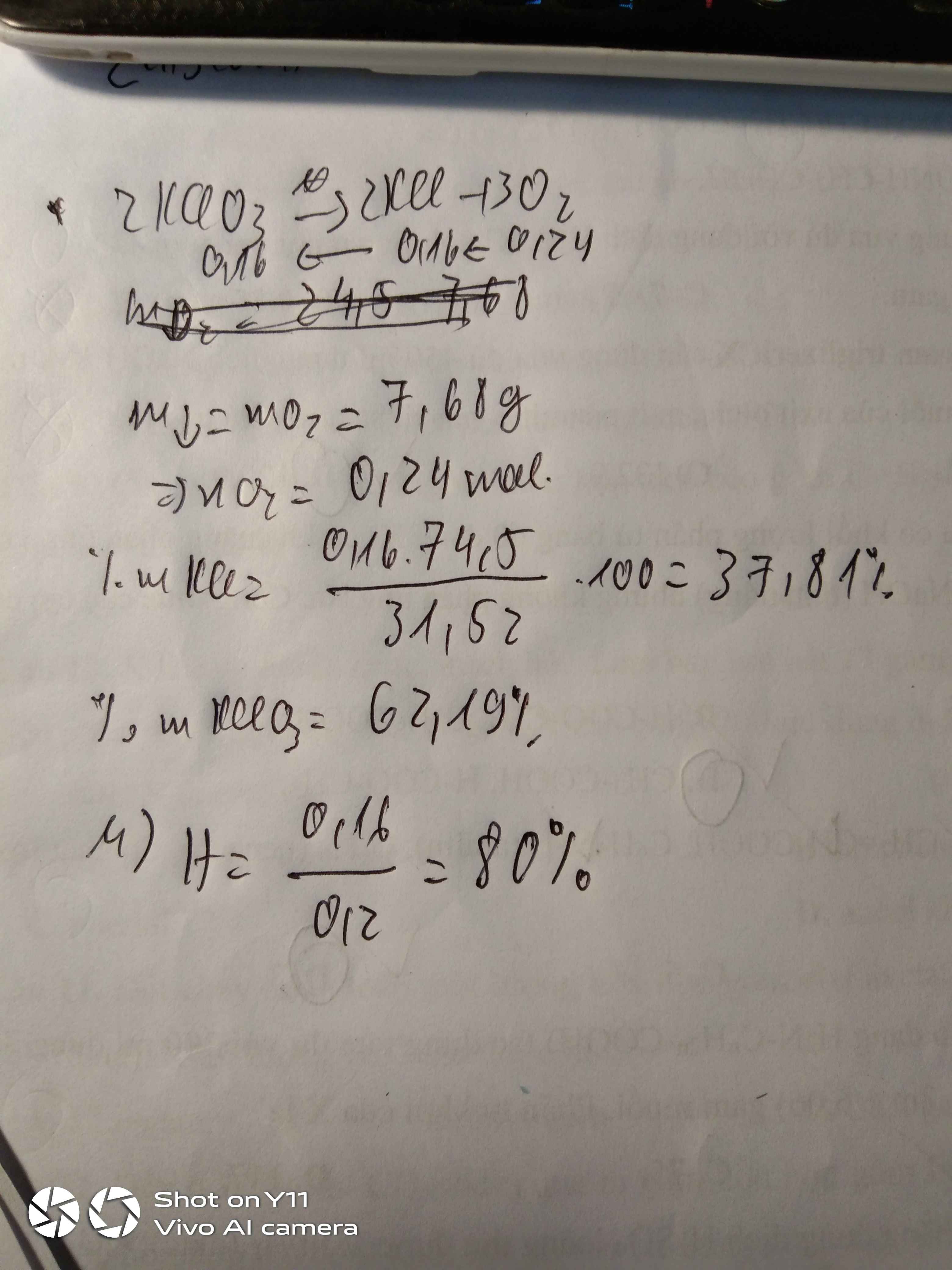
\(2KMnO_4\rightarrow K_2MnO_4+MnO_2+O_2\)
Áp dụng ĐLBT khối lượng:
\(m_{O2\left(thu.duoc\right)}=23,7-22,26=1,44\left(g\right)\)
\(\Rightarrow n_{O2}=\frac{1,44}{32}=0,045\left(mol\right)\)
Theo PTHH,
\(\Rightarrow n_{KMnO4\left(np\right)}=2.0,045=0,09\left(mol\right)\)
\(m_{KMnO4\left(np\right)}=0,09.158=14,22\left(g\right)< 23,7\left(g\right)\)
\(\Rightarrow\) KMnO4 bị nhiệt phân không hoàn toàn
\(m_{KMnO4\left(dư\right)}=23,7-14,22=9,48\left(g\right)\)
\(\Rightarrow n_{K2MnO4}=0,045\left(mol\right)\)
\(\Rightarrow m_{K2MnO4}=0,045.197=8,865\left(g\right)\)
Trong hh X gồm: KMnO4 dư; K2MnO4;MnO2
\(\%_{KMnO4}=\frac{9,48}{22,26}.100\%=42,58\%\)
\(\%_{K2MnO4}=\frac{8,865}{22,26}.100\%=39,83\%\)
\(\%_{MnO2}=100\%-42,58\%-39,83\%=17,59\%\)
\(\Rightarrow H=\frac{14,22}{23,7}.100\%=60\%\)