Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a)
n O = 6,13.23,491%/16 = 0,09(mol)
=> n Al2O3 = 1/3 n O = 0,03(mol)
n H2 = 1,456/22,4 = 0,065(mol)
$H_2O \to OH^- + \dfrac{1}{2}H_2$
Suy ra: n OH = 2n H2 = 0,065.2 = 0,13(mol)
Al2O3 + 2OH- → 2AlO2- + H2O
0,03......0,06..........0,06.....................(mol)
DUng dịch G có :
AlO2- : 0,06
OH- : 0,13 - 0,06 = 0,07(mol)
Áp dụng CT :
n H+ = 4n AlO2- + n OH- - 3n Al(OH)3
<=> 0,16 = 0,06.4 + 0,07 - 3n Al(OH)3
<=> n Al(OH)3 = 0,05(mol)
<=> m = 0,05.78 = 3,9(gam)
Trong F :
m Na + m K + m Ba = m D - m Al2O3 = 6,13 - 0,03.102 = 3,07(gam)
n Cl = n HCl = 0,16(mol)
n Al3+ = 0,06 - 0,05 = 0,01(mol)
=> m chất tan = 3,07 + 0,16.35,5 + 0,01.27 = 9,02(gam)

PTHH: \(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
Ta có: \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(\Rightarrow n_{Al}=0,2\left(mol\right)\) \(\Rightarrow m_{Al}=0,2\cdot27=5,4\left(g\right)\)

\(2R+2nHCl\rightarrow2RCl_n+nH_2\)
.0,12/n...............0,12/n......0,06......
\(R_2O_n+2nHCl\rightarrow2RCl_n+nH_2O\)
.0,3/n......................................0,3....
\(n_{H_2O}=2n_{O_2}=0,3\left(mol\right)\)
Có : \(m=13,44=m_R+m_{R_2O_n}=\dfrac{0,12R}{n}+\dfrac{\left(2R+16n\right)0,3}{n}\)
\(\Rightarrow R=12n\)
=> R là Mg
\(n_{Al\left(I\right)}=\dfrac{3}{2}n_{H_2}=0,045\left(mol\right)\)
\(n_{Al\left(II\right)}=2n_{Al_2O_3}=\dfrac{2}{3}n_{H_2O}=\dfrac{2}{3}.2n_{O_2}=\dfrac{4}{3}n_{O_2}=\dfrac{1}{15}\left(mol\right)\)
\(\Rightarrow m_{Al}=m=3,015\left(g\right)\)

$a)PTHH:2Al+6HCl\to 2AlCl_3+3H_2$
$n_{H_2}=\dfrac{5,04}{22,4}=0,225(mol)$
$\Rightarrow n_{Al}=0,15(mol)$
$\Rightarrow \%m_{Al}=\dfrac{0,15.27}{9,45}.100\%\approx 42,86\%$
$\Rightarrow \%m_{Cu}=100-42,86=57,14\%$
$b)$ Theo PT: $n_{HCl}=2n_{H_2}=0,45(mol)$
$\Rightarrow C_{M_{HCl}}=\dfrac{0,45.110\%}{0,5}=0,99M$

Vì các phản ứng hoàn toàn mà khi cho Y + NaOH ----> H2 chứng tỏ Al dư, Fe2O3 chuyển hết thành Fe. Vậy trong Y có chứa Al: 0,03 mol ( nH2 = 3/2nAl); nFe = 0,06 mol (mFe = m rắn = 3,36 g)
Từ pư: 2Al + Fe2O3 ---> Al2O3 + 2Fe => nFe2O3 = nAl2O3, mà nFe2O3 = nFe/2 => nAl2O3 = 0,03 mol
m phần 1 = 7,23 g => m phần 2 = 21,69 g. Hay p2 = 3 p1
=> Trong phần 2 có: Al: 0,09 mol; Fe: 0,18 mol; Al2O3: 0,09 mol
Bảo toàn e (giả sử chỉ tạo Fe2+, vì ta chưa biết sản phẩm có Fe3+ hay không): 3nNO < 3nAl + 2nFe => có NH4+
Gọi số mol Fe2+: x, Fe3+: y, NH4+: z
=> Bảo toàn electron: 0,09.3 + 2x + 3y = 0,17.3 + 8z
x + y = 0,18 (bảo toàn Fe)
1,52 = 0,09.3.2 ( nH+ phản ứng với Al2O3) + 0,17.4 + 10z
=> x = 0,06; y = 0,12; z = 0,03
Bảo toàn N: nNO3- = nHNO3 - nNO - nNH4+ = 1,32 mol
=> m = 21,69 + NO3- = 103,53 g

Đặt nZn = x mol; nFe = y mol.
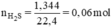
Ta có hệ phương trình: 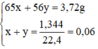
Giải hệ phương trình trên ta được:
x = 0,04 mol, y = 0,02 mol.
mZn = 65 × 0,04 = 2,6g
mFe = 56 × 0,02 = 1,12g

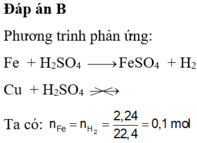
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
0,4 0,3 0,2 ( mol )
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\)
\(Al_2O_3+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2O\) ( không giải phóng H2)
=> Chất rắn tạo ra H2 là Al
\(2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\)
0,2 0,3 ( mol )
\(\Rightarrow m_{Al}=\left(0,2.27\right)+\left(0,4.27\right)=16,2g\)