Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Ta có: \(n_{Ca}=\dfrac{6}{40}=0,15\left(mol\right)\)
PT: \(2Ca+O_2\underrightarrow{t^o}2CaO\)
\(n_{CaO}=n_{Ca}=0,15\left(mol\right)\Rightarrow m_{CaO}=0,15.56=8,4\left(g\right)\)
\(2Ca+O_2\rightarrow\left(t^o\right)2CaO\\ n_{Ca}=\dfrac{6}{40}=0,15\left(mol\right)\\ n_{CaO}=n_{Ca}=0,15\left(mol\right)\\ m_{CaO}=0,15.56=8,4\left(g\right)\)

Chọn B.
Khi cho 0,06 mol M tác dụng với NaOH thì: 
Hỗn hợp ancol G gồm Y (0,04 mol) và Z (0,06 mol) Þ số nguyên tử C trong G là 3.
Vì MY > MZ nên Y là CH2=CH-CH2OH và Z là CH≡C-CH2OH.
Xét a gam M có 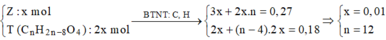
Vậy T là C12H16O4 (0,02 mol) có %mT = 88,89%.

Chọn đáp án B
♦ đốt a mol T + O2
b mol CO2 + c mol H2O.
có b – c = 4a ⇔ ∑nCO2 – ∑nH2O = (5 – 1).nT ⇒ T có 5π.
T sẵn có 3πC=O trong 3 chức este ⇒ còn 2πC=C trong gốc hiđrocacbon nữa.
||⇒ phản ứng hiđro hóa xảy ra như sau: T + 2H2 → G ||⇒ nG = ½.nH2 = 0,03 mol.
||⇒ 25,86 gam G (0,03 mol) + 0,12 mol NaOH → m gam c.rắn + 0,03 mol C3H5(OH)3.
||⇒ BTKL có m = 25,86 + 0,12 × 40 – 0,03 × 92 = 27,90 gam

Giải thích: Đáp án C
Bảo toàn khối lượng m↑ = 23-7,2 =15,8 g
→ hỗn hợp khí có Cl2 : 0,2 mol và O2 :0,05 mol
Đặt hóa trị của M là x
Bảo toàn e có 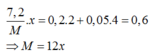
→x=2 và M =24 (Mg)

nCO2 = nH2O = 0.3 mol => este no đơn
Gọi este X: CnH2nO2
\(nX=\dfrac{nCO2}{n}=\dfrac{0.3}{n}\)
=> \(\dfrac{0.3}{n}\times\left(12n+2n+32\right)=7.4\Leftrightarrow n=3\)
=> X là C3H6O2
Mà X tham gia phản ứng tráng gương nên có gốc HCOO-R
=> X là HCOOC2H5 (không có đáp án)

2CH3COOC2H3 + 9O2 \(-^{t^o}\rightarrow\)8CO2 + 6H2O
\(n_{CH_3COOC_2H_3}=0,125\left(mol\right)\)
Theo PT : \(n_{CO_2}=4n_{CH_3COOC_2H_3}=0,5\left(mol\right)\)
CO2 + Ca(OH)2 ----------> CaCO3 + H2O
\(n_{CaCO_3}=n_{CO_2}=0,5\left(mol\right)\)
=> \(m_{CaCO_3}=0,5.100=50\left(g\right)\)

Đáp án D
Định hướng tư duy giải
Chú ý: Mỗi thằng có 2π và 2O
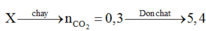

![]()
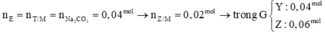

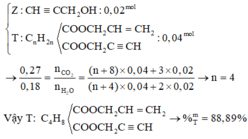
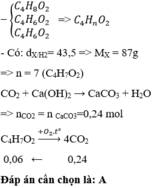
\(n_{CH_3COOC_2H_5}=\dfrac{8,8}{88}=0,1\left(mol\right)\)
BTNT C: \(n_{CO_2}=4n_{CH_3COOC_2H_5}=0,4\left(mol\right)\)
BTNT H: \(n_{H_2O}=4n_{CH_3COOC_2H_5}=0,4\left(mol\right)\)
`=> m = m_{CO_2} + m_{H_2O} = 0,4.44 + 0,4.18 = 24,8 (g)`