Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Số nguyên tử Cacbon trung bình = \(\dfrac{V_{CO_2}}{V_{hh}} = \dfrac{11,2}{4,48} = 2,5\)
Suy ra : Hai anken là \(C_2H_4(x\ lít)\ ; C_3H_6(y\ lít)\)
Bảo toàn nguyên tố với C :
\(V_{CO_2} = 2x + 3y = 11,2(1)\)
\(V_{hỗn\ hợp} = x + y = 4,48(2)\\ (1)(2) \Rightarrow x = 2,24 ; y = 2,24\\ \Rightarrow \%V_{C_2H_4}=\%V_{C_3H_6} = \dfrac{2,24}{4,48}.100\% = 50\%\)

Đáp án D
CnH2n + 1,5nO2 → nCO2 + nH2O
3 10,5
=> n = 7/3 => C2H4 và C3H6
Lấy nX = 3 => nC2H4 = 2 và nC3H6 = 1
=> Y gồm C2H5OH (2 mol); CH3-CH2-CH2OH (a mol) và CH3-CHOH-CH3 (b mol)
=> a + b = 1
60b = 6(2.46+ 60a)/13
=> a = 0,2 và b = 0,8
=> %CH3-CH2-CH2OH = 7,89%

Giả sử trong 18,9 g hỗn hợp X có x mol ancol etylic và y mol hai ankan (công thức chung C n H 2 n + 2 ).
46x + (14 n + 2)y = 18,90 (1)
C 2 H 5 O H + 3 O 2 → 2 C O 2 + 3 H 2 O
x mol 2x mol 3x mol
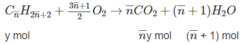
Số mol
C
O
2
= 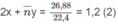
Số mol
H
2
O
= 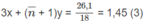
Giải hệ phương trình (1), (2), (3) tìm được x = 0,1 ; y = 0,15 ; n = 6,6
Công thức của hai ankan là C 6 H 14 và C 7 H 16 .
Đặt lượng C 6 H 14 là a mol, lượng C 7 H 16 là b mol :
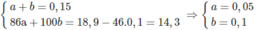
% về khối lương của
C
6
H
14
: 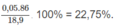
% về khối lượng của
C
7
H
16
: 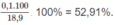

Đốt cháy hỗn hợp X gồm 2 anken ⇒ nCO2 = nH2O
mCO2 – mH2O = 6,76
⇒ nCO2 = nH2O = 6,76 : (44 – 18) = 0,26
Gọi công thức chung của 2 chất là CnH2n ( n>2)
⇒ n = 0,26 : 0,1 = 2,6
Mà 2 anken đồng đẳng kế tiếp ⇒ 2 anken đó là : C2H4 và C3H6
Đáp án A.

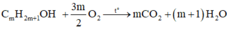
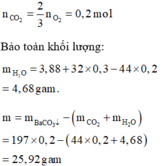

Bạn tham khảo nhé! Đây là bài mik từng làm.