Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

1. Đề phải là tính V và lập cthh của oxit kim loại chứ
Không hiểu sao làm xong bài bạn mình thấy mình lên voi xuống chó ghê :)) Hơi dài, mà không biết đúng không
---------------------------------
Gọi ct oxit cần tìm là AcOd
Gọi x, y lần lượt là số mol của CuO, AcOd
Dẫn CO đi qua hỗn hợp gồm 2 oxit là CuO và AcOd
PTHH:
\(CO+CuO\underrightarrow{t^o}Cu+CO_2\) (1)
x <----- x ------> x ----> x
\(A_cO_d+dCO\underrightarrow{t^o}cA+dCO_2\) (2)
y -----> yd -----> cy ---> yd
sau phản ứng thu được : Kim loại X gồm: Cu, A
Hỗn hợp khí Y: CO dư, CO2
Theo đề ra: \(80x+y\left(cA+16d\right)=31,2\)(I)
\(64x+Acy=23,2\) (II)
Lấy (I) trừ (II) ta được: \(16x+16yd=8\) \(\Leftrightarrow x+yd=0,5\) (III)
Đặt số mol của CO dư spu là a (mol)
Theo gt: \(\dfrac{M_Y}{H_2}=20,667\)
\(\Rightarrow M_Y=41,334=\dfrac{28a+44.0,5}{a+0,5}\)
\(\Rightarrow a=0,1\)
\(n_{CO}=0,5+0,1=0,6\left(mol\right)\) \(\Rightarrow V_{CO}=0,6.22,4=13,44\left(l\right)\)
Cho X vào dd HCl dư, thấy khí thoát ra => \(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Vì Cu đứng sau hidro trong dãy hoạt động hóa học nên chỉ có A phản ứng .
Đặt hóa trị của A \(\dfrac{2d}{c}=n\) \(;1\le n\le3\)
PTHH: \(A+nHCl\rightarrow ACl_n+\dfrac{1}{2}nH_2\) (3)
\(\dfrac{0,6}{n}\)<------------------------------0,3 mol
Từ (2) và (3) ta có:\(cy=\dfrac{0,6}{\dfrac{2d}{c}}\)\(\Leftrightarrow\) \(cy=\dfrac{0,3c}{d}\) \(\Leftrightarrow y=\dfrac{0,3}{d}\)\(\Leftrightarrow yd=0,3\) (IV)
Từ (III) và (IV) => x = 0,2 (mol )
Ta có: \(64x+\dfrac{0,6}{n}A=23,2\)
\(\Leftrightarrow A=\dfrac{52}{3}n\)
| n | 1 | 2 | 3 |
| A | 52/3 | 104/3 | 52 |
loại loại nhận
\(\Rightarrow A\) là crom.
\(\Rightarrow\dfrac{2d}{c}=3\)\(\Leftrightarrow\dfrac{d}{c}=\dfrac{3}{2}\)
Vậy ct của oxit là Cr2O3

Cho hỗn hợp X vào H2SO4 thu được (a+b)g --> hh X gồm oxit kim loại A và kim loại B
Trong đó: oxit kim loại A ko bị khử bởi CO, kim loại B ko tan trong d.d H2SO4
-->Dễ suy ra kim loại B là Cu
(*)Giả sử oxit kim loại A là AO
AO+H2SO4-->ASO4+H2O
1..........1..........1 mol
m d.d sau pư=A+16+980=A+996 g
C% ASO4=11,765%
\(\Rightarrow\frac{A+96}{A+996}=0,11765\)
\(\Rightarrow A=24\left(Mg\right)\)
(*) Giả sử là A2O3 làm tương tự -->loại
Nếu ko chia trường hợp thì gọi là A2Ox hoặc AxOy

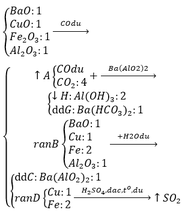
a, - Hh khí X gồm: CO2 và CO dư.
BTNT C, có: \(n_{CO_2}+n_{CO\left(dư\right)}=\dfrac{20,16}{22,4}=0,9\left(mol\right)\left(1\right)\)
Mà: dX/H2 = 58/3 \(\Rightarrow\dfrac{44n_{CO_2}+28n_{CO\left(dư\right)}}{n_{CO_2}+n_{CO\left(dư\right)}}=\dfrac{58}{3}.2\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}n_{CO_2}=0,6\left(mol\right)\\n_{CO\left(dư\right)}=0,3\left(mol\right)\end{matrix}\right.\)
Bản chất pư: \(CO+O\rightarrow CO_2\)
⇒ nO (trong oxit) = nCO2 = 0,6 (mol)
- \(n_{H_2}=\dfrac{10,08}{22,4}=0,45\left(mol\right)\)
Giả sử M có hóa trị n.
PT: \(2M+2nHCl\rightarrow2MCl_n+nH_2\)
Theo PT: \(n_M=\dfrac{2}{n}n_{H_2}=\dfrac{0,9}{n}\left(mol\right)\)
\(\Rightarrow M_M=\dfrac{25,2}{\dfrac{0,9}{n}}=28n\left(g/mol\right)\)
Với n = 2 thì MM = 56 (g/mol)
→ M là Fe. ⇒ nM = 0,45 (mol)
Gọi CTHH của oxit là FexOy
⇒ x:y = 0,45:0,6 = 3:4
Vậy: CTHH cần tìm là Fe3O4.
b, BTNT C, có: nCaCO3 = nCO2 = 0,6 (mol)
⇒ mCaCO3 = 0,6.100 = 60 (g)

1.
Zn + 2HCl \(\rightarrow\)ZnCl2 + H2 (1)
Fe + 2HCl \(\rightarrow\)FeCl2 + H2 (2)
nH2=\(\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Vì Cu không tan trong axit bình thường nên chất rắn là Cu
mCu=3(g)
Đặt nZn=a
nFe=b
Ta có:
\(\left\{{}\begin{matrix}65a+56b=18,6\\a+b=0,3\end{matrix}\right.\)
=>a=0,2;b=0,1
mZn=65.0,2=13(g)
mFe=56.0,1=5,6(g)
2.
Gọi CTHH của oxit là MO
MO + 2HCl \(\rightarrow\)MCl2 + H2
mHCl=30.\(\dfrac{14,6}{100}=4,38\left(g\right)\)
nHCl=\(\dfrac{4,38}{36,5}=0,12\left(mol\right)\)
Theo PTHH ta có:
\(\dfrac{1}{2}\)nHCl=nMO=0,06(mol)
MMO=\(\dfrac{4,8}{0,06}=80\)
MM=80-16=64
Vậy M là Cu,CTHH của oxit là CuO
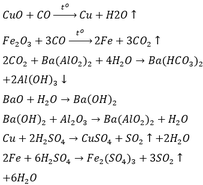
Ta có: \(n_{O_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Gọi \(\left\{{}\begin{matrix}n_A=a\left(mol\right)\\n_B=b\left(mol\right)\end{matrix}\right.\Rightarrow aM_A+bM_B=23,8\left(1\right)\)
PTHH:
\(2A+O_2\xrightarrow[]{t^o}2AO\)
a--->0,5a--->a
\(4B+3O_2\xrightarrow[]{t^o}2B_2O_3\)
b--->0,75b--->0,5b
=> 0,5a + 0,75b = 0,4 (2)
- TH1: AO không bị khử, B2O3 bị khử
PTHH:
\(B_2O_3+3H_2\xrightarrow[]{t^o}2B+3H_2O\)
0,5b-------------->b
=> a(MA + 16) + bMB = 33,4
=> aMA + bMB + 16a = 33,4
Lấy (3) - (1) => 16a = 9,6 => a = 0,6
Thay a = 0,6 vào (2) => 0,5.0,6 + 0,75.b = 0,4
=> \(b=\dfrac{2}{15}\)
=> \(0,6M_A+\dfrac{2}{15}.M_B=23,8\)
=> 9MA + 2MB = 357
=> \(\left\{{}\begin{matrix}M_A< \dfrac{357}{9}=\dfrac{119}{3}\\M_B=178,5-4,5M_A\end{matrix}\right.\)
Do A không bị khử
=> A có thể là Be, Mg
Nếu A là Be (9) => \(M_B=138\) (Loại)
Nếu A là Mg (24) => \(M_B=70,5\) (Loại)
Vậy loại TH1
- TH2: AO bị khử, B2O3 không bị khử
PTHH:
\(AO+H_2\xrightarrow[]{t^o}A+H_2O\)
a-------------->a
=> aMA + 0,5b.(2MB + 16.3) = 33,4
=> aMA + bMB + 24b = 33,4 (4)
Lấy (4) - (1) => 24b = 9,6 => b = 0,4
Thay b = 0,4 vào (2) => 0,5a + 0,4.0,75 = 0,4
=> a = 0,2
=> 0,2MA + 0,4MB = 23,8
=> MA + 2MB = 119
=> \(\left\{{}\begin{matrix}M_A=119-2M_B\\M_B< 59,5\end{matrix}\right.\)
Mà B không bị khử => B là Al
=> MA = 119 - 2.27 = 65 (g/mol)
=> A là Zn
Vậy CTHH của 2 oxit là ZnO và Al2O3
Em cảm ơn anh ạ