Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a) 4 P + 5 O2 = 2 P2O5
S + O2 = SO2
b) ta có nP2O5= 28.4/142= 0.2 (mol)
Mà nP2O5 gấp 2 lần nSO2 nên nSO2=0.2/2=0.1 (mol)
+) 4P +5O2 =2P2O5
0.4 0.5 <= 0.2 (mol)
+) S + O2 = SO2
0.1 0.1 <= 0.1 ( mol)
=> m hỗn hợp =0.1x 32+0.4x31=15.6 (g)
mà theo gthiet hỗn hợp ban đầu chứa 20% tạp chất nên khối lượng hỗn hợp thực tế ban đầu là m= 15.6+ 15.6x0.2=18.72 (g)
%m(P)=(0.4x31)/18.72= 66.24%
%m(S)=(0.1x32)/18.72=17.09%
c) tong n(O2)=0.5 + 0.1 =0.6 (mol)
=> V(O2) dktc =0.6x22.4 =13.44 (l)

3Fe+2O2 =(t0) Fe3O4
nFe=0,3 mol ; nO2= 0,3 mol;==> O2 dư
nFe3O4=nFe/3=0,1 mol suy ra mFe3O4=23,2 g
nO2 = 6,72/22,4 = 0,3 mol
=> mO2 = 0,3 * 32 = 9,6 g
theo định luật bảo toàn khối lượng:
mFe + mO2 = mFe3O4
=> mFe3O4 = 16,8 + 9,6 = 26,4 g
Vậy khối lượng của Fe3O4 tạo thành sau phản ứng là 26,4 g

2KMnO4 ---> K2MnO4 + MnO2 + O2
C + O2 ---> CO2
S + O2 ---> SO2
nO2 = 1/2nKMnO4 = 0,15 mol nên VO2 = 0,15.22,4 = 3,36 lít.
nC = 0,05 mol; nS = 0,1 mol.
Lượng oxi phản ứng vừa đủ với S, và C nên khí thu được sau phản ứng là CO2 (0,15 mol).

2Mg + O2 ---> 2MgO
n(MgO) = n(Mg) = 9,6/24 = 0,4 mol.
m(MgO) = 0,4.40 = 16 g.
V = 22,4.0,2 = 4,48 lit.

a) Phương trình hóa học của S cháy trong không khí:
S + O2 → SO2
b. Số mol của S tham gia phản ứng:
nS = = 0,05 mol
Theo phương trình hóa học, ta có: = nS =
= 0,05 mol
=> Thể tích khí sunfurơ sinh ra ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Tương tự thể tích khí oxi cần dùng ở đktc là:
= 22,4 . 0,05 = 1,12 lít
Vì khí oxi chiếm 1/5 thể tích của không khí nên thể tích không khí cần là:
=> Vkk = 5 = 5 . 1,12 = 5,6 lít
Khí metan CH4 có trong khí tự nhiên hoặc trong khí bioga. Khí metan cháy trong không khí sinh ra khí cacbon đioxit và nước:
CH4 + 2O2
#Hỏi cộng đồng OLM
#Mẫu giáo

a) Theo phương trình hóa học, ta thấy nếu đốt cháy hết 1 mol phân tử khí CH4 thì phải cần 2 mol phân tử khí O2 . Do đó thể tích khí oxi cần dùng để đốt cháy hoàn toàn 2 lít khí metan là:
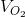 = 2 . 2 = 4 lít
= 2 . 2 = 4 lít
b) Theo phương trình phản ứng, khi đốt cháy hoàn toàn 0,15 mol khí metan thì cũng sinh ra 0,15 mol khí cacbon đioxit. Do đó thể tích khí CO2 thu được là:
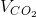 = 0,15 . 22,4 = 3,36 lít
= 0,15 . 22,4 = 3,36 lít
c) Tỉ khối của khí metan và không khí là:
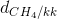 =
= 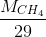 =
= 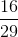 ≈ 0,55
≈ 0,55
Vậy khí metan nhẹ hơn không khí 0,55



a) lập pthh của pư
4p+5o2→2p2o5
4mol 5mol 2mol
0,2 mol 0,25mol 0,1 mol
số mol của p
np \(\frac{6,2}{31}\) =0,2mol
khối lượng p2o5 tạo thành
mp2o5= 0,1 . 142 =14,2 (g)
thể tích không khí đã dùng
Vo2 = 0,25 . 22, 4=5,6 (lít)
(tìm số mol của p2o5 và oxi là mình dùng quy tắc tam suất nói ngắn gọn là nhân chéo chia ngang ) óc gì hk hiểu bạn cứ nhắn cho mình
nP=6,2/31=0,2(mol)
4P+5O2→2P2O5
a) TPT nP2O5=1/2nP=0,1(mol)
→mP2O5=0,1*142=14,2(g)
b)TPT nO2=5/4nP=0,25(mol)
→VO2=0,25*22,4=5,6(l)