Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Câu 1:
\(Mg+Br_2\rightarrow MgBr_2\\ n_{Br_2}=\dfrac{11,2}{160}=0,07\left(mol\right)=n_{Mg}=n_{MgBr_2}\\ a=m_{Mg}=0,07.24=1,68\left(g\right)\\ m_{MgBr_2}=184.0,07=12,88\left(g\right)\)

Đáp án A
Khối lượng chất rắn tăng bằng khối lượng của Cl2 => Số mol Cl2
=> Số mol Al tham gia phản ứng => Khối lượng Al tham gia phản ứng:
nCl2 = 4,26/71 = 0,06 mol
=> nAl = 0,06x2/3 = 0, 04 mol
=> mAl = 0,04 x 27 = 1,08 gam.

Câu 1: Nhôm có tính chất hóa học riêng là có thể tác dụng được với:
A. HCl B. H2SO4 C. HNO3 D. NaOH
Câu 2: Sắt tác dụng với khí clo ở nhiệt độ cao sinh ra hợp chất:
A. FeCl3 B. FeCl2 C. FeCl D. Fe3Cl
Câu 3: Nhôm và sắt đều tác dụng được với dung dịch của:
A. NaOH B. KOH C. HCl D. Ba(OH)2
Câu 4: Sắt cháy trong khí oxi sinh ra:
A. Fe3O4 B. FeO C. Fe2O3 D. Fe2O
Câu 5: Nhôm tác dụng với axit clohiđric sinh ra muối:
A. AlCl2 B. AlCl C. AlCl3 D. Al2Cl3
Câu 6: Nguyên tắc trong sản xuất gang là dùng chất khử nào để khử quặng sắt?
A. H2 B. CO C. CO2 D. NO
Câu 7: Nguyên tắc trong sản xuất thép là dùng chất oxihóa nào để loại bỏ bớt các nguyên tố C, Mn, Si... trong gang?
A. Khí oxi B. Khí nitơ C. Khí oxi và gỉ sắt D. Khí CO
Câu 8: Hòa tan 2,7 gam Al cần dùng V lít dung dịch axit sunfuric H2SO4 1M. Giá trị của V là:
A. 0,15 B. 0,2 C. 0,25 D. 0,3
Câu 9: Để khủ hoàn toàn a gam Fe2O3 cần dùng 6,72 lít khí CO ở đktc. Giá trị của a là:
A. 16 B. 8 C. 24 D. 32
Câu 10: Hòa tan hoàn toàn 8 gam hỗn hợp A gồm 30% Mg và 70% Fe bằng dung dịch HCl dư, sau phản ứng thu được V lít khí H2 ở đktc. Giá trị của V là:
A. 2,24 B. 3,36 C. 4,48 D. 6,72

2Al + 6HCl => 2AlCl3 + 3H2
0,6 < -----0,2
2M + 2nHCl => 2MCln + nH2
0,2/n <----- 0,8 - 0,6
nH2 = 0,4 mol => nHCl = 2nH2 = 0,4.2 =0,8
=> mddHCl = \(\frac{0,8.36,5}{7,3\%}\) = 400 (g)
=> mdd = 11+ 400 - 0,4.2 = 410,2 (g)
=> mAlCl3 = 26,70402 (g) => nAlCl3 = 0,2 mol
=> nAl = nAlCl3 = 0,2 => mAl = 5,4 (g)
=> mM = 11 - 5,4 = 5,6 (g)
=> MM = \(\frac{5,6}{\frac{0,2}{n}}\) = 28n => Fe
% Al = 5,4/11 .100% = 49,09%
%Fe = 50,91%

Gọi số mol của Al và Fe lần lượt là a và b
Ta có 1,5a + b = 0,25
1,5a = 0,15
=> a = 0,1 và b = 0,1
=> %Al = 32,53%
%Fe= 67,47%
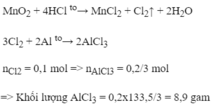
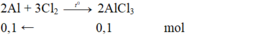


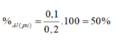
a. Đặt công thức của chất là AlxCly
\(n_{Al}=\frac{1.35}{27}=0,05\left(mol\right)\)
Bảo toàn khối lương
mAl+mCl2=6,675
\(\text{-->mCl2=5.325-->nCl2=0.075-->nCl=1.5}\)
Ta có x/y=nAl/nCl=0.05/1.5=1/3
\(\text{-->Công thức là AlCl3}\)
b. mCl2=5.325g
a) CTDC:AlxOy
Áp dụng định luật baro toàn khối lượng ta có
m Cl2=m AlxOy-m Al=6,675-1,3=5,375(g)
n Cl2=\(\frac{5,375}{71}=0,076\left(mol\right)\)--->n Cl=0,152
n Al=\(\frac{1,3}{27}=0,048\left(mol\right)\)
-->n Al:n Cl2=0,048:0,152=1:3
--->CTHH: AlCl3