Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Cách khác:
\(n_{O_2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\Rightarrow m_{O_2}=0,15.32=4,8\left(g\right)\\ Đặt.KL:B\\ 4B+3O_2\rightarrow\left(t^o\right)2B_2O_3\\ ĐLBTKL:m_B+m_{O_2}=m_{oxit}\\ \Leftrightarrow m_B+4,8=10,2\\ \Leftrightarrow m_B=5,4\left(g\right)\\ Mà:n_B=\dfrac{4}{3}.n_{O_2}=0,2\left(mol\right)\\ \Rightarrow M_B=\dfrac{5,4}{0,2}=27\left(\dfrac{g}{mol}\right)\\ \Rightarrow B\left(III\right):Nhôm\left(Al=27\right)\)

Vì kim loại có hóa trị II nên áp dụng quy tắc hóa trị
=> CTHH của sản phẩm là: `RO`
\(PTHH:2R+O_2-^{t^o}>2RO\)
tỉ lệ 2 : 1 : 2
n(mol) 0,3<----0,15---->0,3
áp dụng định luật bảo toàn khối lg ta có
\(m_R+m_{O_2}=m_{RO}\\ =>19,2+m_{O_2}=24\\ =>m_{O_2}=4,8\left(g\right)\)
\(n_{O_2}=\dfrac{m}{M}=\dfrac{4,8}{32}=0,15\)
\(M_R=\dfrac{m}{n}=\dfrac{19,2}{0,3}=64\left(g/mol\right)\)
=> R là sắt

\(n_R=\dfrac{9,75}{R};n_{RO}=\dfrac{12,15}{R+16}\)
\(PTHH:2R+O_2\xrightarrow[]{}2RO\)
tỉ lệ : 2 1 2
số mol :\(\dfrac{9,75}{R}\) \(\dfrac{12,15}{R+16}\)
=>\(\dfrac{9,75}{R}=\dfrac{12,15}{R+16}\)
=>\(R=65\)
Vì kẽm có phân tử khối là 65 và hoá trị không đổi(ll)
=>kim loại R là kẽm(Zn)

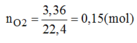
Gọi A là kí hiệu của kim loại có hóa trị III, M A là nguyên tử khối của A.
Ta có PTHH:

Theo PTHH trên ta có:
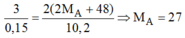
Vậy A là nhôm.

\(^nH_2=\dfrac{5,04}{22,4}=0,225\left(mol\right)\)
Gọi hóa trị của kim loại Z là x
2Z + 2xHCl ---> 2\(ZCl_x\) + xH\(_2\)
Mol \(\dfrac{0,45}{x}\) 0,225
--> Z = \(\dfrac{4,05.x}{0,45}\) = 9x
--> x = 3 thì Z = 27 (Al)
Có \(^nAl=\dfrac{5,4}{27}=0,2\left(mol\right)\)
\(4Al+3O_2\rightarrow2Al_2O_3\)
Mol 0,2 0,15
Có \(\%VO_2\left(kk\right)=20\%\)
--> V không khí cần dùng = \(\dfrac{0,15}{20\%}\) = 0,75 (mol)
Chúc bạn học tốt!!!

nO2 = 3,36/22,4 = 0,15 mol
gọi kim loại cần tìm là x
3O2 + 4X -> 2X2O3
0,15 -> 0,2 -> 0,1 (mol)
Mx2O3 = 10,2/ 0,1 = 102
=> Mx = (102 - 16*3)/2 = 27
=> kim loại đó là Al
Gọi kim loại đó là R
4R + 3O2 \(\underrightarrow{t^o}\) 2R2O3
nO2 = 0,15 mol
nR2O3 = \(\dfrac{10,2}{2R+48}\)
Theo PTHH
nR2O3 = 0,1 mol
\(\Rightarrow\) \(\dfrac{10,2}{2R+48}\) = 0,1
\(\Leftrightarrow\) 0,2R + 4,8 = 10,2
\(\Leftrightarrow\) 0,2R = 5,4
\(\Leftrightarrow\) R = 27 ( Al )
Vậy kim loại R là nhôm

nO2 = 3,36 : 22,4 = 0,15 (mol)
pthh : 4X + 3O2 -t-> 2X2O3
0,15 0,1
=> MX2O3 = 10,2 : 0,1 = 102 (G/MOL)
=> MX = (102 - 48):2 = 27 (g/mol)
=> X là Al