Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

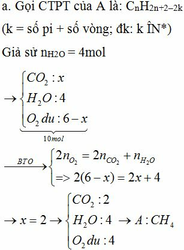
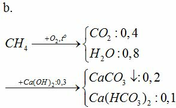
pt:
CO2 + Ca(OH)2 → CaCO3↓ + H2O
0,3 → 0,3 0,3
CO2 + CaCO3 + H2O → Ca(HCO3)2
0,1 → 0,1 0,1
m dd tăng = mCO2 + mH2O – mCaCO3 = 12g

1./ Dẫn luồng khí H2 qua ống đựng CuO:
CuO + H2 → Cu + H2O
a a a
Khối lượng chất rắn giảm:
Δm = m(CuO pư) - m(Cu) = 80a - 64a = 80 - 72,32 = 7,68g
⇒ a = 7,68/16 = 0,48g
Số mol H2 tham gia pư: n(H2) = 0,48/80% = 0,6mol
Theo ĐL bảo toàn nguyên tố, số mol HCl tham gia pư là: n(HCl pư) = 2.n(H2) = 1,2mol
Theo ĐL bảo toàn khối lượng:
m(hh rắn) + m(HCl pư) = m(muối) + m(H2) ⇒ m(muối) = m(hh rắn) + m(HCl pư) - m(H2)
⇒ m(muối) = 65,45 + 0,12.36,5 - 0,6.2 = 108,05g
Gọi x, y là số mol Al và Zn có trong hh KL ban đầu.
m(hh KL) = m(Al) + m(Zn) = 27x + 65y = 40,6g
m(muối) = m(AlCl3) + m(ZnCl2) = 133,5x + 136y = 108,05g
⇒ x = 0,3mol và y = 0,5mol
Khối lượng mỗi kim loại:
m(Al) = 0,3.27 = 8,1g; m(Zn) = 65.0,5 = 32,5g
Thành phần % khối lượng mỗi kim loại:
%Al = 8,1/40,6 .100% = 19,95%
%Zn = 32,5/40,6 .100% = 80,05%

Phương trình hóa học của phản ứng:
C O 2 + Ca OH 2 → Ca CO 3 + H 2 O
CuO + CO → t ° C O 2 + Cu
Theo phương trình ta có:
n CO 2 = n CaCO 3 = 5/100 = 0,05 mol
n CO = n Cu = 3,2/64 = 0,05 mol
n CaCO 3 = 5/100 = 0,05 mol
n Cu = 3,2/64 = 0,05 mol
Như vậy: n hh = 10/22,4 = 0,45 mol; n N 2 = 0,45 - 0,05 - 0,05 = 0,35 mol
% V N 2 = 0,35/0,45 x 100% = 77,78%
% V CO 2 = % V CO = 0,05/0,45 x 100% = 11,11%
Nếu cho phản ứng (2) thực hiện trước rồi mới đến phản ứng (1) thì
∑ n CO 2 = 0,05 + 0,05 = 0,1 mol
n CaCO 3 = 0,1 mol
Vậy m CaCO 3 = 0,1 x 100 = 10g

C chứa N2, O2
Gọi \(\left\{{}\begin{matrix}n_{N_2}=x\left(mol\right)\\n_{O_2\left(dư\right)}=y\left(mol\right)\end{matrix}\right.\)
=> \(\overline{M}=\dfrac{28x+32y}{x+y}=15,2.2=30,4\left(g/mol\right)\)
=> 2,4x = 1,6y
=> 1,5x = y (1)
\(n_{H_2O}=\dfrac{9}{18}=0,5\left(mol\right)\)
Gọi số mol CO2 là z (mol)
=> \(x+y+z=\dfrac{14,56}{22,4}=0,65\left(mol\right)\) (2)
Bảo toàn C: nC(A) = z (mol)
Bảo toàn H: nH(A) = 1 (mol)
Bảo toàn N: nN(A) = 2x (mol)
\(n_{O_2\left(pư\right)}=\dfrac{13,44}{22,4}-y=0,6-y\left(mol\right)\)
Bảo toàn O: \(n_{O\left(A\right)}+2n_{O_2\left(pư\right)}=2n_{CO_2}+n_{H_2O}\)
=> \(n_{O\left(A\right)}=2y+2z-0,7\left(mol\right)\)
Do mA = 15 (g)
=> 12z + 1 + 28x + 32y + 32z - 11,2 = 15
=> 28x + 32y + 44z = 25,2 (3)
(1)(2)(3) => \(\left\{{}\begin{matrix}x=0,1\left(mol\right)\\y=0,15\left(mol\right)\\z=0,4\left(mol\right)\end{matrix}\right.\)
nC(A) = 0,4 (mol)
nH(A) = 1 (mol)
nO(A) = 0,4 (mol)
nN(A) = 0,2 (mol)
Xét nC(A) : nH(A) : nO(A) : nN(A) = 0,4 : 1 : 0,4 : 0,2 = 2 : 5 : 2 : 1
Mà A có 1 nguyên tử N
=> CTPT: C2H5O2N

Y gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:b\left(mol\right)\\H_2O:c\left(mol\right)\end{matrix}\right.\)
Z gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:b\left(mol\right)\end{matrix}\right.\)
Do nZ = 50%.nY
=> a + b = 0,5a + 0,5b + 0,5c
=> \(c=a+b\)
Khí thoát ra khỏi dd NaOH là khí A
\(n_{CO_2}=83,33\%.n_Z\)
=> b = 0,8333.(a + b)
=> 5a = b
=> Y gồm \(\left\{{}\begin{matrix}A:a\left(mol\right)\\CO_2:5a\left(mol\right)\\H_2O:6a\left(mol\right)\end{matrix}\right.\)
=> nC(A pư) : nH(A pư) = 5a : 12a = 5 : 12
=> CTPT: (C5H12)n
Chọn n = 1 thỏa mãn => CTPT: C5H12

Câu 1 :
Theo đề : V H2O = 1600 - 800 = 800ml
V CO2 = 800 - 200 = 600ml
V O2 dư = 200ml \(\Rightarrow\) V O2 pứ = 800ml
Đặt CTPT của A là CxHyOz
PTPƯ cháy :
CxHyOz + \(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)O2 \(\rightarrow\) xCO2 + \(\dfrac{y}{2}\)H2O
1ml............\(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)ml......xml.........\(\dfrac{y}{2}\)ml
200ml..................800ml..............600ml........800ml
\(\Rightarrow\) \(\dfrac{1}{200}=\dfrac{x+\dfrac{y}{4}-\dfrac{z}{2}}{800}=\dfrac{x}{600}=\dfrac{y}{1600}\)
\(\Rightarrow\) x=3 , y=8 , z=2
Vậy CTPT của A là C3H8O2
Câu 2 :
Theo đề ta có : M\(_A\)= 62 \(\Rightarrow\) n\(_A\)=0,1 mol
n O2 = 0,25 mol
Đặt CTPT của A là CxHyOz
PTPƯ cháy :
CxHyOz + \(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)O2 \(\rightarrow\) xCO2 + \(\dfrac{y}{2}\)H2O
0,1mol.......\(\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)\)0,1mol..0,1xmol...0,05ymol
Ta có hệ phương trình :
\(\left\{{}\begin{matrix}\left(x+\dfrac{y}{4}-\dfrac{z}{2}\right)0,1=0,25\\12x+y+16z=62\\\dfrac{0,1x}{0,05y}=\dfrac{2}{3}\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=2\\y=6\\z=2\end{matrix}\right.\)
Vậy CTPT của A là C2H6O2
Ai giải hộ tui với
C3H8 đó bạn