Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

a, xử lí số liệu:( đơn vị %)
| năm | 1990 | 2000 | 2005 | 2010 |
|---|---|---|---|---|
| dân số | 100 | 117,7 | 125,8 | 133,4 |
| sản lượng lúa | 100 | 136,8 | 155,8 | 183,4 |
Vẽ biểu đồ:
- vẽ khung như biểu đồ cột, trục tung là sản lượng lúa(%), trục hoành là năm, nhưng trục tung và trục hoành giao nhau ở 1 điểm đó, mày lấy là 0 và năm 1990, trục hoành chia 0, 20, 40,..., 200; trục tung chia năm là 1990 , 2000, 2005, 2010( khoảng cách mấy năm khác nhau đấy)
- đánh dậu đậm vào mốc 100 => năm 1990 sản lượng là 100%
- dóng mầy cái năm kia lên, vẽ biểu đồ gấp khúc, nhớ đánh dấu đậm mấy cái điểm ứng với các năm và ghi số liệu ra
- làm 2 lần, 2 đường gấp khúc là dân số và sản lượng lúa=> kí hiệu dấu đậm ở cột sản lượng là tròn đậm, cột năm là vuông đậm, mốc 100 là cả 2 đè lên nhau
- ghi tên biểu đồ ở dưới
b,
| năm | 1990 | 2000 | 2005 | 2010 |
|---|---|---|---|---|
| sản lượng lúa bình quân đầu người(kg/người) | 250,7 | 291,5 | 310,3 | 344,8 |
Nhận xét:
- sản lượng láu bình quân đầu người của đna có xu hướng tăng
- tăng nhanh nhất khi nào, ít nhất khi nào
( nhớ nêu ra số liệu)
cho mk ik

Hàng 1: (17+8)=5x5
Hàng 2: (13+7)=5x4
Hàng 3: (6+12)=6x3
Hàng 4: (10x6)=4x15
=> ?=15

a,
QUẢNG CÁO
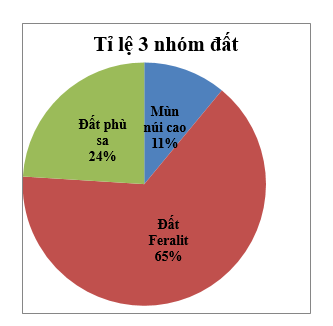
b, Nhận xét:
– Đất phù sa mới chủ yếu phân bố ở các đồng bằng: đồng bằng sông Hồng, đồng bằng sông Cửu Long và các đồng bằng Duyên hải miền Trung.
– Đất xám phân bố ở Đông Nam Bộ và phía tây Tây Nguyên.
– Đất pheralit badan tập trung nhiều nhất ở Tây Nguyên.
– Các loại đất pheralit khác và đất mùn núi cao có diện tích lớn nhâ’t và phân bô ở nhiều khu vực nước ta Trung du và miền núi Bắc Bộ, Ouyên hải Miền Trung, Tây Nguyên…

Khoản chi tiêu | Số tiền (đồng) | Tỉ lệ (%) |
Cho học tập của con, dịch vụ y tế và chăm sóc sức khỏe | 800 000 | 16 |
Cho các con nhu cầu thiết yếu | 2 500 000 | 50 |
Cho mua sắm cá nhân | 700 000 | 14 |
Cho tiết kiệm | 1 000 000 | 20 |