Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
Các phương trình phản ứng:
Nhiệt phân hỗn hợp X:
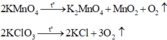
Chất rắn Y gồm K2MnO4, MnO2, KCl, KMnO4 dư. Rắn Y tác dụng với dung dịch HCl đặc:
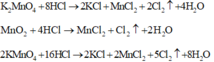
Tính toán:
Gọi số mol các chất trong hỗn hợp X là KMnO4: a mol ; KClO3: b mol. Ta có:
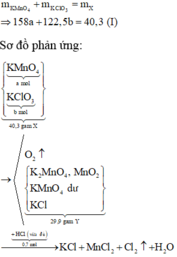
Bảo toàn khối lượng cho giai đoạn nhiệt phân X ta có:
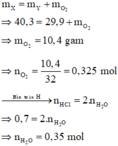
Theo sơ đồ thì cuối cùng O trong Y chuyển hết về H2O. Bảo toàn nguyên tố O cho giai đoạn nhiệt phân X ta có:

Xét giai đoạn nhiệt phân X:
Gọi x là số mol KMnO4 phản ứng
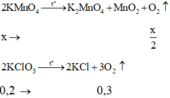
Hiệu suất nhiệt phân KMnO4 là:
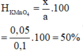

a) \(\left\{{}\begin{matrix}160n_{Fe_2O_3}+80n_{CuO}=24\\n_{Fe_2O_3}=n_{CuO}\end{matrix}\right.\Rightarrow n_{Fe_2O_3}=n_{CuO}=0,1\)
\(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{160.0,1}{24}.100\%=66,67\%\\\%m_{CuO}=\dfrac{80.0,1}{24}.100\%=33,33\%\end{matrix}\right.\)
PTHH: Fe2O3 + 3H2SO4 --> Fe2(SO4)3 + 3H2O
0,1------>0,3-------->0,1
CuO + H2SO4 --> CuSO4 + H2O
0,1-->0,1---------->0,1
nCuSO4 = 0,1 (mol)
nFe2(SO4)3 = 0,1 (mol)
=> m = 0,1.160 + 0,1.400 = 56(g)
b) \(m_{H_2SO_4\left(pthh\right)}=\left(0,3+0,1\right).98=39,2\left(g\right)\)
=> mH2SO4(thực tế) = \(\dfrac{39,2.125}{100}=49\left(g\right)\)
c) \(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
=> nBaSO4 = 0,5 (mol)
=> mBaSO4 = 0,5.233 = 116,5(g)

Gọi số mol Fe2O3, CuO là a, b (mol)
nHCl = 0,3.2 = 0,6 (mol)
PTHH: Fe2O3 + 6HCl --> 2FeCl3 + 3H2O
a----->6a------->2a
CuO + 2HCl --> CuCl2 + H2O
b----->2b------->b
=> \(\left\{{}\begin{matrix}\dfrac{2a}{b}=\dfrac{3}{4}\\6a+2b=0,6\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}a=\dfrac{9}{170}\left(mol\right)\\b=\dfrac{12}{85}\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{Fe_2O_3}=\dfrac{\dfrac{9}{170}.160}{\dfrac{9}{170}.160+\dfrac{12}{85}.80}.100\%=42,857\%\\\%m_{CuO}=\dfrac{\dfrac{12}{85}.80}{\dfrac{9}{170}.160+\dfrac{12}{85}.80}.100\%=57,143\%\end{matrix}\right.\)

Vì các kim loại không thay đổi hóa trị nên khối lượng muối của oxit phản ứng với HCl bằng khối lượng muối của kim loại phản ứng với Cl2 dư
Có nHCl=2\(n_{H_2}\)=0,1(mol)
=>mHCl=0,1.36,5=3,65(g)
\(m_{H_2O}\)=\(\dfrac{0,1}{2}.18=0.9\left(g\right)\)
Theo ĐLBTKL ta có
moxit+maxit=mmuối+mnước
=>mmuối=24,35(g)
Khối lượng muối clorua thu được khi cho X tác dụng với Cl2 dư hay oxit Y tác dụng với HCl là như nhau vì mX không đổi, hoá trị không đổi
PTHH: \(MgO+2HCl\rightarrow MgCl_2+H_2O\)
\(Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2O\)
\(ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
Ta có: \(n_{HCl}=0,1\cdot1=0,1\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}m_{HCl}=0,1\cdot36,5=3,65\left(g\right)\\n_{H_2O}=0,05\left(mol\right)\Rightarrow m_{H_2O}=0,05\cdot18=0,9\left(g\right)\end{matrix}\right.\)
Bảo toàn khối lượng: \(m_{muối}=m_{oxit}+m_{HCl}-m_{H_2O}=21,6+3,65-0,9=24,35\left(g\right)\)

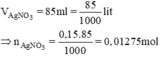
Phương trình hóa học của phản ứng:
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Theo pt:
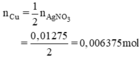
mCu tham gia phản ứng: 0,006375 × 64 = 0,408 g.

\(n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ \Rightarrow n_{Fe_2(SO_4)_3} = \dfrac{1}{2}n_{Fe} = 0,1(mol)\\ \Rightarrow m_{Fe_2(SO_4)_3} = 0,1.400 = 40(gam) \)
\(m_{O_2}=14.4-11.2=3.2\left(g\right)\)
\(n_{O_2}=\dfrac{3.2}{32}=0.1\left(mol\right)\)
\(O_2+4e\rightarrow2O^{2-}\)
\(0.1....0.4\)
\(S^{+6}+2e\rightarrow S^{+4}\)
\(.......0.4.....0.2\)
\(n_{H_2SO_4}=2\cdot0.2=0.4\left(mol\right)\)
\(n_{H_2O}=\dfrac{1}{2}n_{H_2SO_4}=\dfrac{0.4}{2}=0.2\left(mol\right)\)
\(BTKL:\)
\(m_{Muối}=14.4+0.4\cdot98-0.2\cdot64-0.2\cdot18=37.2\left(g\right)\)

Đáp án C.
Do số mol FeO bằng số mol Fe2O3,
Coi hỗn hợp chỉ có Fe3O4.
![]()
Fe3O4 + 4H2SO4 → Fe2(SO4)3 + FeSO4 + 4H2O
0,01 0,04
V = 0,04/0,5 = 0,08 lít

HD:
Cu + 2AgNO3 \(\rightarrow\) Cu(NO3)2 + 2Ag
Số mol Cu = 1/2 số mol AgNO3 = 0,15.0,085/2 = 0,006375 mol.
Khối lượng Cu = 0,006375.64 = 0.408 g.




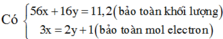
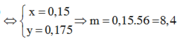
nO = nCO(phản ứng) = 0,7mol
m(rắn) = mhh - mO = 40 – 0,7.16 = 28,8g