Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

-Thí nghiệm: Cho một ít KMnO4 hoặc KClO3 vào ống nghiệm có cắm ống dẫn khí,đầu ống nghiệm được nút lại.
Câu hỏi là: cách điều chế oxi trong phòng thí nghiệm á
Giúp mình đi mọi ngừi ơiii 😥🥺

PTHH: Na2O + H2O → 2NaOH
Số mol của NaOH là: 16 : 40 = 0,4 mol
Số mol của Na2O là: 0,4 : 2 = 0,2 mol
Khối lượng Na2O cần lấy là: 0,2 . 62 = 12,4 gam

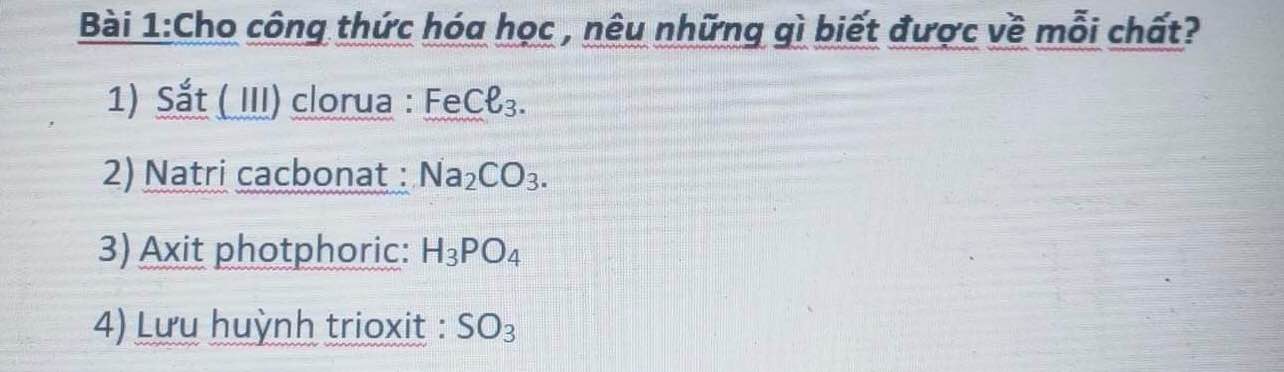
1.
- Hợp chất cấu tạo từ 2 nguyên tố: Fe và Cl
- Hợp chất có: 1 nguyên tố Fe và 3 nguyên tố Cl
- PTK=56+35,5 x 3=162,5(đvC)PTK=56+35,5 x 3=162,5(đvC)
===========
2.
- Hợp chất cấu tạo từ 3 nguyên tố: Na, C và O
- Hợp chất có: 2 nguyên tố Na, 1 nguyên tố C và 3 nguyên tố O
- PTK=23 x 2+12+16 x 3=106(đvC)PTK=23 x 2+12+16 x 3=106(đvC)
==========
3.
- Hợp chất cấu tạo từ 3 nguyên tố: H, P và O
- Hợp chất có: 2 nguyên tố H, 1 nguyên tố P và 4 nguyên tố O
- PTK=1 x 3+31+16 x 4=98(đvC)PTK=1 x 3+31+16 x 4=98(đvC)
==========
4.
- Hợp chất cấu tạo từ 2 nguyên tố: S và O
- Hợp chất có: 1 nguyên tố S và 3 nguyên tố O
- PTK=32+16 x 3=80(đvC)

n NaOH= 16 : 40 = 0,4 (mol)
pthh: Na2O + H2O --> 2NaOH
0,2<--------------------0,4(mol)
=> mNa2O = 0,2 . 62= 12,4 (g)


Fe + 2HCl \(\rightarrow\) FeCl2 + H2
nFe = \(\dfrac{28}{56}=0,5mol\)
a)Theo pt: nHCl = 2nFe = 1mol
=> mHCl = 1.36,5 = 36,5g
=> mddHCl = \(\dfrac{36,5.100}{10}=365g\)
b) Theo pt nFeCl2 = nFe = 0,5 mol
=> mFeCl2 = 0,5.129 = 64,5g
Theo pt: nH2 = nFe = 0,5 mol
=> VH2 = 0,5.22,4=11,2 lít
c) FeCl2 chứ nhỉ
Bảo toàn khối lượng: mddFeCl2 = mFe + mddHCl - mH2
= 28 + 365 - 0,5.2 = 392g
C%ddFeCl2 = \(\dfrac{64,5}{392}.100\%=46,45\%\)




\(n_{Ca\left(OH\right)_2}=\dfrac{7,4}{74}=0,1\left(mol\right)\)
PTHH: CaO + H2O --> Ca(OH)2
0,1<--------------0,1
=> mCaO = 0,1.56 = 5,6 (g)