Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(n_{Fe_2O_3}=\dfrac{m}{M}=\dfrac{24}{160}=0,15\left(mol\right)\\ n_{Fe}=\dfrac{m}{M}=\dfrac{19,2}{56}=\dfrac{12}{35}\left(mol\right)\)
\(pthh:\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }Fe_2O_3+3H_2\overset{t^0}{\rightarrow}2Fe+3H_2O\)
\(Theo\text{ }pthh:1mol\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }3mol\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }2mol\)
\(Theo\text{ }đb:0,15mol\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\dfrac{12}{35}mol\)
Phản ứng:\(\dfrac{0,15mol}{ }\text{ }\text{ }0,45mol\text{ }\text{ }\text{ }\dfrac{0,3mol}{ }\)
\(\text{Sau pứ: }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }0\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\text{ }\dfrac{3}{70}mol\)
\(\Rightarrow V_{H_2}=n\cdot22,4=0,45\cdot22,4=10,08\left(l\right)=1008\left(cm^3\right)\)

dẫn luồng khí CO đi qua ống sứ chứa 0,3 mol hỗn hợp A(FeO và Fe2O3) nung nóng . Sau một thời gian phản ứng thu được 24 gam chất rắn B gồm FeO,Fe3O4,Fe2O3,Fe và

PTHH:
4H2+Fe3O4----->3Fe+4H2O
nH2=V/22,4=6,72/22,4=0,3mol
Theo PTHH:4molH2--->3molFe 0,3molH2->0,3.3/4=0,225molFe
mFe=nFe.M=0,225.56=12,6g
nO= nH2O= nH2= 0,3(mol)
m=m(oxit) - mO= 24- 0,3.16= 19,2(g)

\(m_{H_2SO_4}=\dfrac{100.96,48}{100}=96,48\left(g\right)\)
\(m_{dd.sau.thí.nghiệm}=\dfrac{96,48.100}{90}=107,2\left(g\right)\)
=> \(m_{H_2O\left(thêm\right)}=107,2-100=7,2\left(g\right)\Rightarrow n_{H_2O}=\dfrac{7,2}{18}=0,4\left(mol\right)\)
=> nO(mất đi) = 0,4 (mol)
Có: mX = mY + mO(mất đi) = 113,6 + 0,4.16 = 120 (g)

Cho a gam Fe tan hết trong dd HCl thu dc V lít H2 (đktc) . Cho V lít H2 đi qua ống đựng 81 gam ZnO đã nung nóng , sau 1 thời gian còn lại73 gam chất rắn và chỉ có80% H2 tham gia phản ứng.
a, Tính V
b, Tính a

\(a,n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:2K+2H_2O\rightarrow2KOH+H_2\uparrow\\ Theo.pt:n_K=2n_{H_2}=2.0,1=0,2\left(mol\right)\\ m_K=0,2.39=7,8\left(g\right)\\ m_{K_2O}=17,2-7,8=9,4\left(g\right)\\ b,n_{CuO\left(bđ\right)}=\dfrac{12}{80}=0,15\left(mol\right)\\ PTHH:CuO+H_2\underrightarrow{t^o}Cu+H_2O\\ LTL:0,15>0,1\Rightarrow Cu.dư\)
Gọi nCuO (pư) = a (mol)
=> nCu = a (mol)
mchất rắn sau pư = 80(0,15 - a) + 64a = 10,8
=> a = 0,075 (mol)
=> nH2 (pư) = 0,075 (mol)
\(H=\dfrac{0,075}{0,1}=75\%\)

\(n_{H_2}=\dfrac{8.96}{22.4}=0.4\left(mol\right)\)
\(BTKL:\)
\(m+0.4\cdot2=28.4+7.2\)
\(\Rightarrow m=34.8\left(g\right)\)
\(b.\)
\(m_{Fe}=0.59155\cdot28.4=16.8\left(g\right)\)
\(n_{Fe}=\dfrac{16.8}{56}=0.3\left(mol\right)\)
\(PTHH:\)
\(\dfrac{x}{y}=\dfrac{n_{Fe}}{n_{H_2}}=\dfrac{0.3}{0.4}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)

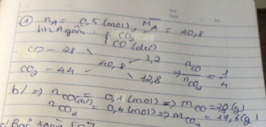
nFe3O4=24/232=0,1(mol)
Fe3O4+4H2--->3Fe+4H2O
0,1___________0,3
mFe=0,3.56=16,8(g)
=>Fe3O4 dư
=> A chứa: \(\left\{{}\begin{matrix}Fe\\Fe3O4dư\end{matrix}\right.\)