Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án D
(NH4)2SO4+ Ba(OH)2 → BaSO4+ 2NH3+ 2H2O
2FeCl3+3 Ba(OH)2 → 2Fe(OH)3+ 3BaCl2
2Cr(NO3)3+ 3Ba(OH)2 → 2Cr(OH)3+ 3Ba(NO3)2
2Cr(OH)3+ Ba(OH)2 → Ba(CrO2)2+ 4H2O
K2CO3+ Ba(OH)2 → BaCO3+ 2KOH
2AlCl3+ 3Ba(OH)2 →2Al(OH)3+ 3Ba(NO3)2
2Al(OH)3+ Ba(OH)2 → Ba(AlO2)2+ 4H2O
Số ống nghiệm có kết tủa là: (NH4)2SO4; K2CO3; FeCl3

Đáp án A
Ba2+ + SO42- →BaSO4
0,05.2→ 0,1
Al3++ 3NH3+ 3H2O→ Al(OH)3+ 3NH4+
0,1← 0,1
Gọi số mol Cu2+, NO3- có trong 500 ml dung dịch X lần lượt là x, y mol
ĐLBT ĐT: 0,1.3+2x=y+0,1.2
27.0,1+64x+62y+ 0,1.96= 37,3 suy ra 0,1; y=0,3
Nồng độ mol của Cu2+ là: 0,1/0,5=0,2M

Đáp án B
(NH4)2SO4 + Ba(OH)2 → BaSO4↓ + 2NH3 + 2H2O
FeCl2 + Ba(OH)2 → BaCl2 + Fe(OH)2 ↓
2Cr(NO3)3 + 4Ba(OH)2 → 3Ba(NO3)2 + Ba(CrO2)2 + 4H2O
K2CO3 + Ba(OH)2 → BaCO3 ↓ + 2KOH
2Al(NO3)3 + 4Ba(OH)2 → 3Ba(NO3)2 + Ba(AlO2)2 + 4H2O
Đáp án B.

Đáp án C
Gọi số mol mỗi ion NH4+, K+, CO32-, SO42- trong mỗi phần lần lượt là x, y, z , t mol
Phần 1: Ba2++ CO32-→ BaCO3
z z
Ba2++ SO42- → BaSO4
t t
NH4++ OH-→ NH3+ H2O
x x = 0,3 mol
mkết tủa= mBaCO3+ mBaSO4= 197z+233t= 43 suy ra t= 0,1 mol
Phần 2: 2H++ CO32- → CO2+ H2O
z mol z mol= 0,1
Định luật bảo toàn điện tích: x+y=2z+ 2t suy ra y= 0,1 mol
mmuối= (18x+ 39y+60z+96t).2= 49,8 gam

Đáp án A
Gọi số mol Al3+, NH4+, SO42- trong 100 ml dung dịch Y lần lượt là x, y, z mol
-Phần 1:
Al3++ 3NH3+ 3H2O→ Al(OH)3+ 3NH4+
x/5 x/5 = 2.10-3 suy ra x = 0,01 mol
-Phần 2:
Ba2++ SO42-→ BaSO4
z/5 mol z/5 mol = 0,932/233 = 4.10-3 mol nên z = 0,02 mol
ĐLBT ĐT suy ra y = 0,01 mol suy ra nH2O = 0,12 mol
Suy ra CT là Al.NH4.(SO4)2.12H2O

Chọn đáp án D.
Sau khi điện phân thu được hỗn hợp kim loại => Fe3+, Cu2+ bị điện phân hết, Fe2+ đã bị điện phân.
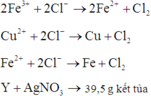
=> Chứng tỏ Y chứa FeCl2 dư.
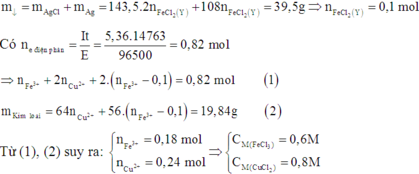

Phương trình minh họa:
CO2 + Ca(OH)2 → CaCO3 + H2O (1)
CaCO3 + CO2 + H2O → Ca(HCO3)2 (2)
Ca(HCO3)2 + 2KOH → CaCO3 + K2CO3 + 2H2O
Số mol kết tủa lần 1 là 0,04 mol và số mol kết tủa lần 2 là 0,08 mol.
Suy ra số mol Ca2+ là 0,12 bằng số mol của Ca(OH)2 ban đầu.
Giá trị m = 0,12.74/18,5% = 48 (g).

Chọn A
Gọi số mol Na + , NH 4 + , CO 3 2 - và SO 4 2 - trong 100ml dung dịch X lần lượt là x, y, z và t.
Bảo toàn điện tích có: x + y – 2z – 2t = 0 (1)
Cho 100ml X tác dụng với HCl dư:
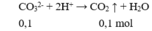
→ z = 0,1 (2)
Cho 100ml X tác dụng với BaCl2 dư:
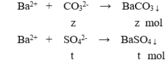
m↓ = 43 (gam) → 197z + 233t = 43 (3)
Cho 100 ml X tác dụng với NaOH
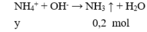
→ y = 0,2 (4)
Từ (1); (2); (3); (4) có x = y = 0,2; z = 0,1; t = 0,1.
Tổng khối lượng muối trong 300ml dung dịch là:
m = 3. (0,2.23 + 0,2.18 + 0,1.60 + 0,1.96) = 71,4 gam.
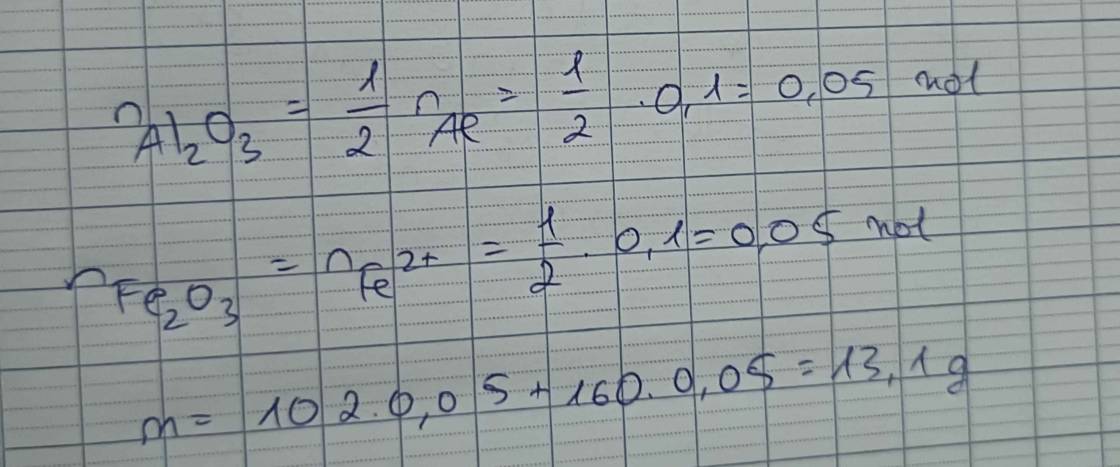
Đáp án B
Khi cho dung dịch muối qua KOH dư thu được kết tủa : Cu(OH)2, Fe(OH)3.
CuCl2 + 2KOH dư → Cu(OH)2↓ + 2KCl
Cr(NO3)3 + 4KOH dư → KCrO2 + 3KNO3 + 2H2O
ZnCl2 + 4KOH dư → K2ZnO4 + 2KCl + 2H2O
FeCl3 + 3KOH dư → Fe(OH)3↓ + 3KCl
AlCl3 + 4KOH dư → KAlO2 + 3KCl + 2H2O
Sau đó cho tác dụng với dung dịch NH3 dư thì chỉ thu được 1 kết tủa duy nhất là Fe(OH)3. Do Cu(OH)2 có khả năng tạo phứ với NH3
Cu(OH)2 + 4NH3 → [Cu(NH3)4](OH)2
Đáp án B.