
Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

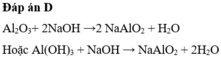

Câu 1:Cho các bazơ NaOH; KOH; Ba(OH)2; Al(OH)3. Bazơ không tan trong nước là NaOH. B. KOH. C. Ba(OH)2 . D. Al(OH)3
Câu 2: Cho các chất NaOH; Fe(OH)3; SO2; K2O. Số cặp chất xảy ra phản ứng hóa học là
A.1 B. 2 C. 3 D. 4
Câu 3: Nhiệt phân hoàn toàn 100 kg CaCO3, thu được 44 kg CO2 và
A. 56 kg Ca. B. 56 kg CaO. C. 65 kg Ca. D. 65 kg CaO.
\(CaCO_3\xrightarrow[]{t^0}CaO+CO_2\\ BTKL:m_{CaCO_3}=m_{CaO}+m_{CO_2}\\ \Rightarrow m_{CaO}=m_{CaCO_3}-m_{CO_2}=100-44=56kg\)
Câu 4: Magie đihiđrophotphat là tên gọi của
A. MgH2SO4 . B. Mg(H2PO4)2. C. Mg(HPO4)2. D. Mg(HSO4)2
Câu 5:Cho các oxit CO2; CO; SO2; N2O5. Oxit không tác dụng với dung dịch KOH là A. CO2 . B. CO. C. SO2. D. N2O5.
Câu 6: Nhôm oxit tác dụng được cặp chất nào sau đây?
A. HCl, KOH. B. HCl, NaOH. C. HCl, H2SO4 . D. HNO3, Ca(OH)2.
Đề sai nhé
Câu 7: Cho các dung dịch Ba(OH)2; NaOH; HCl; H2SO4; K2SO4. Chỉ dùng quỳ tím có thể nhận biết được tối đa bao nhiêu dung dịch?
A. 5 B. 2 C. 3 D.1
| \(Ba\left(OH\right)_2\) | \(NaOH\) | \(HCl\) | \(H_2SO_4\) | \(K_2SO_4\) | |
| Quỳ tím | Xanh | Xanh | Đỏ | Đỏ | _ |
| \(K_2SO_4\) | ↓Trắng | _ | _ | _ | |
| \(Ba\left(OH\right)_2\) | _ | _ | ↓Trắng |
\(K_2SO_4+Ba\left(OH\right)_2\rightarrow BaSO_4+2KOH\\ Ba\left(OH\right)_2+H_2SO_4\rightarrow BaSO_4+2H_2O\)
Câu 8: Những oxit tác dụng được với dung dịch H2SO4 là:
A. Fe2O3, SO2 . B. SO2, CO2 . C. Fe2O3, MgO. D. CuO, CO2 .
Câu 9: Có phương trình hóa học sau: Fe + H2SO4 FeSO4 + H2 . Nếu có 5,6 gam sắt tham gia phản ứng, thì khối lượng của axit sunfuric cần dùng là
A. 35,6 g. B. 7,8 g. C. 24,5 g. D. 9,8 g. .
\(n_{Fe}=\dfrac{5,6}{56}=0,1mol\\ n_{Fe}=n_{H_2SO_4}=0,1mol\\ m_{H_2SO_4}=0,1.98=9,8g\)
Câu 11: Sục khí SO2 vào một cốc nước cất, sau đó nhúng mẩu giấy quỳ tím vào dung dịch thu được, màu của quỳ tím
A. chuyển sang màu xanh. B. mất màu. C. không đổi màu. D. chuyển sang màu đỏ.
\(SO_2+H_2O⇌H_2SO_3\left(axit\right)\)
Câu 12: Cho một mẩu CaO vào một ống nghiệm đựng nước cất, sau đó nhỏ vài giọt dung dịch phenolphtalein vào dung dịch thu được, dung dịch chuyển sang màu gì ?
A. Chuyển sang màu xanh. B. Chuyển sang màu đỏ. C. Không đổi màu. D. Mất màu.
\(CaO+H_2O\rightarrow Ca\left(OH\right)_2\left(bazơ\right)\)
Câu 13:Cho các bazơ NaOH, Ca(OH)2, Al(OH)3, Ba(OH)2. Số bazơ tác dụng với dung dịch HCl là
A. 1 B. 2 C. 3 D. 4
Câu 14: Để phân biệt hai dung dịch Na2SO4 và Na2CO3 người ta có thể dùng thuốc thử nào sau đây?
A. Ba(OH)2. B. BaCl2. C. NaNO3. D. HCl.
Câu 15:Khí có khả năng làm đục nước vôi trong là
A. CO2. B. O2 . C. N2 . D. Cl2.
Câu 16: Những oxit tác dụng được với dung dịch HCl là:
A. Fe2O3, SO2 . B. SO2, CO2 . C. Fe2O3, MgO. D. CuO, CO2 .
Câu 17: Biết rằng 1,12 lít khí cacbonddioxxit (đktc) tác dụng vừa đủ với 100ml dung dịch NaOH tạo ra muối trung hòa. Vậy nồng độ mol của dung dịch NaOH đã dùng là:
A. 2M B. 3M C. 4M D. 1M
\(n_{CO_2}=\dfrac{1,12}{22,4}=0,05mol\\ 2NaOH+CO_2\rightarrow Na_2CO_3+H_2O\\ n_{NaOH}=0,05.2=0,1mol\\ C_{M_{NaOH}}=\dfrac{0,1}{0,1}=1M\)
Câu 18: Dãy gồm các bazơ bị nhiệt phân hủy là
A. Cu(OH)2, Mg(OH)2, NaOH.
B. Fe(OH)3, KOH, Mg(OH)2.
C. Al(OH)3, Fe(OH)2, Mg(OH)2
D. Fe(OH)2, Ba(OH)2, Mg(OH)2.
Câu 19: Chất tác dụng với H2O tạo ra dung dịch bazơ là
A. MgO. B. Na2O. C. SO2. D. Fe2O3.
Câu 20: Màng trắng trên bề mặt dung dịch nước vôi trong là sản phẩm của phản ứng giữa cặp chất nào sau đây?
A. CO2 và H2O B. CaO và H2O C. CO2 và Ca(OH)2 D. CaO và CO2
Câu 21: Khí nào được tạo thành khi cho axit sunfuric tác dụng với kẽm?
A. H2 . B. CO2 . C.Cl2 . D. SO2 .
Câu 22: Nguyên liệu để sản xuất NaOH trong công nghiệp là
A. Na B. Na2O C. NaCl D. Na2CO3
Câu 23. Khí nào được tạo thành khi cho axit clohidric tác dụng với sắt?
A. H2 . B. CO2 . C.Cl2 . D. SO2 .
Câu 24. Để phân biệt hai dung dịch K2SO4 và K2CO3 người ta có thể dùng thuốc thử nào sau đây?
A. Ba(NO3)2. B. BaCl2. C. KNO3. D. HCl.
Câu 25. Chất tác dụng với H2O tạo ra dung dịch bazơ (kiềm) là
A. ZnO. B. BaO. C. PbO. D. Al2O3.

- Chất tác dụng được với dd HCl và NaOH: Al
Vì: 2Al + 6HCl → 2AlCl3 + 3H2
2Al + 2NaOH + 2H2O → 2NaAlO2 + 3H2
- Axit axetic không phản ứng được với: NaCl

\(MgCl_2+Ba\left(OH\right)_2\rightarrow BaCl_2+Mg\left(OH\right)_2\downarrow\)
\(Al\left(OH\right)_3+3HCl\rightarrow AlCl_3+3H_2O\)
\(2AgNO_3+CuCl_2\rightarrow Cu\left(NO_3\right)_2+2AgCl\downarrow\)
\(K_2O+H_2O\rightarrow2KOH\)
\(Na+H_2O\rightarrow NaOH+\dfrac{1}{2}H_2\)

a. Fe2O3 + 6HCl ---> 2FeCl3 + 3H2O
FeCl3 + 3NaOH ----> Fe(OH)3 + 3NaCl
2Fe(OH)3 --t°-> Fe2O3 + 3H2O
2Fe2O3 --t°--> 4Fe + 3O2
Fe +H2SO4 ---> FeSO4 + H2
FeSO4 + 2HNO3 ---> Fe(NO3)2 + H2SO4
Bài 1: Hoàn thành chuỗi phản ứng sau:
a) Fe2O3+6HCl →2FeCl3+3H2O
FeCl3+3NaOH → Fe(OH)3+3NaCl
2Fe(OH)3 → Fe2O3 +3H2O
Fe2O3+3H2→ 2Fe+3H2O
Fe+H2SO4→ FeSO4+H2
FeSO4+Ba(NO3)2→ Fe(NO3)2+BaSO4
b)2 Al +3Cl2→ 2AlCl3
AlCl3+3NaOH → Al(OH)3+3NaCl
2Al(OH)3+3Fe(NO3)2→ 2Al(NO3)3+3Fe(OH)2
Al(NO3)3+3NaOH→ Al(OH)3 +3NaNO3
Al(OH)3→ Al2O3 +H2O
2Al2O3→ 4Al+3O2
c) MnO2 +4HCl→ Cl2+2H2O+MnCl2
Cl2+H2→ 2HCl
2HCl+Mg→ MgCl2 +H2
MgCl2+2AgNO3→ Mg(NO3)2 +2AgCl
Mg(NO3)2+3NaOH→ Mg(OH)2 +2NaNO3
Mg(OH)2→ MgO+H2O
Bài 2: Bằng phương pháp hóa học, hãy nhận biết (trình bày bằng sơ đồ):
a. 3 dung dịch: HCl ; Na2SO4 ; KOH.
-Cho QT vào
+Làm QT hóa đỏ là HCl
+Làm QT hóa xanh là KOH
+K làm QT đổi màu là Na2SO4
b. 4 dung dịch: HCl ; H2SO4 ; NaOH ; NaCl
Cho QT vào
+Làm QT hóa xanh là HCl,H2SO4(N1)
+Làm QT hóa xanh là NaOH
+Ko làm QT đổi màu NaCl
-Cho dd BaCl2 vào N1
+Tạo kết tủa trawsg là H2SO4
H2SO4+BaCl2--->2HCl+BaSO4
+K có ht là HCl
c. 4 d: HNO3 ; NaOH ; Ca(OH)2 ; HCl
-Cho QT vào
=Làm QT hóa đỏ là HCl và HNO3(N1)
+Làm QT hóa xanh là NaOH,Ca(OH)2(N2)
+Códd AgNO3 vào N1
+Tạo kết tủa trắng là HCl
HCl+AgNO3--->AgCl+HNO3
+K có hiện tượng là HNO3
-Sục khí CO2 vào 2 dd Ca(OH)2 và NaOH
+Tạo kết tủa là Ca(OH)2
Ca(OH)2+CO2--->CaCO3+H2O
+K có ht là NaOH
NaOH+CO2--->Na2CO3+H2O
d. 3 kim loại: Al ; Fe ; Cu
-Cho qua dd HCl
+Tạo khí là Fe và Al(N1)
Fe+2HCl--->FeCl2+H2
2Al+6HCl--->2AlCl3+3H2
+ k có ht là Cu
-Cho dd NaOH dư vào N1
+Tạo khí là Al
2Al+2H2O+2NaOH----->2NaAlO2+3H2
+K có ht là Fe
f. 2 oxit bazơ: CaO và MgO
Cho vào nước
+Tan là CaO
CaO+H2O--->Ca(OH)2
+K tan là MgO

Phùng Hà ChâudungHà Yến NhiHoàng Thảo LinhNguyen PhamHắc Hường
a). \(NaOH+H_2SO_4;NaOH+MgCO_3;NaOH+CuSO_4;NaOH+CO_2;NaOH+Al_2O_3;\\ H_2SO_4+BaCl_2;H_2SO_4+MgCO_3;H_2SO_4+Cu\left(t^o\right);H_2SO_4+Fe;\\ BaCl_2+CuSO_4;BaCl_2+MgCO_3\)
b).
\(CuO+HCl;\\ MnO_2+NaOH\\ SiO_2+HCl;SiO_2+NaOH\\ HCl+NaOH\)
C).
\(H_2O+MgCl_2;H_2O+CO_2;H_2O+CuO;\\ HCl+CO_2;HCl+Ba\left(OH\right)_2;HCl+Fe;HCl+Fe\left(OH\right)_3\\ MgCl_2+Ba\left(OH\right)_2\\ CO_2+Ba\left(OH\right)_2\)
d). \(CuSO_4+Ba\left(OH\right)_2;HCl+Ba\left(OH\right)_2;HCl+Fe\)
e).
\(Cu+Cl_2;Cu+HCl\left(t^o\right)\\ Fe_2O_3+CO;Fe_2O_3+Al;Fe_2O_3+HCl;\\ Cl_2+CO;Cl_2+Al;Cl_2+NaOH;\\ CO+HCl;CO+NaOH;\\ Al+HCl;Al+NaOH\\ HCl+NaOH\)