Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

(a) v tăng lên 83 lần
(b) v tăng lên 23 = 8 lần
(c) v tăng lên 4.22 = 16 lần
(d) v tăng lên 42/2 = 8 lần
Đáp án B

Đáp án C
Tốc độ phản ứng tức thời: v = k[H2]3.[N2]
Vậy khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên 23 = 8 lần.

Đáp án C
Tốc độ phản ứng tức thời: v = k[H2]3.[N2]
Vậy khi tăng nồng độ H2 lên hai lần (giữ nguyên nồng độ của khí nitơ và nhiệt độ của phản ứng) thì tốc độ phản ứng tăng lên 23 = 8 lần.

Áp suất tăng 2 lần thì thể tích giảm 2 lần nên nồng độ tăng 2 lần và phản ứng xảy ra chiều thuận. Do đó tốc độ phản ứng sẽ tăng 2.2 = 4 lần.

a) Công thức tính tốc độ tức thời của phản ứng là: v1 = k.CNO2.CO2
b)
- Nồng độ O2 tăng 3 lần, nồng độ NO không đổi: v2 = k.CNO2.(CO2.3)
=> v2 tăng 3 lần so với v1
- Nồng độ NO tăng 3 lần, nồng độ O2 không đổi: v3 = k.(CNO.3)2.CO2 = k.CNO2.9.CO2
=> v3 tăng 9 lần so với v1
- Nồng độ NO và O2 đều tăng 3 lần: v4 = k.(CNO.3)2.(CO2.3) = k.CNO2.27.CO2
=> v4 tăng 27 lần so với v1
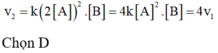
Tốc độ phản ứng tăng 8 lần nếu nồng độ cả 2 chất tăng lên 2 lần là thỏa mãn
A thì tốc độ phản ứng tăng 16 lần
C thì tốc độ phản ứng tăng 4 lần
D thì tốc độ phản ứng tăng 32 lần
Vậy chọn B