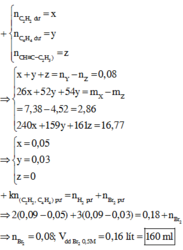Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.


Ta có: \(\left\{{}\begin{matrix}n_{O_2}=\dfrac{5,6.20\%}{22,4}=0,05\left(mol\right)\\n_{N_2}=\dfrac{5,6.80\%}{22,4}=0,2\left(mol\right)\end{matrix}\right.\)
- Hỗn hợp 3 khí gồm: CO2, O2 dư và N2.
\(C+O_2\underrightarrow{t^o}CO_2\)
Gọi: nCO2 = x (mol) ⇒ nO2 (pư) = x (mol) ⇒ nO2 (dư) = 0,05 - x (mol)
Mà: hh khí có tỉ khối so với H2 là 14,88.
\(\Rightarrow\dfrac{44x+32.\left(0,05-x\right)+28n_{N_2}}{x+0,05-x+n_{N_2}}=14,88.2\)
⇒ x = 0,02 (mol)
BTNT C, có: nC = nCO2 = 0,02 (mol)
⇒ m = mC = 0,02.12 = 0,24 (g)

Đáp án A
Sử dụng sơ đồ đường chéo, ta có :
n C 4 H 4 ban đầu n H 2 ban đầu = 32 - 2 52 - 32 = 3 2 = 3 x 2 x
Gọi a là số mol H 2 phản ứng. Theo sự bảo toàn số liên kết π , bảo toàn C và sự tăng giảm số mol khí, ta có :
3 n C 4 H 4 ⏟ 3 x = n Br 2 phản ứng ⏟ 0 , 16 + n H 2 phản ứng ⏟ a n Y = 3 x ⏟ n C 4 H y - + ( 2 x - a ) ⏟ n H 2 dư = 1 , 792 22 , 4 = 0 , 08
⇒ 9 x = 0 , 16 + a 5 x - a = 0 , 08 ⇒ x = 0 , 02 a = 0 , 02
Đốt cháy hỗn hợp Y cũng chính là đốt cháy hỗn hợp X. Theo bảo toàn electron, ta có :
4 n O 2 ⏟ ? = 20 n C 4 H 4 ⏟ 0 , 02 . 3 + 2 n H 2 ⏟ 0 , 02 . 2
⇒ n O 2 = 0,32
⇒ V khong khi ( đktc ) = 0,32.5.22,4 = 35,84 lit

Đáp án A
Chọn 100 mol không khí.
Tỉ lệ thể tích cũng là tỉ lệ số mol nên
![]()
Gọi 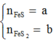
Có
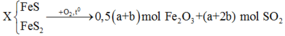

![]()
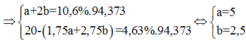

Đáp án A
Xử Lý hỗn hợp khí X: 3 khí đó chỉ có thể là NO, N2 và N2O.
NO + ½O2 → NO2 và bị giữ lại bởi NaOH.
⇒ Hỗn hợp khí Y chứa N2 và N2O với MTrung bình = 36 = MTrung bình cộng của 2 khí.
⇒ nN2 = nN2O || Đặt nNO = a và nN2 = nN2O = b ta có hệ:
a + 2b = 0,04 || 30a + 28b + 44b = 1,32 ||⇒ a = 0,02 và b = 0,01.
⇒ ∑ne cho nhận = 3nNO + 10nN2 + 8nN2O = 0,24 mol.
● Đặt số mol 2 kim loại lần lượt là x và y ta có hệ:
(24+17×2)x + (27+17×3)y = 6,42 || 2x + 3y = 0,24.
⇒ nMg = 0,03 và nAl = 0,06 mol ⇒ mHỗn hợp kim loại = 2,34 gam
+ Bảo toàn nguyên tố Nitơ ⇒ nHNO3 đã pứ = 0,24 + 0,02 + 0,01×2×2 = 0,3 mol.
⇒ ∑nHNO3 ban đầu = 0,3 + 0,3×0,15 = 0,345 mol.
⇒ mDung dịch HNO3 = 0 , 345 × 63 × 100 24 = 90,5625 gam