


Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.




MgCO3 + 2HCl → MgCl2 + CO2 + H2O (1)
BaCO3 + 2HCl → BaCl2 + CO2 + H2O (2)
CO2 + Ca(OH)2 → CaCO3↓ + H2O. (3)
Theo (1), (2) và (3), để lượng kết tủa B thu được là lớn nhất thì:
nCO2 = nMgCO3 + nBaCO3 = 0,2 mol
Ta có:  = 0,2
= 0,2
=> a = 29,89.

Chọn B.
Dung dịch X chứa Mg(NO3)2 và Cu(NO3)2 . Khi cho X tác dụng với Fe thì:
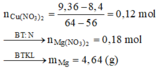

Dung dịch X chứa Mg(NO3)2 (a mol) và Cu(NO3)2 dư (b mol)
Bảo toàn N => 2a + 2b = 0,1 + 0,25.2
X với Fe: ∆ m = 64b - 56b = 9,36 - 8,4
Giải hệ được a = 0,18 và b = 0,12
Trong 19,44 gam kết tủa chứa Ag (0,1), Cu
(0,25 - 0,12 = 0,13) => mMg dư = 0,32
m = 0,18.24 + 0,32 = 4,64
Đáp án C

Đáp án : D
Dung dịch X chứa 2 muối chắc chắn là Cu2+ và Mg2+
Trong kết tủa có thể có Mg chưa kịp phản ứng với Cu2+
Thêm 4,2g Fe và thu được 4,68g > mFe => Phản ứng với Cu2+
=> nCu2+ = (4,68 – 4,2)/(64 – 56) = 0,06 mol
=> Dung dịch muối có 0,09 mol Mg2+ ; 0,06 mol Fe2+(bảo toàn điện tích với NO3-)
Bảo toàn khối lượng :
, m + mAgNO3 + Cu(NO3)2 = mKết tủa + mdd X
,mdd X + mFe = mrắn + mdd sau
=> m = 2,32g

Đáp án C
► Ta có: Mg2+/Mg > Cu2+/Cu > Ag+/Ag || X chứa 2 muối.
||⇒ X gồm Mg(NO3)2 và Cu(NO3)2. Tăng giảm khối lượng:
nFe phản ứng = 0,12 mol < nFe ban đầu ⇒ Fe dư, Cu2+ hết.
⇒ nCu(NO3)2 = 0,12 mol. Bảo toàn gốc NO3: nMg(NO3)2 = 0,18 mol.
► Bỏ qua gốc NO3 (do được bảo toàn), bảo toàn khối lượng gốc kim loại:
||⇒ m = 0,18 × 24 + 0,12 × 64 + 19,44 – 0,1 × 108 – 0,25 × 64 = 4,64(g)

Câu 1/
\(2C\left(\dfrac{m}{12}\right)+O_2\left(\dfrac{m}{24}\right)\rightarrow2CO_2\left(\dfrac{m}{12}\right)\)
\(CO_2\left(\dfrac{m}{12}\right)+Ca\left(OH\right)_2\rightarrow CaCO_3\left(\dfrac{m}{12}\right)+H_2O\)
Nếu như O2 thì tỷ khối của hỗn hợp so với O2 phải là: \(\dfrac{44}{32}=1,375>1,25\) vậy trong hỗn hợp khí phải có O2
\(n_C=\dfrac{m}{12}\left(mol\right)\)
\(n_{O_2}=\dfrac{V}{22,4}\left(mol\right)\)
\(\Rightarrow n_{O_2\left(dư\right)}=\dfrac{V}{22,4}-\dfrac{m}{12}\left(mol\right)\)
\(\Rightarrow\dfrac{44.\dfrac{m}{12}+32.\left(\dfrac{V}{22,4}-\dfrac{m}{24}\right)}{\dfrac{m}{12}+\dfrac{V}{22,4}-\dfrac{m}{24}}=1,25.32=40\)
\(\Leftrightarrow15V-28m=0\left(1\right)\)
Ta lại có: \(n_{CaCO_3}=\dfrac{6}{100}=0,06\left(mol\right)\)
\(\Rightarrow\dfrac{m}{12}=0,06\Leftrightarrow m=0,72\left(2\right)\)
Từ (1) và (2) ta có hệ: \(\left\{{}\begin{matrix}15V-28m=0\\m=0,72\end{matrix}\right.\)
\(\Leftrightarrow\left\{{}\begin{matrix}m=0,72\left(g\right)\\V=1,344\left(l\right)\end{matrix}\right.\)