Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Đáp án A
nHCl = 0,1 (mol)
Ta có X + 2HCl → dung dịch Y + H2
0,1 0,05 (mol)
Kim loại còn phản ứng với nước :
![]()
Dung dịch sau phản ứng : Kim loại, Cl-: 0,1 mol, OH-: 0,1 mol
m dd = m KL + mCl + m OH = 9,95 + 0,1.35,5 + 0,1.17 = 15,2 (gam)

KL kiềm, kiềm thổ ngoài phản ứng với HCl chúng còn phản ứng với H2O
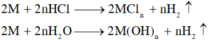
n Cl-= nHCl=2nH2
![]()
Sau phản ứng 2 có xảy ra
nH2(pu2)=nH2 - nH2(pu1)=0,05
![]()
![]()
Đáp án A

Đáp án B
Gọi
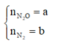
Có
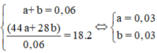
Ta có nAl = 0,46 Þ ne nhường = 3nAl = 1,38mol
Nếu sản phẩm khử có NH4NO3 thì
![]()
Do đó sản phẩm khử có chứa NH4NO3
Áp dụng định luật bảo toàn mol electron, ta có:
n e n h ư ờ n g = n e n h ậ n
![]()

Khi đó
![]()
Chú ý: Đề bài cho đồng thời các dữ kiện để có thể tính được số mol nhôm và số mol các sản phẩm khử là các khí, trong khi để tính được lượng muối nitrat của kim loại thì chỉ cần một trong hai dữ kiện trên.
Khi đó đề bài có vẻ "thừa". Tuy nhiên những bài như vậy thường có sự tạo thành muối amoni nền các bạn cần kiểm tra có sự tạo thành muối này không thông qua việc so sánh giữa số mol electron cho và số mol electron nhận.

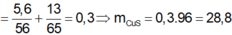



M thuộc nhóm IA => khi cho M vào dung dịch CuSO4 thì M sẽ tác dụng với nước trước.
M + H2O --> MOH + \(\dfrac{1}{2}\)H2
nH2 = \(\dfrac{3,36}{22,4}\)= 0,15 mol => nMOH = 0,15 . 2 = 0,3 mol
nCuSO4 = 0,1. 1 = 0,1 mol
2MOH + CuSO4 --> Cu(OH)2 + M2SO4
0,3 0,1
Theo tỉ lệ phản ứng => MOH dư, CuSO4 hết
nMOH dư = 0,3 - 0,2 = 0,1 mol
Vậy dung dịch X gồm \(\left\{{}\begin{matrix}MOH_{dư}=0,1mol\\M_2SO_4=0,1mol\end{matrix}\right.\)
=> 0,1.(M + 17) + 0,1.(2M + 32 +16.4) = 18,2
=> M = 23 (g/mol)
=>mM = 0,3.23 = 6,9 gam