Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

Phương trình hóa học:
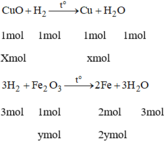
Gọi x là số mol của CuO
y là số mol của F e 2 O 3 .
Ta có: 80x + 160y = 16 (1)
Khối lượng hỗn hợp giảm do oxit tạo thành kim loại:
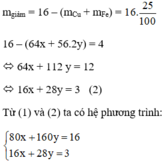
Giải hệ phương trình ta được:
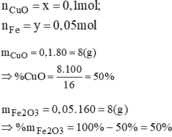

a) PTHH : \(2Al+6HCl-->2AlCl_3+3H_2\) (1)
\(Fe+2HCl-->FeCl_2+H_2\) (2)
\(H_2+CuO-t^o->Cu+H_2O\) (3)
b) Ta có : \(m_{CR\left(giảm\right)}=m_{O\left(lay.di\right)}\)
=> \(m_{O\left(lay.di\right)}=32-26,88=5,12\left(g\right)\)
=> \(n_{O\left(lay.di\right)}=\frac{5,12}{16}=0,32\left(mol\right)\)
Theo pthh (3) : \(n_{H_2\left(pứ\right)}=n_{O\left(lay.di\right)}=0,32\left(mol\right)\)
=> \(tổng.n_{H_2}=\frac{0,32}{80}\cdot100=0,4\left(mol\right)\)
Đặt \(\hept{\begin{cases}n_{Al}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\end{cases}}\) => \(27a+56b=11\left(I\right)\)
Theo pthh (1) và (2) : \(n_{H_2\left(1\right)}=\frac{3}{2}n_{Al}=\frac{3}{2}a\left(mol\right)\)
\(n_{H_2\left(2\right)}=n_{Fe}=b\left(mol\right)\)
=> \(\frac{3}{2}a+b=0,4\left(II\right)\)
Từ (I) và (II) => \(\hept{\begin{cases}a=0,2\\b=0,1\end{cases}}\)
=> \(\hept{\begin{cases}m_{Al}=27\cdot0,2=5,4\left(g\right)\\m_{Fe}=56\cdot0,1=5,6\left(g\right)\end{cases}}\)

$m_{O\ trong\ oxit} = m_{giảm} = 20.24\%= 4,8(gam)$
$\Rightarrow n_O = \dfrac{4,8}{16} = 0,3(mol)$
Gọi $n_{Fe_2O_3} = a(mol) ; n_{CuO} = b(mol) \Rightarrow 160a + 80b = 20(1)$
Ta có : $n_O = 3a + b = 0,3(2)$
Từ (1)(2) suy ra : a = 0,05 ; b = 0,15
$\%m_{CuO} = \dfrac{0,15.80}{20}.100\% = 60\%$

Gọi $n_{Al}= a(mol) ; n_{Fe} = b(mol) \Rightarrow 27a + 56b = 4,44(1)$
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
$Fe_3O_4 + 4H_2 \xrightarrow{t^o} 3Fe + 4H_2O$
B gồm : $Al_2O_3, Fe$
$n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,5a(mol)$
Suy ra: $0,5a.102 + 56b = 5,4(2)$
Từ (1)(2) suy ra a = 0,04 ; b = 0,06
$m_{Al} = 0,04.27 =1,08\ gam$
$m_{Fe} = 0,06.56 = 3,36\ gam$

ta có Ax + By = 23.8 (1) ( dữ kiện : khối lượng hỗn hợp kim loại )
x+ 3y = 0.8 ( dữ kiện : cần 8.96 lít O2 )
và có dữ kiện cuối cùng là hỗn hợp chất rắn sau khi bị khử bởi H2 còn lại 33.4 gam
thì ta tính đọc số mol Oxi còn trong hỗn hợp là 0.6
TH1 chỉ có A bị khử thì số mol oxi trong hỗn hợp trên là của B  3y = 0.6
3y = 0.6  x = 0.2
x = 0.2
mà B hóa trị 3 và không bị khủ thì chỉ có thể là Al  A là Zn
A là Zn
TH2 chỉ có B bị khử ta tính được số mol trong hỗn hợp trên là của A  x =0.6 y = 0.2/3
x =0.6 y = 0.2/3
ta tính : ráp số vào phương trình (1) ta được 0.6A +0.4/3B =23.8
từ đó ta có 23.8 / 0.6 < A,B< 23.8*3/0.4
lúc này ta lục bảng tuần hoàn và thế vô đều không thỏa mãn nên th2 loại
vậy kim loại cần tìm là Zn và Al

FeO + CO -> Fe + CO2
mol: x -> x
pt2: Fe2O3 + CO ->2 Fe + CO2
mol: y -> 2y
theo gt thu được 2.94 g
Fe trong đó có Fe tạo thành và Fe ban đầu và gọi Z là số mol Fe ban đầu
=> ta có Pt : 72x + 160y +56z=3.54 (1)
và x + 2y + z =3.92/56=0.0525 (2)
hh trên vào CuSO4 thì chỉ có Fe phản ứng
pt: Fe + CuSO4 -> FeSO4 + Cu
mol: z -> z
thu được 3.72g rắn gồm Cu , FeO, Fe2O3
=> ta có pt: 72x + 160y + 64Z=3.72 (3)
từ (1),(2),(3) ta có x=0.015= nFeO , y=0.0075 mol =nFe2O3 , z=0.0225 mol=nFe
Có số mol áp dụng công thức m=n*M em tự tính khối lượng các chất nha
Số ko đẹp lắm nên số mol hơi dài,cứ giữ nguyên để tính để tránh sai số
CHÚC EM HỌC TỐT !!!!!!(nhớ hậu tạ nha hi hi.....)




\(Fe_2O_3 + 3CO \xrightarrow{t^o} 2Fe + 3CO_2\)
Gọi \(n_{Fe_2O_3\ pư} = a(mol)\)
Theo PTHH : \(n_{Fe} = 2n_{Fe_2O_3} = 2a(mol)\)
Ta có :
\(m_{hỗn\ hợp} = m_{Al_2O_3} + 160a(gam)\)
\(m_{rắn\ sau\ phản\ ứng} = m_{Al_2O_3} + m_{Fe} = m_{Al_2O_3} + 112a(gam)\)
Ta có :
\(m_{giảm} = 160a - 112a = 36,4(100\% - 86,813\%)\)
Suy ra : a = 0,1
Vậy : \(m_{Fe} = 0,1.2.56 = 11,2(gam)\)
Al2O3+3CO→2Al+3CO2
Fe2O3+3CO→2Fe+3CO2
m kim loại=36,4x86,813%=31,6 g