Hãy nhập câu hỏi của bạn vào đây, nếu là tài khoản VIP, bạn sẽ được ưu tiên trả lời.

\(A/PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\\ Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(B/n_{H_2}=\dfrac{6,72}{22,4}=0,3mol\\ n_{Fe}=a;n_{Zn}=b\\ \Rightarrow\left\{{}\begin{matrix}56a+65b=18,6\\a+b=0,3\end{matrix}\right.\\ \Rightarrow a=0,1;b=0,2\\ m_{Fe}=0,1.56=5,6g\\ m_{Zn}=18,6-5,6=13g\)

a) Đặt: nZn=x(mol); nFe= y(mol) (x,y: nguyên, dương)
Zn + H2SO4 -> ZnSO4 + H2
x_______x_______x________x
Fe + H2SO4 -> FeSO4 + H2
y____y_________y___y(mol)
b) m(rắn)=mCu=3(g)
=> m(Zn, Fe)= 21,6 - 3= 18,6(g)
Ta có hpt:
\(\left\{{}\begin{matrix}65x+56y=18,6\\22,4x+22,4y=6,72\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
=> Zn= 65.0,2=13(g)
=>%mZn= (13/21,6).100=60,185%
%mCu=(3/21,6).100=13,889%
=>%mFe=25,926%
c) nH2SO4=x+y=0,3(mol) =>mH2SO4=29,4(g)
=> mddH2SO4= (29,4.100)/25=117,6(g)

Đặt nFe=a nZn=b(mol)
Từ đó suy ra \(56a+65b=25,1\left(1\right)\)
\(n_{HCl}=0,8\left(mol\right)\\ Fe+2HCl\rightarrow FeCl_2+H_2\\ Zn+2HCl\rightarrow ZnCl_2+H_2\)
Lại suy ra được \(2a+2b=0,8\left(2\right)\)
Suy ra a=0,1 b=0,3 (mol)
\(V_{H_2}=\dfrac{0,8\cdot22,4}{2}=8,96\left(l\right)\\ m_{muoi}=m_{KL}+m_{Cl}=25,1+0,8\cdot35,5=53,5\left(g\right)\\ \%m_{Fe}=\dfrac{0,1\cdot56}{25,1}\cdot100\%\approx22,31\left(\%\right)\\ \%m_{Zn}=100\%-22,31\%=77,69\left(\%\right)\)

\(n_{H_2}=\dfrac{1,12}{22,4}=0,05mol\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,05 0,05
\(m_{Zn}=0,05\cdot65=3,25\left(g\right)\)
\(\Rightarrow m_{Cu}=6,45-3,25=3,2\left(g\right)\)

\(a,n_{H_2}=\dfrac{4,48}{22,4}=0,2mol\\ Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2 0,4 0,2 0,2
\(m_{Zn}=0,2.65=13g\\ m_{ZnO}=29,2-13=16,2g\\ b.n_{ZnO}=\dfrac{16,2}{81}=0,2mol\\ ZnO+2HCl\rightarrow ZnCl_2+H_2O\)
0,2 0,4 0,2
\(m_{HCl}=\left(0,4+0,4\right).36,5=29,2g\\ C_{\%HCl}=\dfrac{29,2}{200}\cdot100\%=14,6\%\\ c.m_{ZnCl_2}=\left(0,2+0,2\right).136=54,4g\)


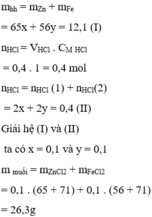
Zn + 2HCl => ZnCl2 + H2 ↑ (1)
Fe + 2HCl => FeCl2 + H2 ↑ (2)
m HCl = 100.29,2% = 29,2 (g)
M HCl = 1 + 35,5 = 36,5 (g/mol)
=> n HCl = \(\dfrac{29,2}{36,5}\) = 0,8 (mol)
Goị số mol của Zn , Fe lần lượt là a , b (mol) ; (a,b > 0)
Theo phương trình (1) , n HCl (1) = 2.n Zn = 2.a (mol)
Theo phương trình (2) , n HCl (2) = 2.n Fe = 2.b (mol)
Có n HCl = n HCl (1) + n HCl (2)
=> 0,8 = 2.a + 2.b (1)
Theo phương trình (1) , n ZnCl2 = n Zn = a (mol)
M ZnCl2 = 65 + 35,5.2 = 136 (g/mol)
=> m ZnCl2 = 136.a (g)
Theo phương trình (2) , n FeCl2 = n Fe = b (mol)
M FeCl2 = 56 + 35,5.2 = 127 (g/mol)
=> m ZnCl2 = 127.b (g)
Theo bài ra , ta có :
m muối = m FeCl2 + m ZnCl2
=> 52,6 = 127.b + 136.a (2)
Từ (1) và (2) => a = 0,2 ; b = 0,2
m Zn = 0,2.65 = 13 (g)
m Fe = 0,2.56 = 11,2 (g)
=> m hỗn hợp = m Zn + m Fe = 13 + 11,2 = 24,2 (g)
=> %m Fe = \(\dfrac{11,2}{24,2}.100\%\) ≃ 46,28 %
=> %m Zn = \(\dfrac{13}{24,2}.100\%\) ≃ 53,72 %